Clear Sky Science · pt
Alnuctamab, um engajador de células T bivalente que mira no antígeno de maturação de células B para pacientes com mieloma múltiplo recidivado ou refratário: resultados de um estudo de fase 1, primeiro em humanos
Por que este novo medicamento contra o câncer importa
Para pessoas vivendo com mieloma múltiplo, um câncer do sangue que quase sempre retorna após o tratamento, cada nova opção pode significar mais tempo e melhor qualidade de vida. Este estudo testa uma imunoterapia de próxima geração chamada alnuctamab, projetada para ajudar as próprias células de defesa do corpo a localizar e matar células de mieloma. A pesquisa faz uma pergunta prática que interessa tanto a pacientes quanto a médicos: seria possível administrar essa terapia potente como uma simples injeção subcutânea, com fortes efeitos anticâncer mas menos efeitos colaterais perigosos?
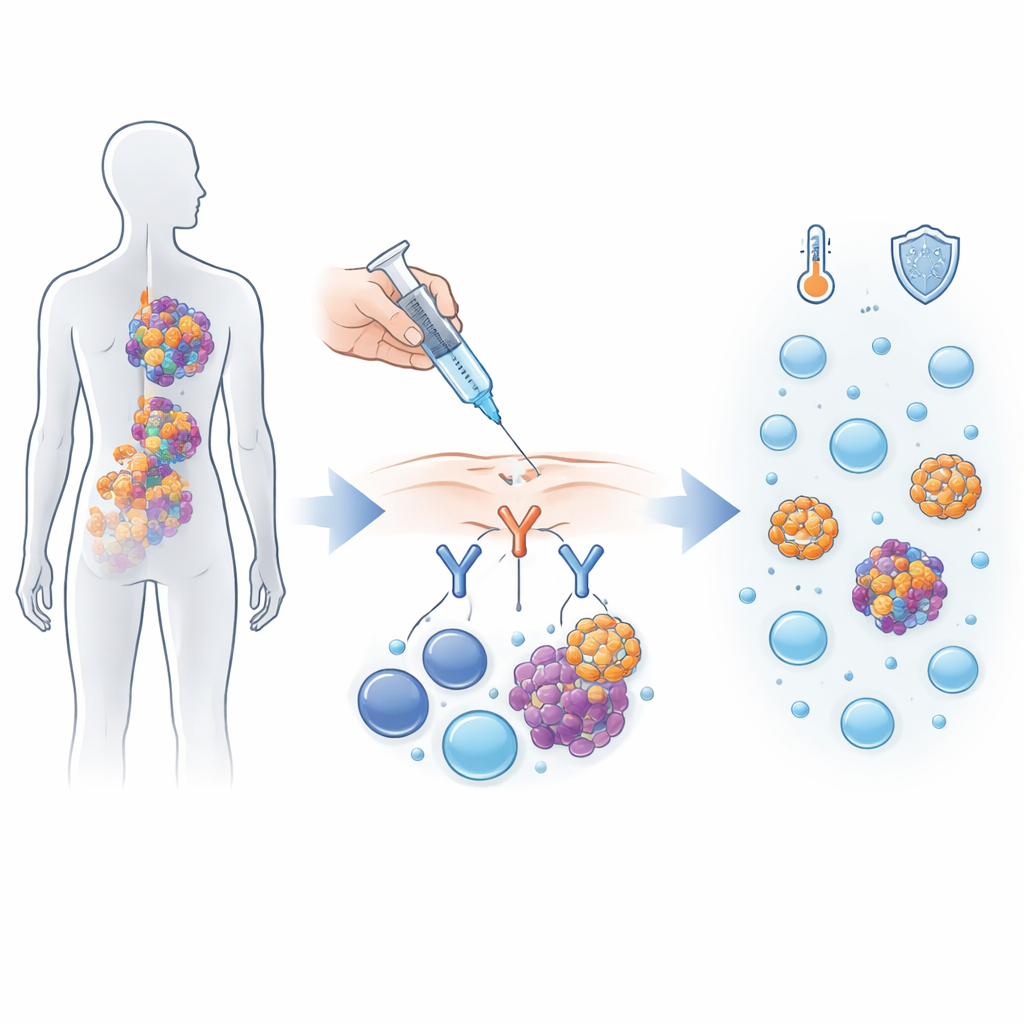
Uma maneira engenhosa de redirecionar o sistema imunológico
Alnuctamab pertence a uma nova classe de medicamentos que atuam como um intermediário molecular entre células cancerosas e células imunes. As células de mieloma carregam um marcador chamado BCMA em sua superfície, enquanto as células T do corpo apresentam um marcador diferente, CD3. Alnuctamab é construído com dois “braços” que se ligam ao BCMA e um braço que se liga ao CD3, aproximando as células T das células de mieloma para que possam atacá‑las. Neste ensaio primeiro em humanos, 165 pessoas com mieloma que havia retornado após pelo menos três tipos diferentes de tratamento receberam alnuctamab, seja por infusão intravenosa ou por injeção subcutânea sob a pele.
Da infusão à injeção
No início, o medicamento foi administrado por via venosa, mas essa abordagem provocou reações imunológicas mais intensas, incluindo um episódio com risco de vida de uma complicação chamada síndrome de liberação de citocinas, na qual o sistema imunológico libera subitamente grandes quantidades de sinais inflamatórios. Por causa dessas preocupações de segurança e de benefício apenas modesto, o estudo mudou para a dose subcutânea, que libera o medicamento de forma mais gradual. Noventa e cinco pacientes foram tratados dessa forma usando um esquema de “aumento gradual”: doses iniciais pequenas seguidas por doses alvo mais altas, com a frequência das injeções reduzida lentamente ao longo do tempo, de semanal para uma vez a cada quatro semanas, caso o tratamento continuasse.
Como os pacientes reagiram e o que enfrentaram
Entre todos os pacientes que receberam as injeções subcutâneas, cerca de 59% viram seu câncer reduzir pelo menos à metade, e quase metade tornou‑se “negativa para doença residual mínima”, o que significa que testes altamente sensíveis não conseguiram mais encontrar células de mieloma na medula óssea. Na dose recomendada de 30 miligramas, as respostas foram ainda mais fortes: cerca de 71% responderam e mais da metade atingiu negatividade para doença residual mínima. Muitos pacientes mantiveram o controle da doença por perto de um ano ou mais, mesmo com o esquema de dose se tornando menos intenso. Os efeitos colaterais foram comuns, mas em sua maioria administráveis. Reações do tipo febre ocorreram em aproximadamente três em cada cinco pacientes, mas todas foram leves ou moderadas. Quedas nos números de glóbulos brancos e infecções ocorreram, refletindo tanto a potência do medicamento quanto o sistema imunológico frágil dos pacientes, porém infecções graves foram menos frequentes do que o relatado com diversos medicamentos semelhantes.
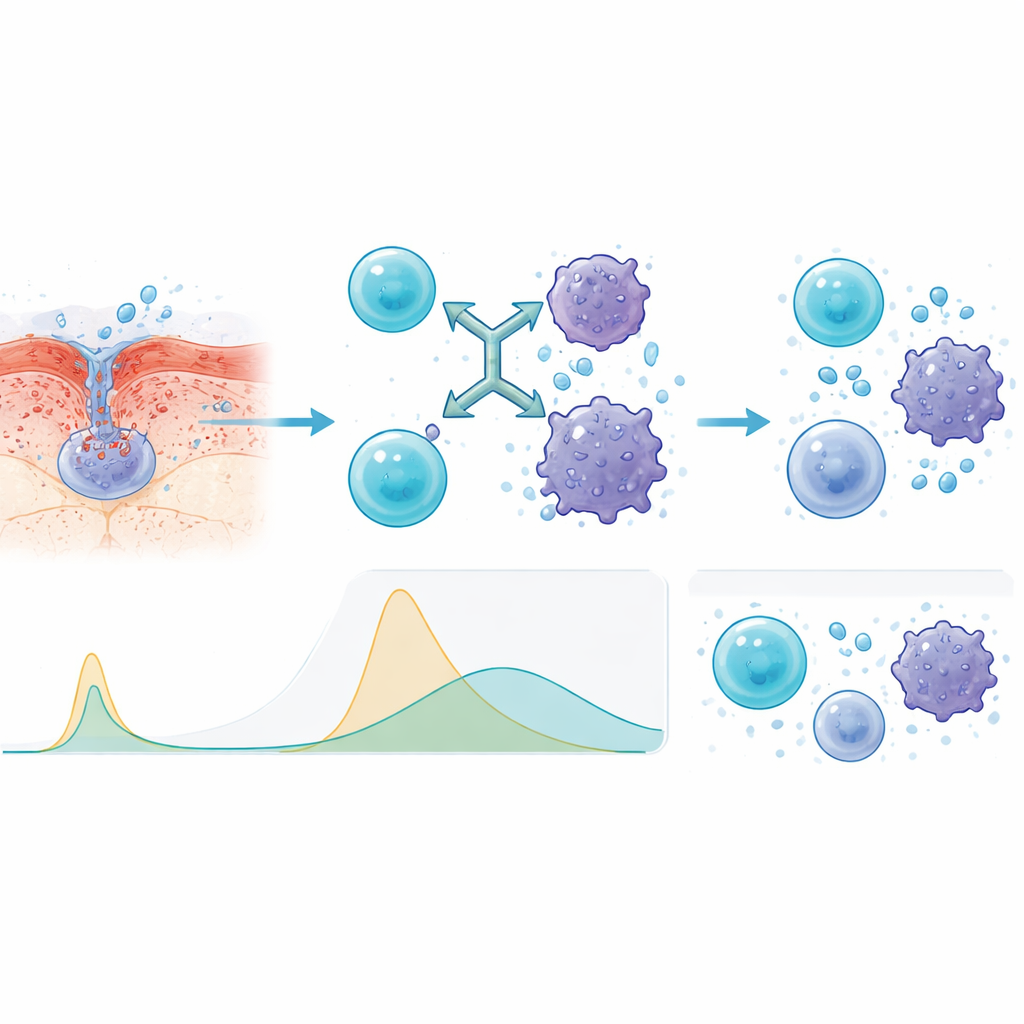
Por que a via de injeção foi mais segura
Para entender por que o método subcutâneo se comportou melhor, os pesquisadores mediram moléculas de sinalização imune no sangue. Comparadas com a infusão intravenosa, as injeções produziram picos mais lentos e mais baixos em sinais inflamatórios-chave, como interleucinas e fator de necrose tumoral. Esse perfil mais achatado significa que o sistema imunológico ainda é ativado contra o câncer, mas sem o mesmo surto súbito que pode deixar os pacientes perigosamente doentes. A equipe também descobriu que pessoas cujo sangue mostrou níveis mais baixos de BCMA shed (BCMA liberado) no início — um sinal de doença menos agressiva ou menos avançada — tenderam a responder melhor e a permanecer em remissão por mais tempo.
O que isso significa para o cuidado futuro do mieloma
Embora a empresa tenha decidido posteriormente não continuar o desenvolvimento do alnuctamab por razões estratégicas, as lições deste ensaio são importantes. O estudo mostra que um engajador imune cuidadosamente desenhado pode ser administrado como uma simples injeção, em um esquema que se torna menos exigente ao longo do tempo, ao mesmo tempo em que produz respostas profundas e duradouras em muitas pessoas com mieloma de difícil tratamento. Também sugere que aumentar gradualmente a dose e evitar picos acentuados na ativação imune pode limitar reações graves sem reduzir o poder anticâncer. Esses insights provavelmente orientarão o desenho de tratamentos imunológicos futuros, oferecendo esperança de que mais pacientes com mieloma recidivado tenham terapias eficazes que sejam não apenas potentes, mas também mais seguras e fáceis de conviver.
Citação: Bar, N., Martin, T., Hofmeister, C.C. et al. Alnuctamab, a bivalent B-cell maturation antigen-targeting T cell engager for patients with relapsed or refractory multiple myeloma: results from a phase 1, first-in-human study. Leukemia 40, 481–490 (2026). https://doi.org/10.1038/s41375-025-02841-x
Palavras-chave: mieloma múltiplo, imunoterapia, anticorpo biespecífico, BCMA, engajador de células T