Clear Sky Science · pt
A implantação desperta o potencial osteogênico peri-implantar via transdução mecânica mediada pelo eixo Snx5-EGFR
Por que conservar o osso mandibular após a perda dentária importa
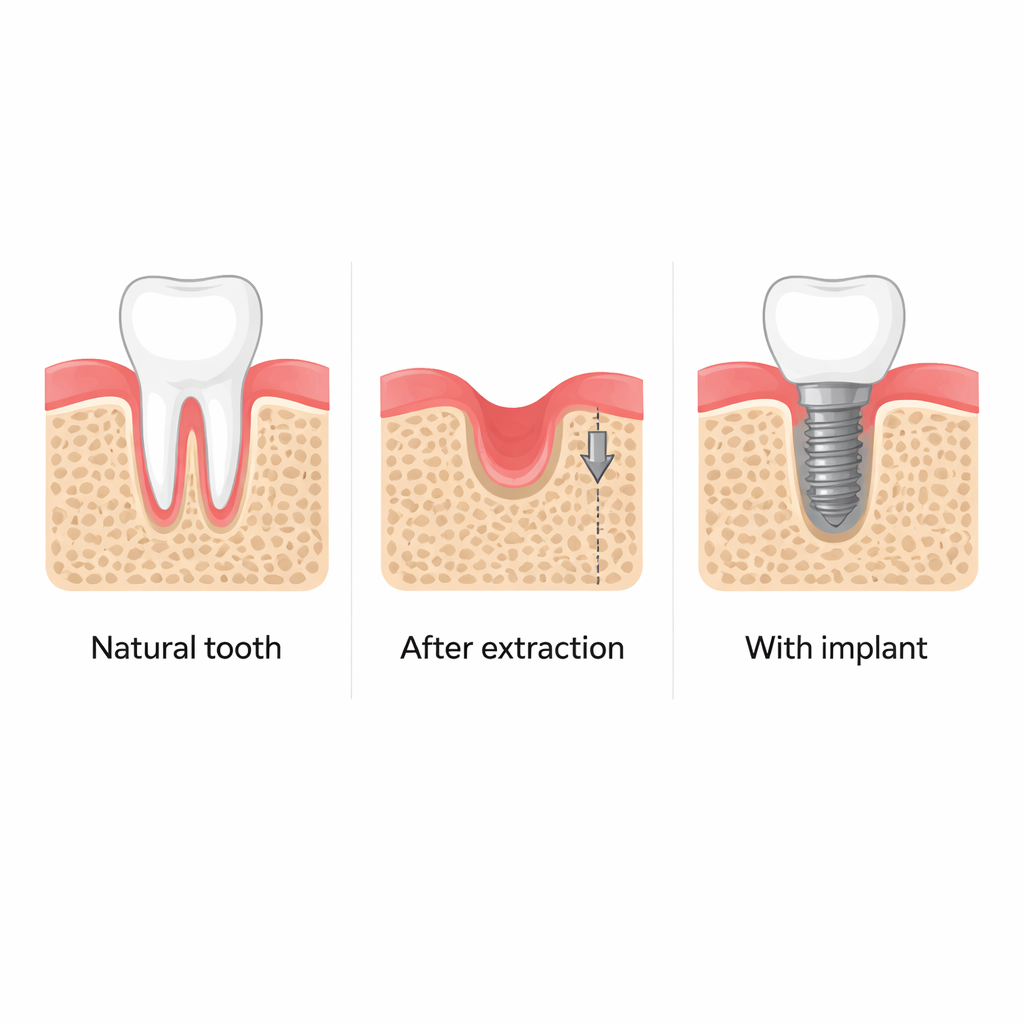
Quando um dente é extraído, o osso alveolar ao redor costuma retrair, dificultando a colocação de implantes dentários estáveis mais tarde e afetando a aparência facial. Há muito tempo os dentistas observam que simplesmente inserir um implante em um alvéolo recém-extraído parece ajudar a preservar esse osso, mesmo antes do implante ser usado na mastigação. Este estudo faz uma pergunta simples, porém importante: como o ato de posicionar o implante em si “desperta” o sistema de reparo ósseo, e podemos aproveitar esse processo para melhorar a regeneração mandibular?
Implantes como protetores silenciosos do osso
Exames clínicos de pacientes e experimentos detalhados em camundongos confirmam que colocar um implante dentário logo após a extração ajuda a manter a altura e a espessura do osso mandibular adjacente. Em contraste, alvéolos deixados para cicatrizar por conta própria perdem quantidade substancial de osso ao longo de vários meses. Em torno dos implantes, os pesquisadores encontraram mais células imaturas formadoras de osso (osteoprogenitoras), indicando que o tecido próximo ao pino metálico está biologicamente mais ativo. Essa atividade aumentada parece ser impulsionada não pelas forças de mastigação, mas pelos esforços mecânicos incomuns gerados quando um implante justo é rosqueado em um osso ligeiramente subdimensionado.
Um interruptor oculto dentro das células-tronco ósseas
A equipe concentrou-se em um grupo especial de células-tronco da medula óssea marcadas por uma proteína chamada LepR, conhecidas por serem fornecedoras-chave de novo osso em adultos. Ao comparar a atividade gênica dessas células em osso normal, em osso adjacente a implantes e em células submetidas a estresse no laboratório, eles focalizaram uma molécula, a sorting nexin 5 (Snx5), cujos níveis caíam consistentemente quando sinais mecânicos estavam presentes. Nas regiões ao redor dos implantes, células LepR com baixo Snx5 eram mais propensas a exibir marcadores de células formadoras de osso em estágio inicial, sugerindo que reduzir Snx5 ajuda a empurrar essas células-tronco silenciosas para um estado ativo de formação óssea.
Quando o interruptor está quebrado, o osso não percebe a força corretamente
Para testar o papel real de Snx5, os pesquisadores usaram camundongos e células-tronco sem essa proteína. Sem Snx5, as células-tronco exibiram uma forte tendência intrínseca a formar osso, mesmo sem estímulos adicionais. Mas quando os cientistas aplicaram alongamento mecânico — imitando as tensões próximas a um implante — células normais aumentaram sua atividade formadora de osso, enquanto células deficientes em Snx5 quase não responderam. Em camundongos vivos, implantes em animais normais desencadearam claro crescimento de novo osso ao redor do pino de titânio. Em contraste, camundongos sem Snx5 não ganharam osso adicional após a implantação, revelando que Snx5 é crucial para converter sinais mecânicos em reparo ósseo adicional, e não para a formação óssea de base por si só.
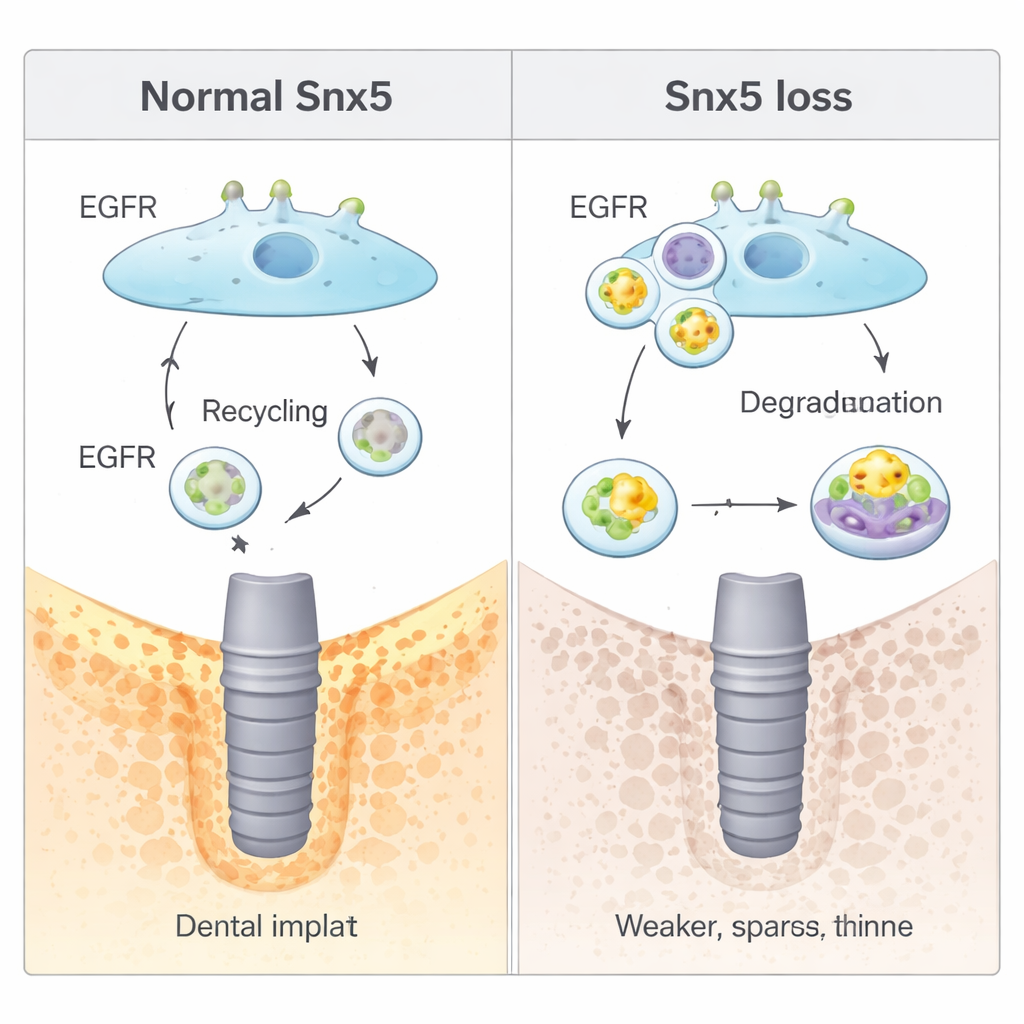
Como uma via de reciclagem controla sinais ósseos
O estudo então revelou como Snx5 atua ao nível molecular. Muitos sinais de crescimento nas células viajam através de receptores na superfície celular que são constantemente internalizados e então reciclados ou destruídos. Snx5 pertence a uma família de proteínas de “ordenamento” que guiam esse tráfego. Aqui, mostrou‑se que Snx5 direciona o receptor do fator de crescimento epidérmico (EGFR) — um controlador chave do crescimento celular e da diferenciação óssea — de volta para a membrana celular após sua internalização. Quando Snx5 estava ausente, mais EGFR era desviado para compartimentos “digestivos” celulares (lisossomos) e degradado. Isso reduziu a sinalização do EGFR e, de forma inesperada, aumentou a formação óssea basal, mas deixou as células menos capazes de ajustar seu comportamento quando as forças mecânicas mudavam. Fármacos que ativaram artificialmente o EGFR atenuaram a formação óssea extra observada sem Snx5, enquanto fármacos que bloquearam a degradação lisossomal restauraram os sinais do EGFR e novamente reduziram a formação óssea.
O que isso significa para futuros pacientes de implantes
Para leigos, esses achados sugerem que o osso mandibular contém um sistema embutido que pode sentir o sutil empurrar e puxar criado quando um implante é colocado e traduzir isso em crescimento ósseo adicional. Snx5 atua como um controlador de tráfego que mantém um receptor de crescimento chave, o EGFR, circulando no nível certo para que as células‑tronco ósseas possam “ouvir” e responder a esses sussurros mecânicos. Quando esse controlador é alterado, o osso pode formar‑se mais facilmente em repouso, mas perde sua resposta fina às forças. Compreender esse eixo Snx5–EGFR abre a porta para novos tratamentos — fármacos ou revestimentos de superfície em implantes — que poderiam ajustar a sensibilidade mecânica do osso, ajudando a preservar a mandíbula e melhorar o sucesso dos implantes em situações clínicas desafiadoras.
Citação: Jiang, X., Weng, Y., Feng, Y. et al. Implantation awakens peri-implant osteogenic potential via Snx5-EGFR axis-mediated mechanical transduction. Int J Oral Sci 18, 18 (2026). https://doi.org/10.1038/s41368-025-00423-2
Palavras-chave: implantes dentários, regeneração do osso mandibular, mecanotransdução, células-tronco ósseas, sinalização EGFR