Clear Sky Science · pt
Caminho glicolítico KDM6B/Pdk1 impulsiona lactilação de ZEB2 e promove a formação de cemento celular
Por que proteger as raízes dos dentes é importante
Doença da gengiva, ou periodontite, é uma das principais causas de perda dentária em adultos. À medida que a doença avança, ela corrói silenciosamente os tecidos que ancoram os dentes ao maxilar. Um dos mais importantes é o cemento, uma camada fina semelhante ao osso que reveste a superfície da raiz e permite que o dente se fixe ao ligamento e ao osso circundantes. Uma vez perdido o cemento, os dentes afrouxam e podem eventualmente cair. Este estudo coloca uma pergunta simples, porém poderosa: podemos entender, em detalhe molecular, como o cemento é construído, para que um dia possamos ajudar o organismo a reconstruí‑lo e manter os dentes no lugar por toda a vida?
Das células que sustentam o dente a um alvo terapêutico
O cemento é produzido por células especializadas chamadas cementoblastos, que se dispõem sobre a superfície da raiz e depositam novo mineral. Essas células se comportam de forma muito semelhante às que formam os ossos, mas os sinais que lhes dizem quando e como construir o cemento foram pouco compreendidos. Os pesquisadores focaram em uma molécula chamada KDM6B, uma enzima que edita marcas químicas nas proteínas que compactam o DNA e pode ativar genes. Estudando dentes de camundongos em idades diferentes e cementoblastos cultivados em laboratório, eles descobriram que os níveis de KDM6B aumentam durante a fase ativa de formação do cemento e caem quando o crescimento diminui. Quando bloquearam KDM6B em células ou em camundongos, a atividade dos cementoblastos reduziu e a porção “celular” do cemento — a parte mais espessa e viva próxima ao ápice radicular — tornou‑se mais fina, sugerindo que KDM6B é um promotor chave do crescimento saudável do cemento.
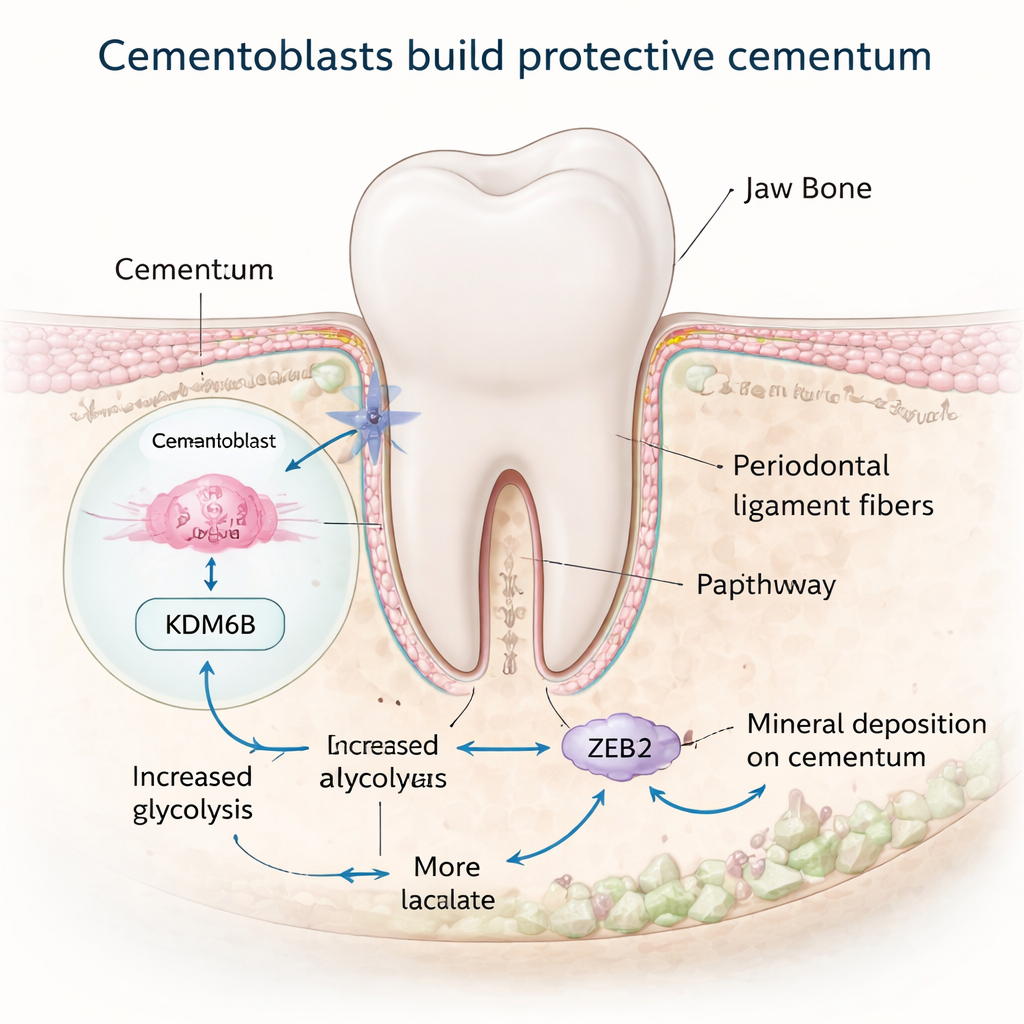
Reconfigurando o metabolismo celular para construir mineral
Construir tecido mineralizado exige muita energia, e muitas células mudam seu metabolismo para um estado de alta potência enquanto o fazem. A equipe descobriu que KDM6B ajuda os cementoblastos a reconfigurar o uso de glicose. Normalmente, essas células favorecem uma via chamada glicólise, que quebra rapidamente a glicose e produz lactato. Quando KDM6B foi reduzido, genes envolvidos na glicólise foram rebaixados, enquanto aqueles ligados a uma produção de energia mais lenta e dependente de oxigênio foram mistos ou aumentaram, e as células produziram menos energia no geral. Um ator central nessa mudança foi a enzima PDK1. Usando ferramentas de mapeamento do genoma, os pesquisadores mostraram que KDM6B remove fisicamente uma marca repressora da região do DNA que controla o gene Pdk1, permitindo que os níveis de PDK1 subam. Restaurar PDK1 em células deficientes em KDM6B recuperou muitos marcadores de formação mineral, revelando um interruptor metabólico KDM6B–PDK1 que alimenta os cementoblastos.
Transformando o lactato de resíduo em sinal útil
O lactato é frequentemente visto como um produto residual de músculos esforçados, mas trabalhos recentes mostram que ele também pode atuar como sinal que modifica proteínas. Aqui, a glicólise mais alta impulsionada por KDM6B e PDK1 aumentou a produção de lactato nos cementoblastos. Os pesquisadores então rastrearam um tipo mais recente de modificação protéica chamada lactilação, na qual marcas derivadas do lactato são ligadas a sítios específicos de proteínas. Eles constataram que os níveis de lactilação nos cementoblastos aumentaram durante períodos de formação ativa do cemento e diminuíram em camundongos mais velhos e em células deficientes em KDM6B. Adicionar lactato de sódio simples ao sistema elevou a lactilação, reativou genes ligados ao mineral e restaurou a formação de nódulos minerais tanto em células cultivadas quanto em um modelo murino, mesmo quando KDM6B estava bloqueado. Isso sugere que o próprio lactato pode ajudar a resgatar a atividade de construção do cemento enfraquecida.
Um impulso molecular para um regulador chave do cemento
A equipe então perguntou quais proteínas eram “decoradas” pela lactilação de maneira relevante para o cemento. Eles se concentraram em ZEB2, uma proteína reguladora de genes já conhecida por promover a mineralização dos cementoblastos. Usando técnicas de mapeamento proteico, identificaram pontos específicos em ZEB2 que carregam marcas de lactilação e mostraram que alterar um sítio crítico enfraqueceu a capacidade da célula de ativar genes de mineralização. Experimentos adicionais demonstraram que a via KDM6B–PDK1 aumenta a lactilação de ZEB2 e que fornecer lactato extra pode restaurar a atividade de ZEB2 quando PDK1 está baixo. Em essência, metabolismo e controle gênico estão ligados: a quebra do açúcar alimenta a produção de lactato, que então ajusta finamente ZEB2 para manter os programas de construção do cemento funcionando vigorosamente.
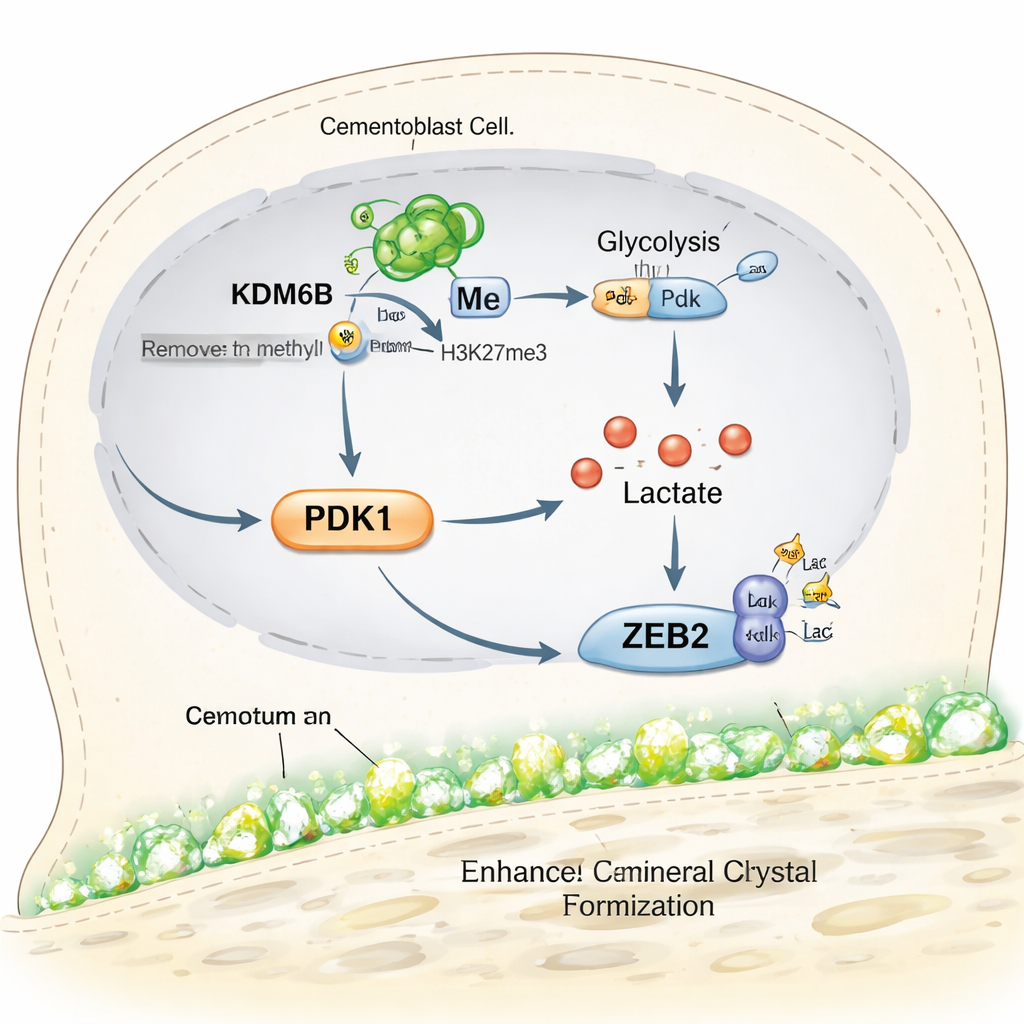
O que isso significa para futuras terapias de preservação dentária
Em termos simples, o estudo revela uma cadeia de eventos dentro das células formadoras de cemento: a enzima KDM6B abre o gene Pdk1, PDK1 empurra as células para o uso rápido de açúcar, esse metabolismo gera lactato, e o lactato ajusta quimicamente a proteína ZEB2 para impulsionar a deposição mineral. Quando qualquer etapa dessa cadeia é bloqueada, o crescimento do cemento enfraquece, mas adicionar lactato de forma controlada pode restaurá‑lo parcialmente. Para pacientes, este trabalho ainda não se traduz em um tratamento clínico, mas destaca alvos novos e precisos para medicamentos ou biomateriais projetados para regenerar o cemento e estabilizar dentes em doenças gengivais avançadas. Também sugere que “interruptores” metabólicos semelhantes poderiam ser aproveitados para incentivar a cicatrização óssea em outras partes do corpo.
Citação: Yang, Z., Wang, H., Xiao, J. et al. KDM6B/Pdk1 glycolytic pathway-driven ZEB2 lactylation promotes cellular cementum formation. Int J Oral Sci 18, 21 (2026). https://doi.org/10.1038/s41368-025-00420-5
Palavras-chave: regeneração do cemento, periodontite, metabolismo de cementoblastos, desmetilase de histonas KDM6B, lactilação de proteínas