Clear Sky Science · pt
Percepções estruturais sobre mutações associadas a doenças na maquinaria de processamento de microRNA
Como Tesouras de RNA Minúsculas Moldam Saúde e Doença
Dentro de cada célula, um sistema de edição oculto aparafusa mensagens genéticas antes que sejam lidas. Esse sistema depende de pequenos fragmentos de RNA chamados microRNAs, que atuam como botões de ajuste fino para milhares de genes ao mesmo tempo. Quando as “máquinas” moleculares que produzem microRNAs funcionam corretamente, as células crescem, se dividem e se especializam de forma controlada. Mas quando essas máquinas são danificadas por mutações, o equilíbrio da atividade gênica pode pender para o câncer, transtornos sanguíneos ou problemas no desenvolvimento cerebral. Este artigo explica como entender as formas 3D dessas máquinas ajuda os cientistas a identificar o que dá errado e como isso pode ser corrigido.
O Kit de Atenuação de Genes da Célula
MicroRNAs são pedaços curtos de RNA, com cerca de 22 blocos construtores, que não codificam proteínas. Em vez disso, eles se anexam a mensageiros de RNA mais longos e ou os marcam para destruição ou bloqueiam sua tradução, efetivamente reduzindo a atividade gênica em vez de desligá-la completamente. Para produzir esses microRNAs, as células fazem passar precursores de RNA mais longos por uma linha de montagem cuidadosamente escalonada. Primeiro, a enzima DROSHA corta grandes transcritos primários no núcleo celular em pedaços mais curtos em forma de alfinete de cabelo. Essas peças então se deslocam para o citoplasma, onde outra enzima, DICER, mede e corta em duplexes do tamanho de microRNA. Finalmente, uma fita de cada duplex é carregada em uma proteína chamada Argonaute 2 (AGO2), que usa o microRNA como guia para encontrar mensagens correspondentes e silenciá-las. 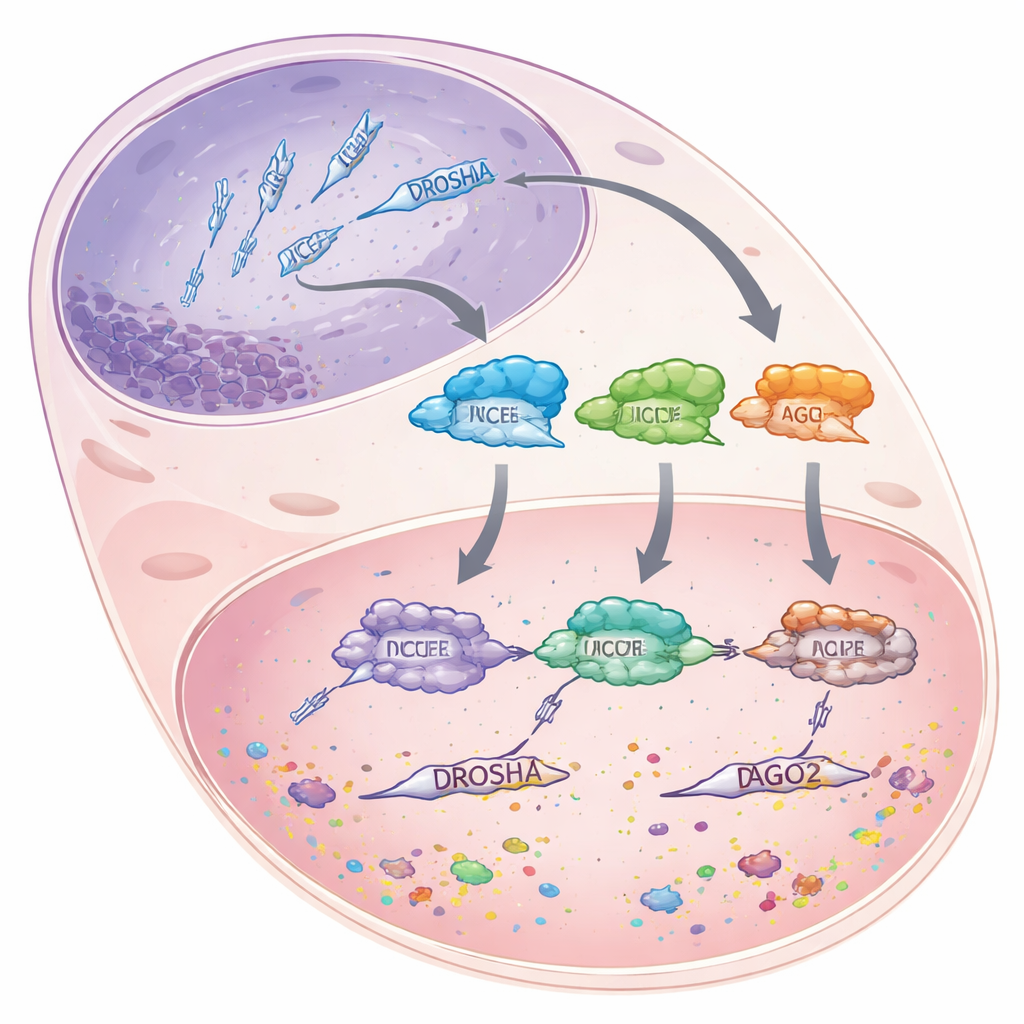
Formas Delicadas com Funções de Precisão
DROSHA, DICER e AGO2 não são tesouras simples; cada um é construído a partir de várias partes que interagem e devem se mover de forma coreografada. DROSHA atua junto com uma proteína parceira, DGCR8, para segurar as extremidades de um penteado primário de microRNA e julgar exatamente onde cortar. DICER usa uma espécie de régua interna formada por seus domínios para definir uma distância fixa entre onde segura a extremidade do alfinete de cabelo e onde seu centro catalítico realiza o corte. AGO2 envolve uma única fita de microRNA de modo que sua região “seed” fique perfeitamente exposta para reconhecer mensagens-alvo, enquanto íons metálicos e aminoácidos-chave em seu núcleo se alinham para fatiar esses alvos quando o pareamento é suficientemente forte. Em todas as três proteínas, sulcos carregados positivamente e elos flexíveis guiam as fitas de RNA ao lugar certo, enquanto bolsões de ligação a metais e resíduos catalíticos efetuam as clivagens químicas.
Quando as Tesouras Estão Entortadas ou Cegas
Estudos genéticos em pacientes com câncer, doenças sanguíneas e síndromes do neurodesenvolvimento revelaram aglomerados de mutações nessas máquinas de microRNA. Muitas das alterações mais danosas residem diretamente em centros catalíticos ou em superfícies de aperto estritas ao RNA. Em DROSHA, por exemplo, substituições como E1147K e D1219G situam-se no coração do sítio de corte e prejudicam a capacidade de reter íons metálicos essenciais, deixando a enzima incapaz de processar microRNAs primários. Outras mutações em DROSHA, como truncações que removem a região de corte ou mudanças que desestabilizam seus helices de suporte, enfraquecem todo o complexo e causam quedas globais nos níveis de microRNA em tumor de Wilms, desordens da medula óssea e doenças do sistema nervoso. Em DICER, mutações recorrentes se agrupam em um de seus dois domínios de corte, distorcendo a produção de modo que um braço do duplex de microRNA se perde, o que desloca o equilíbrio entre sinais promotores e supressores do crescimento. 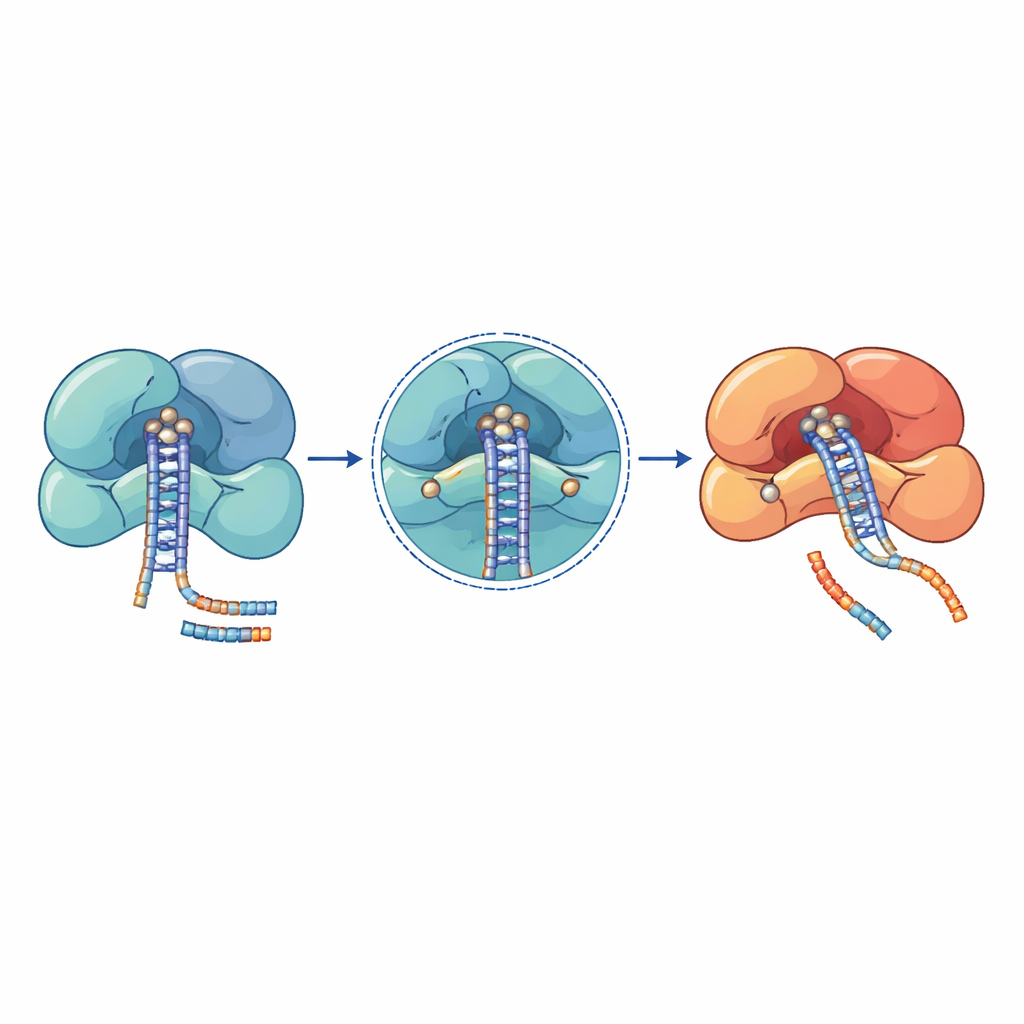
Guias Desalinhados no Cérebro e Além
As mutações em AGO2 contam uma história diferente, mas relacionada. Acertos diretos em seu núcleo catalítico são raros, provavelmente porque seriam letais no início do desenvolvimento. Em vez disso, variantes associadas a doenças tendem a aparecer em regiões de elos flexíveis e nas junções de domínios que mantêm a forma de AGO2. Na síndrome de Lessel–Kreienkamp, uma condição do neurodesenvolvimento, mutações nesses elos e nas superfícies ao redor torcem sutilmente como as partes PAZ, MID e PIWI de AGO2 se empacotam e se movem. Isso pode desalinha o microRNA guia ou enfraquecer sua aderência a RNAs-alvo, borrando a precisão do silenciamento gênico durante o desenvolvimento cerebral. Mudanças estruturais similares em qualquer ponto da via do microRNA — seja em DROSHA, DICER ou AGO2 — podem se propagar, alterando redes inteiras de genes envolvidas no crescimento celular, na formação do sangue ou na fiação neuronal.
Transformando Pistas Estruturais em Tratamentos Futuros
Sobrepondo mutações de doença a mapas 3D de alta resolução dessas proteínas, os pesquisadores podem classificar exatamente como cada alteração causa problema — quer seja embotando a lâmina de corte, afrouxando contatos críticos com proteínas parceiras ou dobrando hélices-chave fora de alinhamento. Essas percepções estruturais abrem a porta para intervenções direcionadas: pequenas moléculas que estabilizam interfaces enfraquecidas, RNAs desenhados que guiem enzimas parcialmente funcionais de volta aos substratos corretos, ou compostos alostéricos que impulsionem proteínas mutantes a formas mais ativas. Para um observador leigo, a mensagem é que pequenos ajustes estruturais nas tesouras de RNA da célula podem ter efeitos desproporcionais na saúde, mas também fornecem alças precisas para projetar terapias de próxima geração atentas às mutações.
Citação: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
Palavras-chave: microRNA, interferência por RNA, DROSHA DICER AGO2, genética do câncer, trastornos do neurodesenvolvimento