Clear Sky Science · pt
Mecanismos regulatórios para a estabilidade da proteína Snail: sistema ubiquitina–proteassoma e autofagia mediada por chaperona
Por que a disseminação do câncer depende de uma proteína frágil
O câncer se torna verdadeiramente ameaçador quando células se desprendem do tumor original e migram para órgãos distantes. Essa disseminação, ou metástase, depende em parte de uma poderosa proteína “chave-mestra” chamada Snail, que ajuda as células a afrouxarem suas ligações e se tornarem mais móveis. Este artigo explica como nossas células normalmente mantêm a Snail sob controle rígido, degradando-a rapidamente por meio de dois grandes sistemas de eliminação de resíduos. Compreender esse equilíbrio oferece novas ideias para desacelerar ou prevenir a metástase.
De células compactas a invasoras errantes
Em tecidos saudáveis, células epiteliais formam camadas ordenadas, semelhantes a tijolos, que permanecem no lugar e aderem firmemente às vizinhas. Para que uma célula tumoral escape, ela frequentemente passa por uma transformação chamada transição epitélio–mesênquima, ou TEM, na qual perde seus contatos estreitos e ganha capacidade de se mover e invadir. A Snail é um motor chave dessa transformação: quando presente no núcleo celular, ela desliga genes que mantêm a adesão célula–célula e ativa genes que favorecem movimento e invasão. Altos níveis de Snail estão ligados a cânceres agressivos e a piores desfechos para pacientes, por isso as células evoluíram mecanismos para manter a Snail escassa e de curta duração em condições normais.
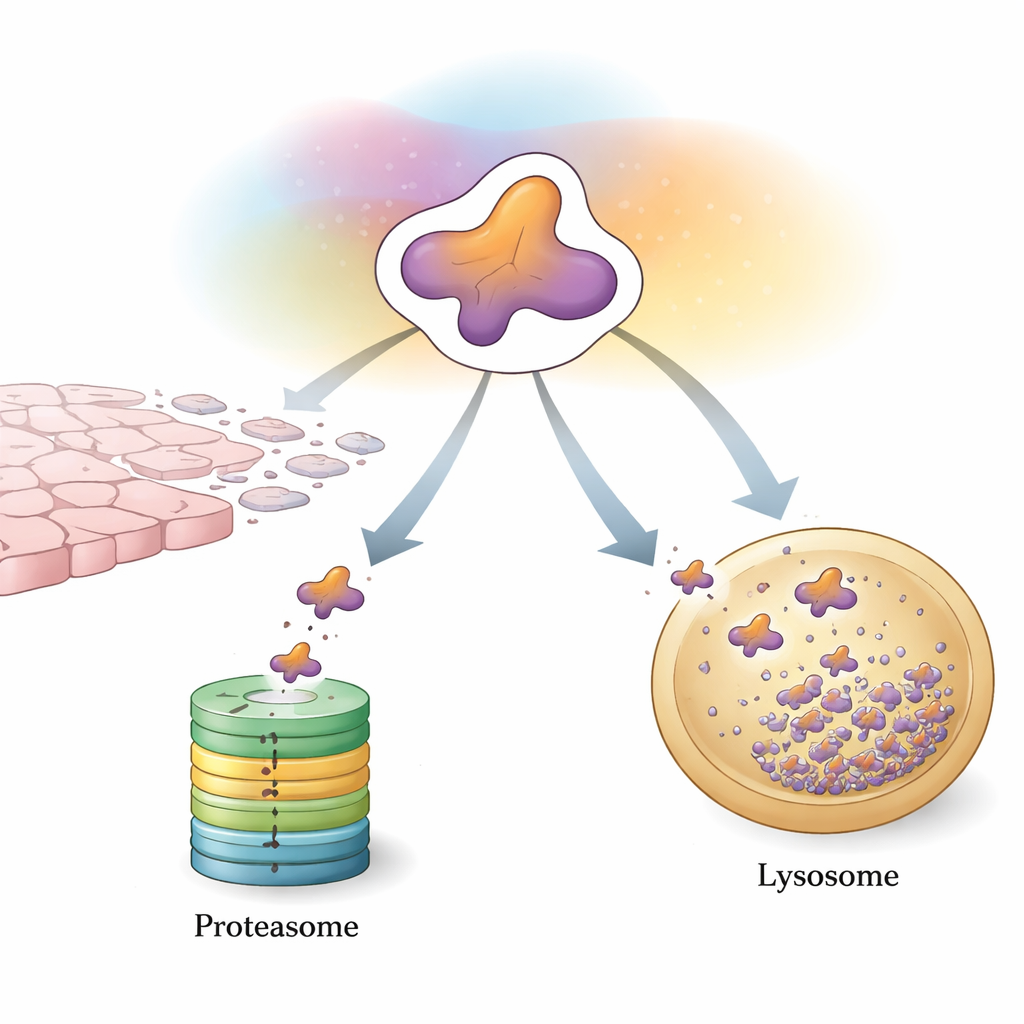
Primeira linha de controle da célula: marcar e triturar
Uma das principais maneiras pelas quais as células controlam a Snail é por meio do sistema ubiquitina–proteassoma, uma máquina de marcar e triturar proteínas indesejadas. Enzimas especializadas anexam pequenas “bandeiras” feitas de uma proteína chamada ubiquitina à Snail. Quando um número suficiente dessas bandeiras se acumula em um padrão específico, a Snail é direcionada ao proteassoma, um complexo em forma de barril que a fragmenta. Um grande elenco de proteínas auxiliares ajusta finamente esse processo. Algumas enzimas adicionam cadeias que promovem a degradação e enviam rapidamente a Snail ao triturador, ajudando a conter o crescimento e a disseminação tumoral. Outras acrescentam cadeias que, em vez disso, estabilizam a Snail ou aumentam indiretamente sua produção gênica, deslocando o equilíbrio em favor da TEM e da metástase. Modificações químicas como fosforilação e acetilação funcionam como interruptores adicionais, controlando quais auxiliares podem se ligar à Snail e se ela será destruída ou poupada.
Removendo os freios: enzimas que resgatam a Snail
A história não termina com a marcação da Snail para destruição. Outro grupo de enzimas, chamadas desubiquitinases, pode remover as bandeiras de ubiquitina, resgatando a Snail do proteassoma. Muitas dessas enzimas são ativadas ou fortalecidas em cânceres, permitindo que a Snail escape da degradação e persista no núcleo. Suas ações dependem fortemente do contexto celular: em alguns cenários elas estabilizam diretamente a Snail, enquanto em outros influenciam onde a Snail se localiza na célula ou como interage com proteínas parceiras. Sinais de vias associadas ao câncer, como fatores de crescimento e respostas ao estresse, alimentam essa rede, decidindo se a Snail será removida rapidamente ou autorizada a conduzir o programa de TEM.
Uma segunda rede de segurança: entrega seletiva ao centro de reciclagem celular
Além do proteassoma, as células dependem da autofagia, um conjunto de vias que transportam proteínas para compartimentos ácidos chamados lisossomos para degradação. Esta revisão destaca uma forma altamente seletiva conhecida como autofagia mediada por chaperona (AMC) como uma segunda rota importante para controlar a Snail. A AMC reconhece uma curta sequência dentro da Snail e, com a ajuda de proteínas escolta, entrega a Snail citoplasmática aos lisossomos para destruição. Em células de câncer de mama menos agressivas, esse sistema mantém a Snail em grande parte fora do núcleo e suscetível à remoção lisossômica. Em cânceres de mama mais agressivos, triplo negativos, a Snail tende a se acumular no núcleo e escapar da AMC, fortalecendo sua capacidade de desencadear TEM e metástase.
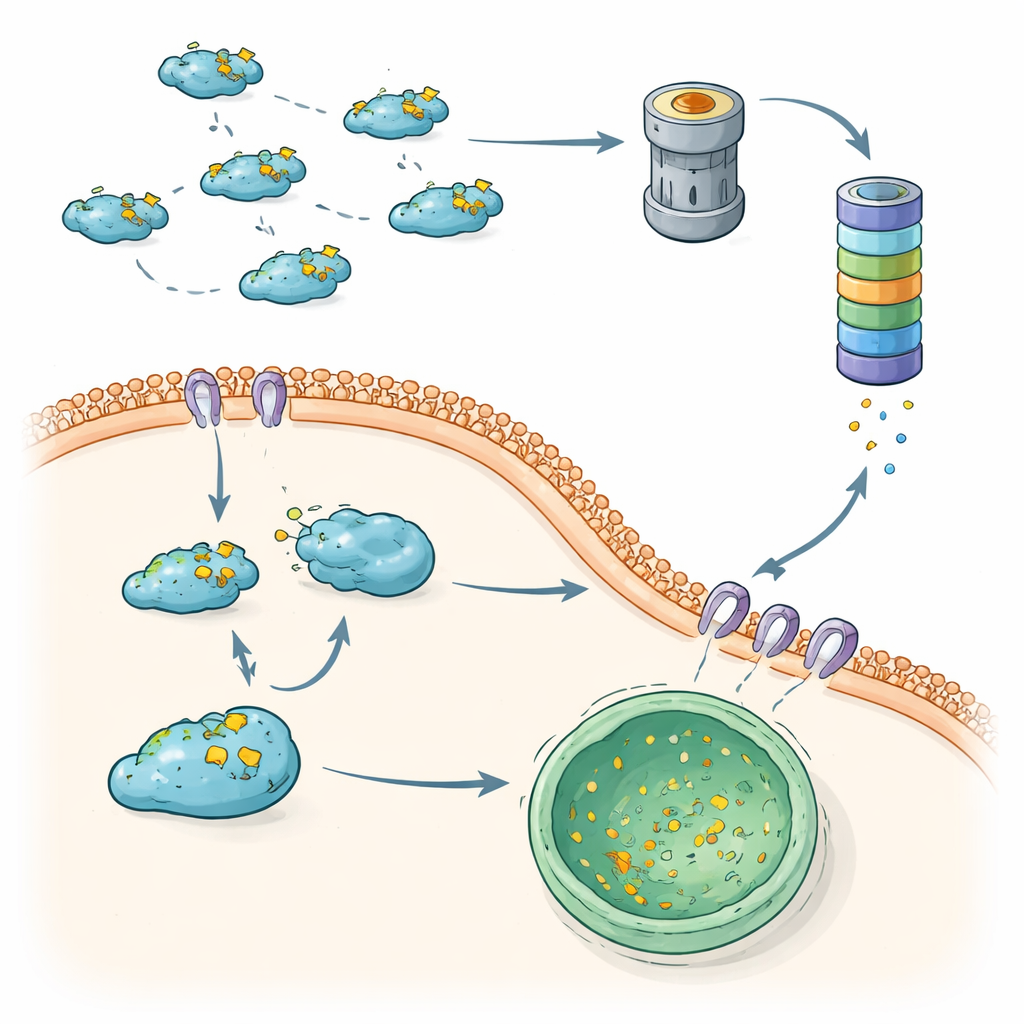
Quando o controle de qualidade falha, a metástase avança
Em conjunto, essas descobertas revelam que as células usam dois eixos complementares de “controle de qualidade” para conter a Snail: a via ubiquitina–proteassoma e a degradação lisossômica baseada em AMC. Quando ambos funcionam corretamente, a Snail é rapidamente renovada, limitando a TEM e ajudando a prevenir a disseminação de células tumorais. Quando qualquer um dos eixos é enfraquecido — por alterações em enzimas de marcação, desubiquitinases ou componentes da AMC — a Snail torna-se mais estável, acumula-se no núcleo e promove fortemente o comportamento invasivo. Ao mapear essas rotas interconectadas de degradação, o artigo delineia novas possibilidades terapêuticas: fármacos que restaurem ou potencializem a degradação da Snail, ou que redirecionem a Snail de volta à AMC ou à destruição proteassomal, poderiam ajudar a reaplicar os freios à metástase sem desligar completamente esses sistemas essenciais de reciclagem de proteínas.
Citação: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
Palavras-chave: metástase do câncer, transição epitélio–mesênquima, proteína Snail, degradação de proteínas, autofagia