Clear Sky Science · pt
Um circuito neuroinflamatório cornea–trigêmeo dependente do receptor vaniloide transiente 1 promove neuropatia corneana
Olhos sensíveis e dor persistente
Muitas pessoas com olhos secos e irritados se surpreendem ao saber que os piores sintomas não vêm da superfície ocular em si, mas dos nervos que detectam irritação e dor. Este estudo em camundongos revela um ciclo de retroalimentação oculto entre o olho e o centro sensorial do cérebro que ajuda a explicar por que a dor ocular pode se tornar persistente e por que às vezes afeta ambos os olhos mesmo quando apenas um parece seco. Ao identificar um guardião molecular específico nesse circuito, o trabalho aponta para novas maneiras de acalmar olhos doloridos sem simplesmente acrescentar mais lágrimas.

Quando o sistema de alarme do olho falha
A janela clara e frontal do olho, a córnea, é densamente povoada por terminações nervosas que monitoram continuamente umidade, temperatura e a composição química das lágrimas. Na doença do olho seco, as lágrimas são reduzidas ou ficam salgadas demais, e os pacientes frequentemente desenvolvem sensação de queimação, ardência ou até dor incapacitante. Os autores concentraram-se em um sensor molecular nas fibras de dor corneanas chamado TRPV1, mais conhecido como o receptor do composto de pimenta caiena, a capsaicina. Esse sensor responde ao calor e a sinais liberados durante estresse tecidual. A equipe investigou se a superativação do TRPV1 pela secura e dano poderia provocar não apenas irritação local, mas também mudanças mais profundas nos nervos que conectam o olho ao cérebro.
Um circuito nervo–imune ligando olho e cérebro
Usando modelos murinos nos quais a produção de lágrima é reduzida cirurgicamente, os pesquisadores demonstraram que o olho seco ativa fortemente as fibras nervosas corneanas que expressam TRPV1. Isso, por sua vez, altera a atividade gênica e o comportamento imune no gânglio trigeminal, um aglomerado de nervos que abriga os corpos celulares dos neurônios sensoriais corneanos. Em camundongos normais, a secura levou a uma onda de genes inflamatórios e relacionados ao sistema imune ali e alterou o estado de macrófagos próximos, células imunes que envolvem neurônios sensoriais. Ao mesmo tempo, as próprias superfícies oculares secas mostraram células imunes ativadas na superfície, redução da densidade nervosa e sensibilidade anormal: a córnea tornou-se menos responsiva ao toque mecânico e a alguns estímulos químicos, mas mais reativa à estimulação de TRPV1, sugerindo que esse sensor em particular havia se hipersensibilizado.
Como um olho lesionado pode afetar o outro
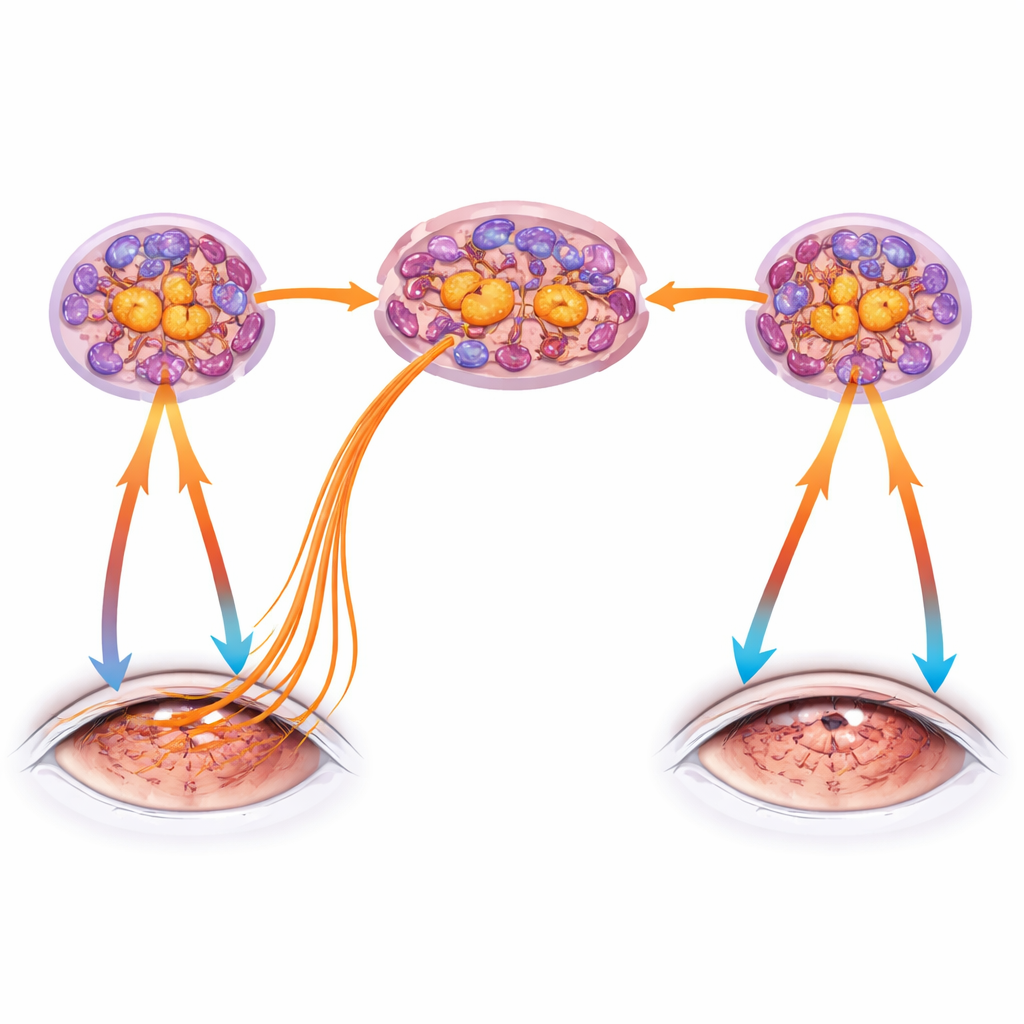
Para separar os efeitos diretos da secura de sinais remotos conduzidos pelos nervos, a equipe criou um olho seco “unilateral” removendo uma glândula lacrimal apenas do lado direito. Surpreendentemente, o olho esquerdo não tratado permaneceu normalmente úmido e manteve uma barreira de superfície saudável, mas com o tempo desenvolveu inflamação sutil e sinais claros de disfunção nervosa — afinamento de fibras nervosas mais profundas e sensibilidade alterada — espelhando, porém atrasando-se em relação, ao lado danificado. Essas mudanças contralaterais dependeram do TRPV1: camundongos geneticamente sem esse sensor foram protegidos em ambos os olhos, o seco e o intocado. Sequenciamento de RNA dos gânglios trigeminais confirmou que a secura unilateral desencadeou uma assinatura imune e inflamatória também no lado oposto, apontando para um circuito córnea–trigêmeo–córnea que pode espalhar o problema de um olho para o outro.
Demonstrando que o TRPV1 é suficiente para causar dano
A secura é complexa e ativa muitas vias, então os autores perguntaram a seguir se o TRPV1 sozinho seria capaz de disparar esse circuito. Aplicaram capsaicina topicamente na córnea de um olho, estimulando o TRPV1 sem secar a superfície. O olho tratado mostrou degeneração marcada dos nervos corneanos e sensibilidade reduzida, embora a barreira epitelial permanecesse íntegra. Notavelmente, o olho não tratado novamente desenvolveu perda mais suave, mas mensurável, de terminações nervosas e alterações na sensibilidade, confirmando que a forte ativação do TRPV1 em uma córnea é suficiente para provocar lesão nervosa e mudanças funcionais no olho parceiro através da rede trigeminal compartilhada. Camundongos sem linfócitos T e B desenvolveram alterações apenas no olho tratado, sugerindo que a propagação bilateral completa requer também uma resposta imune adaptativa além da ativação nervosa.
Um mensageiro que promove dor e um possível caminho terapêutico
O estudo também examinou a substância P, um neuropeptídeo liberado por fibras de dor estimuladas que pode inflamar ainda mais os tecidos e aumentar a atividade do TRPV1. Bloquear receptores de substância P com colírios no olho não seco de camundongos com olho seco unilateral não prejudicou a superfície corneana, mas reduziu significativamente a perda de sensibilidade ao toque e a resposta aumentada à estimulação do TRPV1. Contudo, não evitou completamente a perda estrutural de terminações nervosas, ressaltando que vários fatores cooperam para danificar os nervos corneanos. Em conjunto, os achados delineiam um círculo vicioso: secura e lesão ativam o TRPV1 nos nervos corneanos, que enviam sinais de perigo ao gânglio trigeminal, recrutam e reprogramam células imunes ali e então retroalimentam sinais pró-inflamatórios e liberação de neuropeptídeos à superfície ocular, agravando a degeneração nervosa e espalhando disfunção entre os olhos.
O que isso significa para pessoas com olhos secos e dolorosos
Para não especialistas, a mensagem principal é que a doença do olho seco não é apenas um problema local de falta de lágrimas. Trata-se de um circuito nervo–imune autorreforçador que conecta a superfície ocular a centros sensoriais na cabeça e de volta. O TRPV1 fica na porta de entrada desse circuito, atuando como um alarme hipersensível que, uma vez acionado, ajuda a manter a inflamação e o dano nervoso mesmo que a secura inicial seja modesta ou unilateral. Terapias que reduzam a atividade do TRPV1 nos nervos da córnea, ou que interrompam mensageiros a jusante, como a substância P, podem portanto fazer mais do que acalmar uma superfície ressecada — elas podem romper um circuito mais profundo de dor e proteger a complexa rede nervosa que mantém nossos olhos confortáveis e responsivos.
Citação: Pizzano, M., Vereertbrugghen, A., Martinez Gomez, M.J. et al. A transient receptor potential vanilloid 1-dependent corneal–trigeminal neuroinflammatory circuit promotes corneal neuropathy. Exp Mol Med 58, 605–621 (2026). https://doi.org/10.1038/s12276-026-01653-y
Palavras-chave: doença do olho seco, nervos da córnea, TRPV1, neuroinflamação, substância P