Clear Sky Science · pt
Comunicação metabólica entre fibroblastos associados ao câncer, adipócitos e células imunes como motor de um microambiente tumoral imunossupressor
Por que o bairro do tumor importa
O câncer não cresce isoladamente. Vive em um bairro movimentado de células de suporte, células adiposas e células imunes que trocam constantemente nutrientes e sinais químicos. Este texto explica como o “metabolismo” desse entorno — a forma como as células usam e compartilham combustível — inclina silenciosamente a batalha em favor do tumor e contra o sistema imune. Compreender essa economia oculta de açúcares, gorduras e aminoácidos está abrindo novas maneiras de melhorar imunoterapias e cortar o sistema de apoio do tumor.
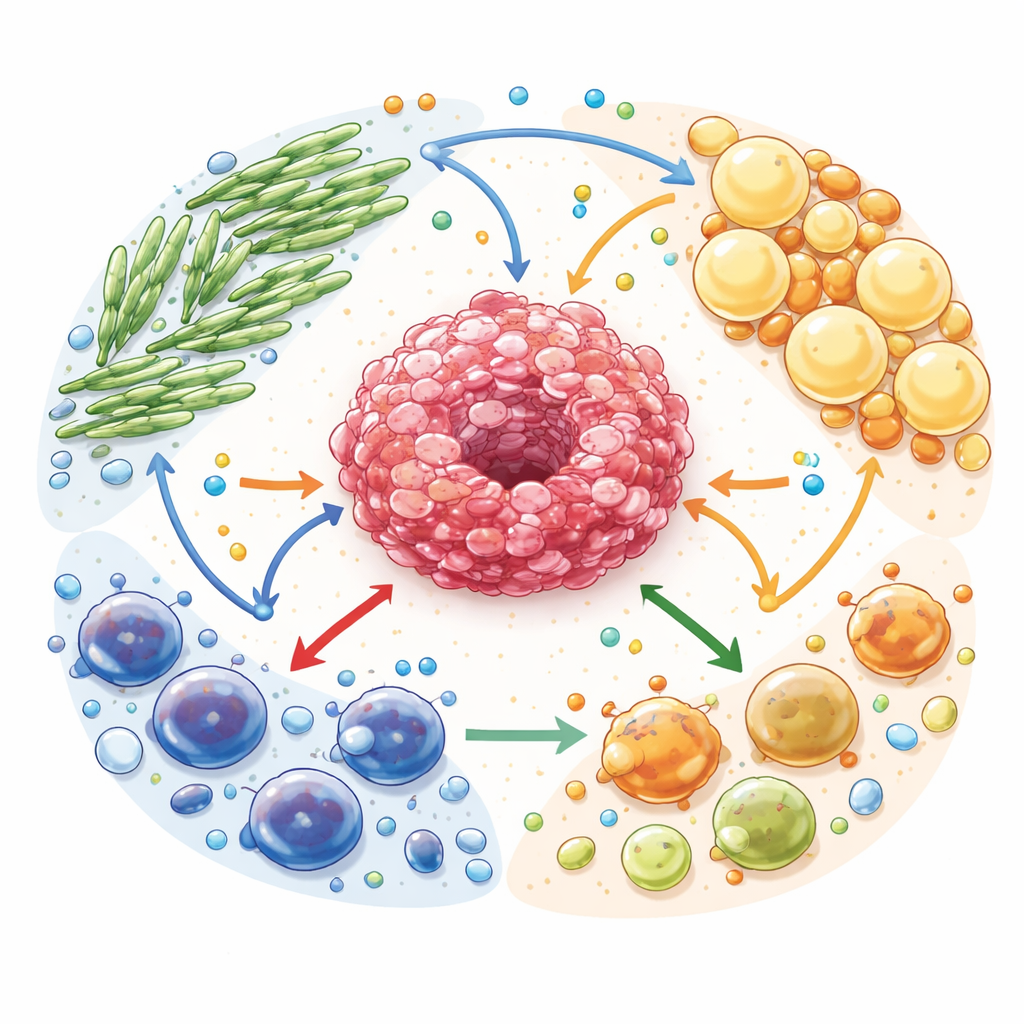
Compartilhamento de combustível em um ecossistema tumoral
Os autores descrevem o microambiente tumoral como um ecossistema complexo. As células cancerígenas estão rodeadas por fibroblastos associados ao câncer (células de suporte semelhantes a tecido cicatricial), adipócitos associados ao câncer (células adiposas reprogramadas) e muitos tipos de células imunes. Todas essas células competem por e trocam combustíveis como glicose, ácidos graxos e aminoácidos. Mas essa troca não é neutra: as células de suporte são reprogramadas para quebrar suas próprias reservas e exportar moléculas ricas em energia que alimentam as células cancerígenas. Ao mesmo tempo, subprodutos semelhantes a resíduos, incluindo lactato e adenosina, se acumulam e atuam como sinais potentes que enfraquecem as células imunes protetoras enquanto favorecem aquelas que atenuam o ataque imune.
Como as células de gordura ajudam os tumores e atrapalham as defesas
As reservas de gordura próximas fazem muito mais do que armazenar calorias. Sob a influência de sinais tumorais e de baixa oxigenação, adipócitos comuns se transformam em adipócitos associados ao câncer. Eles reduzem suas gotículas de gordura, aumentam a quebra de lipídeos e liberam ácidos graxos livres, moléculas inflamatórias e pequenas vesículas cheias de cargo. As células cancerígenas importam essas gorduras com avidez e as queimam em suas mitocôndrias, obtendo uma fonte de energia flexível e duradoura que as ajuda a sobreviver ao estresse, disseminar‑se e resistir ao tratamento. As células imunes em regiões ricas em gordura não se saem tão bem: células T citotóxicas e células NK sobrecarregam‑se com lipídios, sofrem estresse oxidativo e entram em um estado de “exaustão” com capacidade reduzida de destruir células tumorais. Em contraste, células T reguladoras e certos macrófagos prosperam com esses lipídios, tornando‑se mais supressivos e abafando ainda mais as respostas imunes.
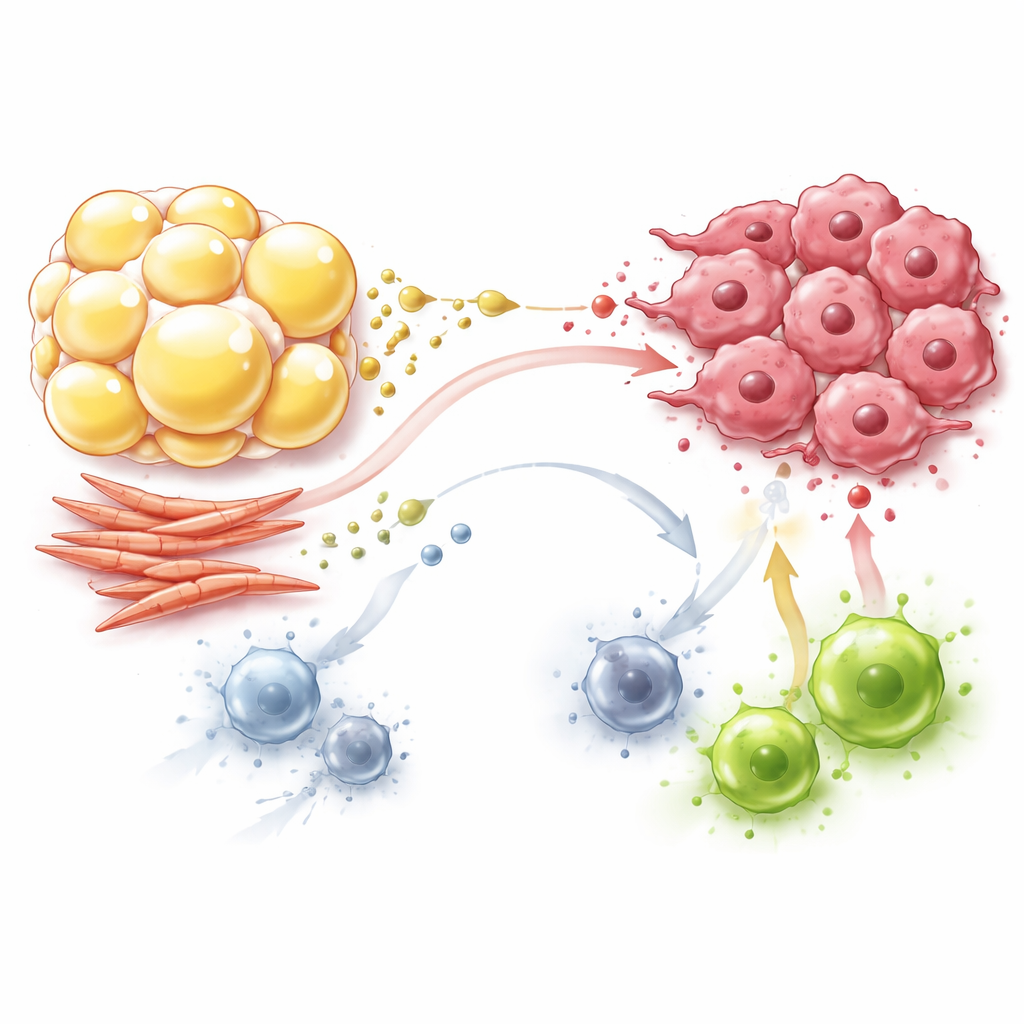
Fibroblastos: construtores que também reprogramam o metabolismo
Os fibroblastos, há muito reconhecidos como construtores do tecido semelhante a cicatriz ao redor dos tumores, também são atores ativos nesse drama metabólico. Os fibroblastos associados ao câncer deslocam‑se para um comportamento ávido por açúcar, convertendo grandes quantidades de glicose em lactato e piruvato mesmo quando o oxigênio está disponível. Eles exportam esses produtos para o espaço ao redor, onde as células cancerígenas os reutilizam como combustível para suas próprias usinas, poupando glicose para o crescimento. Os fibroblastos também sintetizam e trocam aminoácidos como glutamina, prolina e asparagina, que sustentam tanto a estrutura do tumor quanto seu crescimento sob estresse nutricional. Ao mesmo tempo, os fibroblastos consomem nutrientes-chave e liberam lactato, excluindo células T efetoras que dependem de glicose e empurrando macrófagos e células T para estados mais tolerantes e menos agressivos.
Células imunes presas em uma armadilha metabólica
O sistema imune dentro dos tumores é moldado tanto pela disponibilidade de combustível quanto pelos antígenos. Células T citotóxicas e células NK, que precisam queimar rapidamente glicídios para alimentar seu ataque, encontram‑se em um ambiente depauperado de glicose e inundado por lactato, gorduras e outros metabólitos supressivos. Seus motores falham, suas mitocôndrias são danificadas e freios inibitórios em suas superfícies aumentam. Enquanto isso, células T reguladoras e macrófagos associados ao tumor estão bem adaptados a esse ambiente hostil. Eles favorecem a oxidação de lipídios e o metabolismo oxidativo, o que lhes permite prosperar onde outros fracassam. Apoiados por fibroblastos e adipócitos, esses elementos reforçam um estado tolerante, semelhante à cicatrização de feridas, que protege o tumor e reduz o impacto de inibidores de checkpoint e outras imunoterapias.
Transformando o metabolismo em alvo terapêutico
A revisão destaca um conjunto crescente de fármacos experimentais projetados para interromper essa rede de apoio sem simplesmente envenenar células em divisão. Algumas abordagens visam bloquear a liberação de gordura pelos adipócitos ou a captação e oxidação de lipídios nas células cancerígenas. Outras atacam vias conduzidas por fibroblastos que geram lactato, remodelam a matriz ou atraem células mieloides supressivas. Ao reduzir níveis de lactato, bloquear transportadores específicos de combustível ou reprogramar sensores de lipídios dentro das células, essas estratégias buscam restaurar o acesso à glicose e a saúde mitocondrial de células T e células NK exaustas. O objetivo final é não apenas matar a fome do tumor, mas “reeducar” seu entorno para que as células imunes novamente reconheçam, alcancem e ataquem efetivamente as células cancerígenas.
Citação: Kim, T.H., Lim, S.H., Lee, H. et al. Metabolic crosstalk among cancer-associated fibroblasts, adipocytes and immune cells as an immunosuppressive tumor microenvironment driver. Exp Mol Med 58, 366–381 (2026). https://doi.org/10.1038/s12276-026-01650-1
Palavras-chave: microambiente tumoral, metabolismo do câncer, fibroblastos associados ao câncer, adipócitos associados ao câncer, imunossupressão tumoral