Clear Sky Science · pt
Progressão da esclerose múltipla associada à micrógia: identificação de alvos e engajamento terapêutico em modelos humanos in vitro
Por que as células imunes do cérebro importam na esclerose múltipla
A esclerose múltipla (EM) costuma ser descrita como uma doença em que o sistema imunológico do corpo ataca o cérebro e a medula espinhal. Muitos medicamentos atuais reduzem com sucesso as crises agudas, ou recaídas, mas não impedem a piora lenta e silenciosa que muitos pacientes experimentam ao longo dos anos. Esta revisão explica como células imunes minúsculas que vivem permanentemente no cérebro, chamadas micróglias, podem impulsionar esse declínio de longo prazo — e como novos modelos cerebrais humanos cultivados em laboratório estão ajudando os cientistas a encontrar tratamentos que possam, finalmente, desacelerar ou deter a progressão.
O motor oculto do dano contínuo
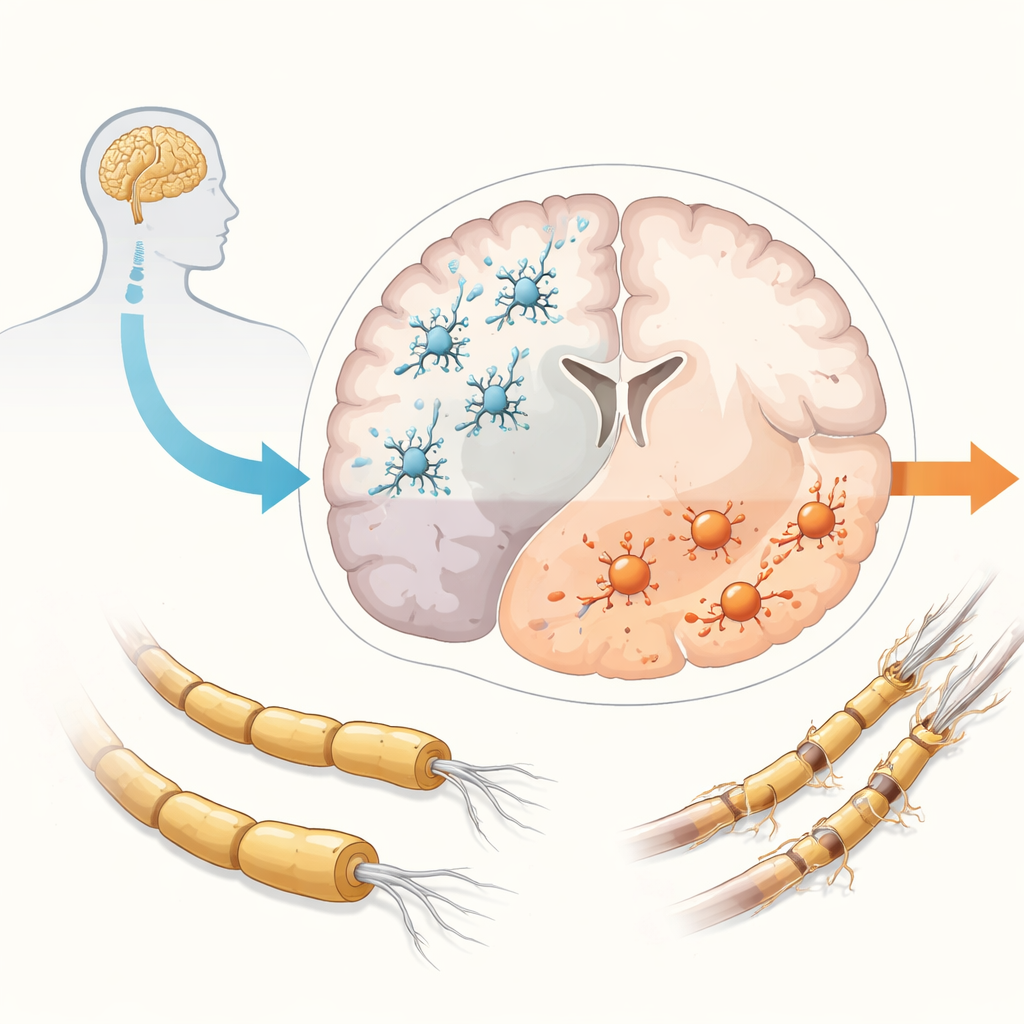
A EM tradicionalmente foi dividida em formas remitente e progressiva, mas evidências agora mostram que a progressão começa muito cedo em quase todos com a doença, mesmo quando ainda parecem ter apenas recaídas. Enquanto as recaídas são alimentadas por células imunes que entram pela corrente sanguínea, a progressão parece ser impulsionada por inflamação aprisionada dentro do cérebro e da medula espinhal. Nesse ambiente selado, as micróglias participam de muitos processos nocivos: inflamação contínua, perda da bainha isolante de mielina nas fibras nervosas tanto da substância branca quanto da cinzenta, acúmulo de substâncias oxigenadas danosas e falha na reparação. O resultado final é a perda gradual de neurônios e de suas conexões. As micróglias normalmente ajudam a manter o cérebro saudável ao remover detritos e apoiar os neurônios, mas na EM elas frequentemente mudam para estados mais agressivos e perdem algumas de suas funções protetoras, o que as torna suspeitas principais na condução da progressão.
Por que modelos animais tradicionais são insuficientes
Por décadas, estudos em camundongos e outros animais foram fundamentais para desenvolver fármacos que limitam recaídas, no entanto falharam em grande parte em produzir terapias que parem a progressão. Uma razão é que os modelos animais apenas imitam parcialmente a EM humana e não reproduzem totalmente a inflamação complexa e duradoura observada nos cérebros dos pacientes. As micróglias de roedores também diferem das humanas em genes e respostas importantes. Como resultado, tratamentos promissores em animais frequentemente não funcionam em seres humanos. A escassez de modelos animais que capturem verdadeiramente a EM progressiva empurrou os pesquisadores a construir novos sistemas humanos em laboratório, onde podem estudar micróglias e outras células cerebrais de forma mais direta.
Construindo modelos cerebrais humanos em uma placa
Os cientistas agora usam várias camadas de modelos laboratoriais para estudar micróglias humanas. Células primárias obtidas diretamente de tecido cerebral de roedores ou humanos preservam muitas características naturais, mas são difíceis de obter, mudam rapidamente fora do ambiente nativo e não podem ser facilmente escaladas. Para superar essas barreiras, os pesquisadores recorrem a células-tronco pluripotentes induzidas (iPS) — células adultas reprogramadas de volta a um estado flexível semelhante a tronco. Essas células iPS podem ser dirigidas para se tornarem micróglias, neurônios ou outras células cerebrais. Em culturas planas simples, micróglias derivadas de iPS capturam muitos traços chave e podem ser produzidas em grande número, permitindo experimentos detalhados e triagens de fármacos. Elas podem até ser geradas a partir de pacientes individuais com EM, revelando diferenças intrínsecas, como atividade gênica alterada e mudanças em como essas células respondem ao estresse e removem detritos.
Adicionando vizinhanças cerebrais realistas
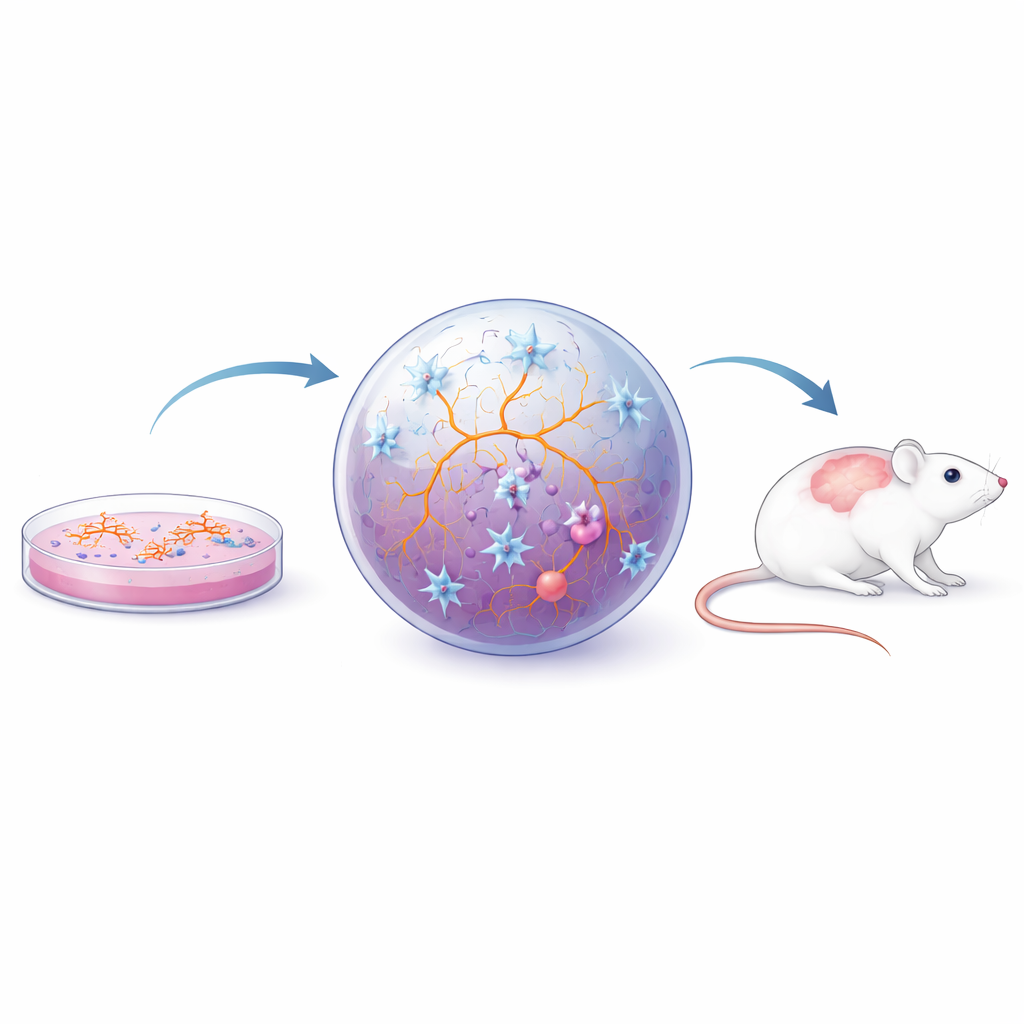
Porque o comportamento das micróglias é fortemente moldado pelo entorno, os pesquisadores foram além de monocamadas celulares para configurações mais realistas. Em coculturas bidimensionais, micróglias crescem junto com neurônios e células de suporte, o que as ajuda a adotar formas e comportamentos mais naturais e permite que os cientistas investiguem como os tipos celulares influenciam uns aos outros. Esferoides tridimensionais e organoides — pequenos fragmentos auto-organizados de tecido semelhante ao cerebral — vão além, oferecendo um ambiente macio e denso que se assemelha mais ao tecido cerebral real. Quando micróglias são incorporadas nessas estruturas, mostram formas ramificadas complexas, reagem a lesões, interagem com uma camada semelhante à barreira hematoencefálica e respondem a sinais inflamatórios do líquido cefalorraquidiano de pessoas com EM. Esses modelos foram usados para estudar como a inflamação crônica desencadeia um estado “cansado porém inflamado” chamado senescência celular em micróglias e astrócitos, e como alterações no manejo lipídico microglial podem prejudicar a reparação da mielina. Em paralelo, o transplante de micróglias humanas derivadas de iPS ou de organoides em cérebros de camundongos permite que essas células maturiem mais dentro de uma rede viva e sejam testadas em modelos estabelecidos de doença semelhante à EM.
Dos modelos de laboratório a tratamentos futuros
No conjunto, esses modelos humanos in vitro e quiméricos formam um conjunto de ferramentas para dissecar como as micróglias contribuem para a progressão da EM e para testar novas terapias que visem acalmar a atividade microglial nociva ao mesmo tempo em que restauram suas funções protetoras. Embora nenhum dos modelos reproduza completamente o cérebro humano, cada um captura diferentes peças do quebra-cabeça e, juntos, preenchem a lacuna entre culturas celulares simples e modelos animais imperfeitos. Ao combinar percepções desses sistemas, os pesquisadores esperam identificar alvos farmacológicos precisos — como vias que controlam inflamação, alterações semelhantes ao envelhecimento e metabolismo lipídico nas micróglias — que possam, finalmente, se traduzir em tratamentos que retardem ou parem a incapacidade gradual que caracteriza a EM progressiva.
Citação: Blenkle, A., Geladaris, A. & Weber, M.S. Microglia-associated progression of multiple sclerosis: target identification and therapeutic engagement in human in vitro models. Exp Mol Med 58, 357–365 (2026). https://doi.org/10.1038/s12276-026-01647-w
Palavras-chave: progressão da esclerose múltipla, micrógia, células-tronco pluripotentes induzidas, organoides cerebrais, neuroinflamação