Clear Sky Science · pt
Um laço de feedback positivo ESRP1/circPHGDH/miR-149/RAP1B promove comportamentos malignos e glicólise em células de câncer de próstata
Por que esta pesquisa importa para a saúde dos homens
O câncer de próstata é um dos tipos de câncer mais comuns entre homens, e muitos tumores acabam se tornando agressivos e resistentes aos tratamentos. Este estudo revela um circuito de controle oculto dentro das células do câncer de próstata que as ajuda a crescer mais rápido, se disseminar com mais facilidade e reprogramar a forma como metabolizam a glicose para obter energia. Ao mapear esse laço molecular, os pesquisadores apontam novas vulnerabilidades que podem ser alvo para retardar a doença ou tornar as terapias existentes mais eficazes.
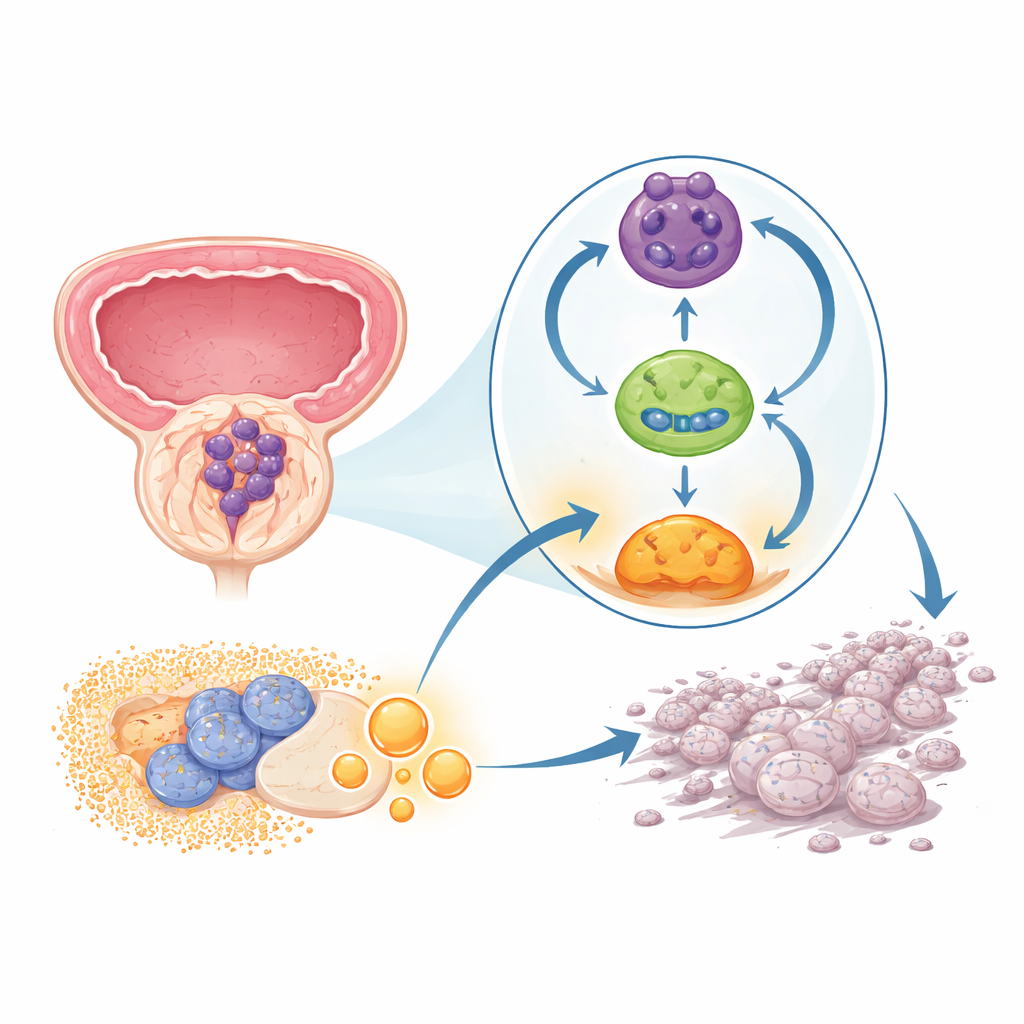
Um laço oculto que mantém o câncer ligado
A equipe concentrou-se em uma classe de material genético recentemente valorizada, chamada RNAs circulares. Ao contrário das fitas lineares usuais, essas moléculas formam anéis fechados e são notavelmente estáveis. Em amostras de tumores de próstata e em linhagens celulares, os pesquisadores encontraram um RNA circular em particular, chamado circPHGDH, consistentemente mais abundante do que nos tecidos não cancerosos adjacentes. Pacientes cujos tumores tinham mais desse RNA tenderam a apresentar tumores maiores, crescimento local mais avançado e disseminação à distância, sugerindo que o circPHGDH contribui para uma forma mais perigosa da doença.
Como as células cancerosas mudam seu comportamento
Para entender o que o circPHGDH realmente faz, os cientistas alteraram seus níveis em células de câncer de próstata cultivadas em laboratório. Quando reduziram o circPHGDH, as células formaram menos colônias, migraram e invadiram membranas com menos eficiência e mostraram sinais de permanecer em um estado mais “epitelial”, menos propenso a se espalhar. Ao mesmo tempo, as células se afastaram de um estilo metabólico ávido por glicose, típico de muitos tumores: a dependência pela glicólise diminuiu e o uso de produção de energia baseada em oxigênio aumentou. Quando o circPHGDH foi aumentado, todas essas características promotoras do câncer mudaram na direção oposta.
Pequenos RNAs e um circuito de sinal de crescimento
O estudo então rastreou como o circPHGDH exerce esses efeitos. No interior aquoso da célula, o circPHGDH atua como uma esponja para um pequeno RNA regulador chamado miR-149, absorvendo-o e impedindo que ele reprima seus alvos habituais. Um alvo chave é o RAP1B, uma proteína de sinalização que alimenta uma via importante de crescimento e sobrevivência conhecida por ter papel no câncer de próstata. Quando o miR-149 é sequestrado pelo circPHGDH, os níveis de RAP1B aumentam e ativam sinais a jusante que promovem divisão celular, mobilidade e um metabolismo com forte dependência da glicólise. Restaurar o miR-149 ou reduzir diretamente o RAP1B reverteu muitos dos efeitos prejudiciais, tanto em culturas celulares quanto em camundongos com tumores humanos de próstata.
Resíduos metabólicos que alimentam o fogo
Outra camada da história envolve como o circPHGDH é produzido em primeiro lugar. Sua criação depende de uma proteína de splicing chamada ESRP1, que ajuda a decidir como mensagens de RNA brutas são cortadas e remontadas. Os pesquisadores mostraram que o ESRP1 se liga a sítios específicos ao redor da região do circPHGDH e favorece sua forma circular em detrimento da versão linear padrão. De forma crucial, descobriram que o lactato — produto final da glicólise — modifica quimicamente o ESRP1 em um único sítio, tornando a proteína mais estável. Como o próprio circPHGDH empurra as células para uma glicólise aumentada e, portanto, mais produção de lactato, isso cria um ciclo autorreforçador: o ESRP1 aumenta o circPHGDH, o circPHGDH eleva o RAP1B e a glicólise, a glicólise gera lactato e o lactato, por sua vez, estabiliza o ESRP1.
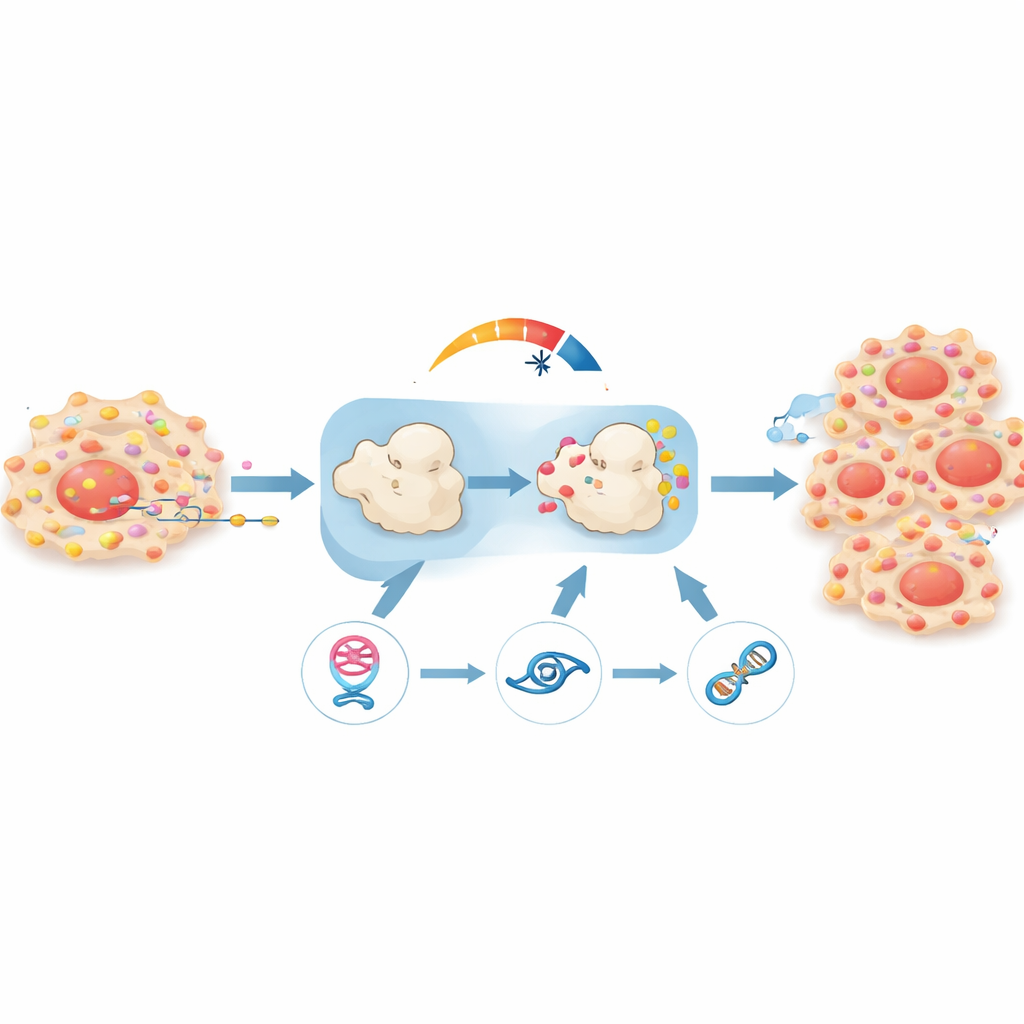
Evidências em modelos animais
Para testar se esse laço realmente importa em um organismo vivo, a equipe implantou células de câncer de próstata humanas em camundongos. Tumores nos quais o circPHGDH havia sido silenciado cresceram mais devagar, pesaram menos e mostraram menos sinais de disseminação, conforme medido por imagem de corpo inteiro e análise de tecidos. Marcadores de proliferação celular estavam menores e a estrutura do tumor parecia menos agressiva ao microscópio. Quando os pesquisadores bloquearam o miR-149 ou forçaram a restauração do RAP1B nesses mesmos tumores, grande parte do crescimento e da disseminação retornou, confirmando que a cadeia circPHGDH–miR-149–RAP1B é um motor central do comportamento da doença.
O que isso significa para tratamentos futuros
Em conjunto, os achados revelam um laço de feedback positivo em que uma proteína de splicing, um RNA circular, um pequeno RNA regulador e uma proteína de sinalização cooperam para direcionar as células do câncer de próstata a um crescimento rápido, invasão e metabolismo dependente de glicose. Para não especialistas, a mensagem-chave é que as células cancerosas podem conectar seus controles genéticos e metabólicos em circuitos autorreforçadores que mantêm a progressão da doença. Romper esse laço — interrompendo o circPHGDH, restaurando o miR-149, bloqueando o RAP1B ou interferindo na modificação de ESRP1 dependente de lactato — oferece várias vias promissoras para futuros fármacos destinados a retardar ou interromper o câncer de próstata agressivo.
Citação: Wang, X., Yu, L., Qian, X. et al. A ESRP1/circPHGDH/miR-149/RAP1B positive feedback loop promotes the malignant behaviors and glycolysis of prostate cancer cell. Exp Mol Med 58, 622–635 (2026). https://doi.org/10.1038/s12276-026-01646-x
Palavras-chave: câncer de próstata, RNA circular, metabolismo tumoral, microRNA, vias de sinalização