Clear Sky Science · pt
A proteína sensível ao redox HMGB1: papéis intra e extracelulares
Por que uma proteína que muda de forma importa para a saúde
Dentro de quase todas as células do seu corpo existe uma pequena proteína chamada HMGB1 que se comporta um pouco como uma ferramenta multifuncional. Em condições calmas, ela ajuda silenciosamente a organizar o DNA. Mas quando as células estão estressadas ou danificadas, a HMGB1 pode sair do núcleo, migrar para o tecido ao redor e funcionar como um sinal de alarme para o sistema imunológico. Este artigo de revisão explica como pequenas mudanças químicas impulsionadas pela oxidação transformam a HMGB1 em personalidades biológicas muito diferentes — que podem proteger tecidos, impulsionar a inflamação ou até contribuir para doenças crônicas. Entender esse “anel de humor” molecular pode abrir novas maneiras de acalmar a inflamação excessiva sem desligar completamente o sistema imunológico.
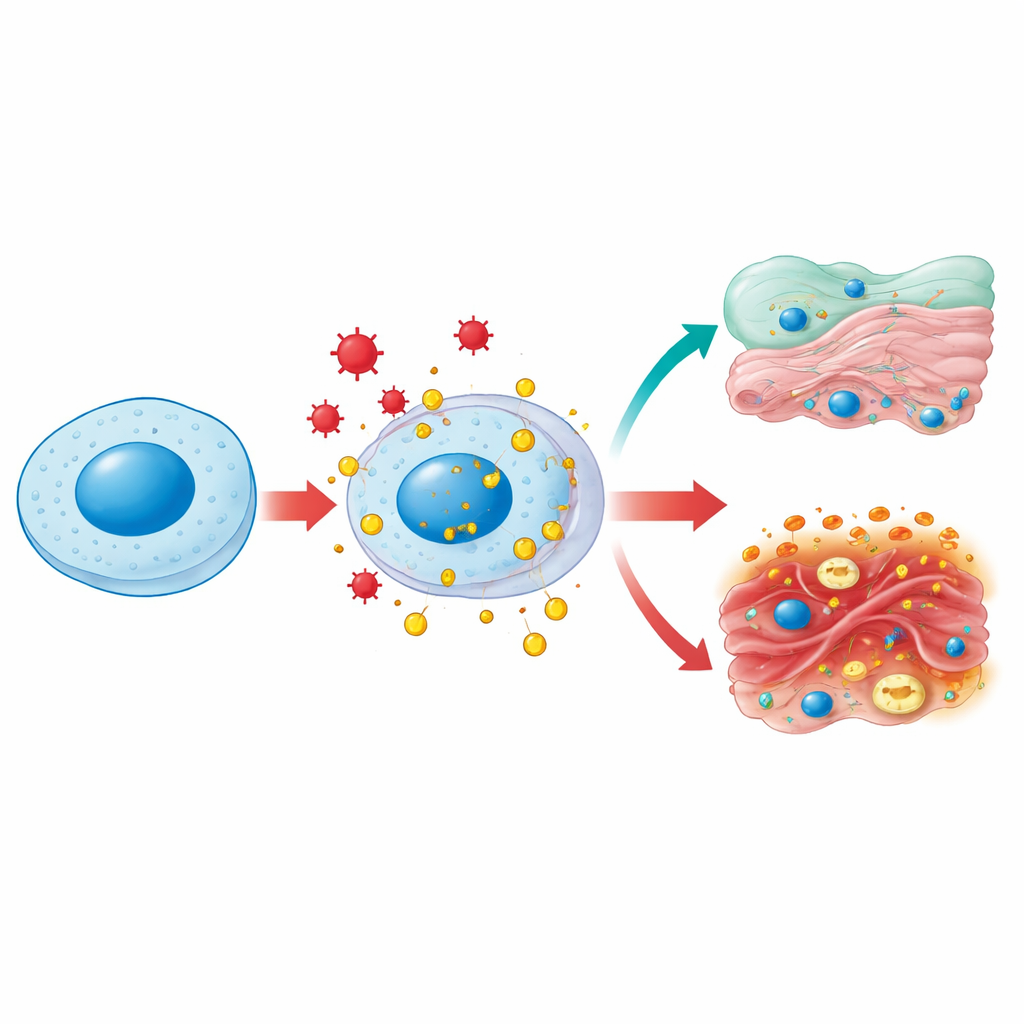
Uma proteína, muitos bairros
A HMGB1 normalmente vive no núcleo celular, onde dobra e afrouxa o DNA para que genes possam ser copiados e reparados. Sob estresse — como infecção, glicose alta ou lesão tóxica — ela pode ser quimicamente modificada e escoltada para o interior aquoso da célula e depois para o exterior. No citoplasma, a HMGB1 ajuda a manter as mitocôndrias, as usinas de energia da célula, saudáveis ao estimular um processo de limpeza chamado autofagia e ao prevenir a fragmentação excessiva desses organelos. Quando liberada para fora da célula, a HMGB1 torna-se um clássico “sinal de perigo”: células imunes a reconhecem como um indício de que tecidos foram lesionados e correm ao local. Assim, a mesma molécula desempenha funções de manutenção dentro das células e papéis de alarme fora delas, dependendo de onde está e de como foi quimicamente modulada.
Como a oxidação reescreve seu comportamento
O ponto central desta revisão é como a oxidação — reações impulsionadas por espécies reativas de oxigênio (ERO) — remodela a HMGB1. A proteína contém três blocos construtores contendo enxofre que atuam como pequenos interruptores. Em seu estado totalmente reduzido, a HMGB1 tende a favorecer a sobrevivência celular e o recrutamento de células reparadoras. Uma oxidação leve pode ligar dois desses sítios dentro da mesma proteína, criando uma forma “disulfeto” que é especialmente boa em se ligar a receptores imunes como os receptores Toll-like e o RAGE na superfície celular. Essa versão estimula fortemente a produção de mensageiros inflamatórios. Um estresse oxidativo mais intenso pode empurrar a molécula para uma forma hiperoxidada que não consegue mais se ligar ao DNA ou aos receptores de forma eficaz; essa versão “queimada” torna-se imunologicamente silenciosa e está associada à fase de resolução da inflamação e a programas de morte celular que não provocam ataque imune.
De sinais de morte celular a motores de doença
A HMGB1 está profundamente entrelaçada com as muitas formas pelas quais as células morrem. Durante formas violentas de morte, como necrose, necroptose, ferroptose e piroptose, a HMGB1 vaza ou é ativamente transportada para fora das células, carregando uma assinatura redox que reflete as condições oxidativas ao redor. No início da necrose, tende a estar em forma reduzida, enquanto o estresse prolongado a empurra para estados mais oxidativos. Uma vez do lado de fora, a HMGB1 reduzida pode promover autofagia protetora em algumas células cancerosas, ajudando-as a sobreviver à quimioterapia, enquanto formas ricas em dissulfeto e dimerizadas amplificam cascatas inflamatórias e a ativação do complemento que podem agravar o dano tecidual. A HMGB1 também pode retroalimentar e promover certas vias de morte — por exemplo, ao se associar a lipídeos bacterianos para desencadear necroptose ou ao impulsionar a morte celular dependente de ferro em células de suporte cerebral após um AVC. Dessa forma, a HMGB1 tanto marca quanto modula o equilíbrio vida–morte nos tecidos.
Ligações com inflamação, autoimunidade e câncer
Porque seu comportamento é tão sensível à oxidação, variantes diferentes da HMGB1 aparecem em padrões distintos nas doenças. A HMGB1 rica em dissulfeto está fortemente associada à inflamação crônica: surge em articulações inflamadas na artrite reumatoide, em fígado fibrótico, em lesão pulmonar, em dano por isquemia–reperfusão após cirurgia e na sepse, onde seus níveis sanguíneos se correlacionam com gravidade e risco de morte. A HMGB1 reduzida, por outro lado, frequentemente acompanha migração celular e remodelamento tecidual, como o movimento de fibroblastos cardíacos ou monócitos guiados pela quimiocina CXCL12. A HMGB1 hiperoxidada e imunologicamente silenciosa está enriquecida em cenários como apoptose em estágio avançado, quando o corpo deseja eliminar células moribundas sem provocar um ataque. Em tumores, a forma disulfeto sustenta um ambiente imune supressor e permissivo ao crescimento, enquanto bloquear a HMGB1 pode reduzir tumores e tornar imunoterapias com bloqueio de checkpoint mais eficazes.
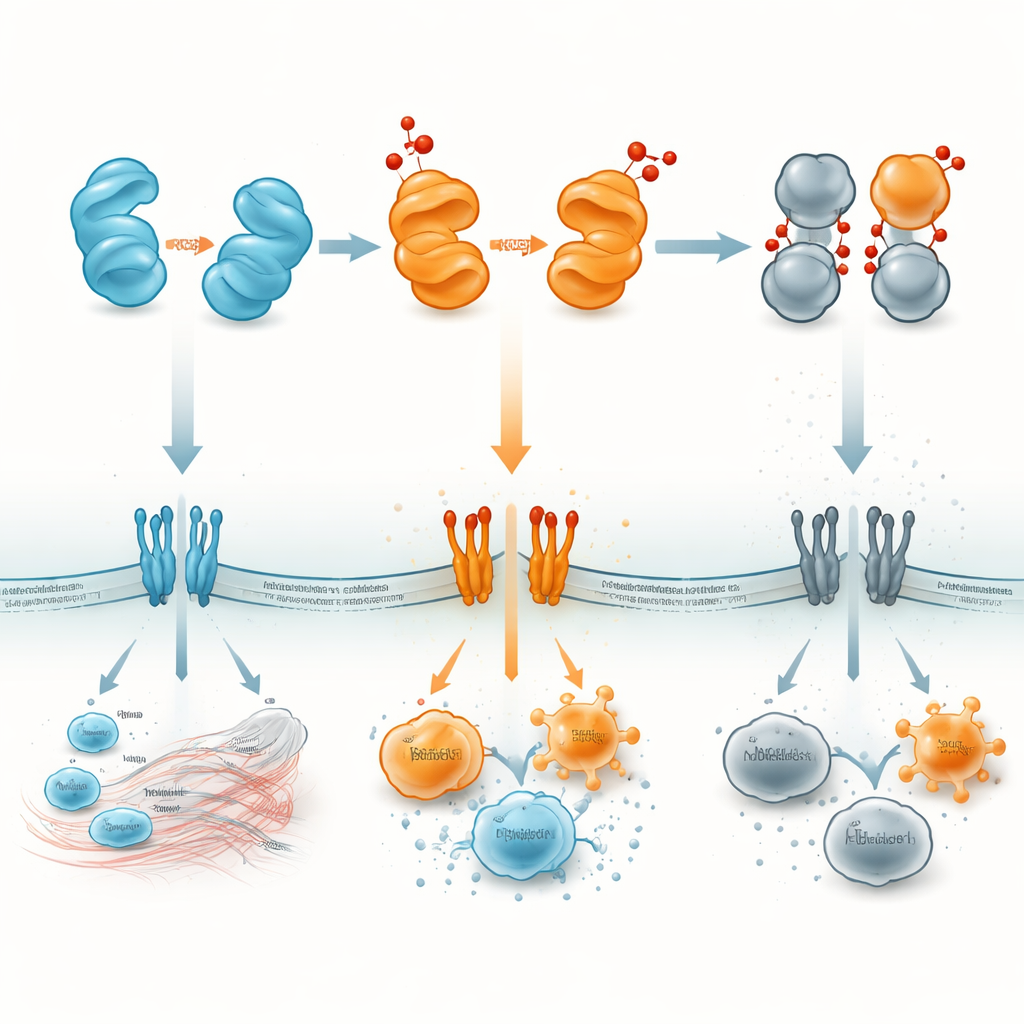
Transformando um alarme molecular em alvo terapêutico
Para um observador leigo, a HMGB1 pode ser pensada como um pequeno alarme proteico cujo volume e mensagem mudam com seu estado químico. A HMGB1 reduzida tende a chamar equipes de reparo; as formas disulfeto e dimerizadas podem soar um alarme estridente que alimenta inflamação prejudicial; e a forma totalmente oxidada cai efetivamente no silêncio, ajudando a inflamação a se encerrar. Ao mapear onde e quando cada versão aparece — dentro de núcleos, no citoplasma, no sangue ou em órgãos específicos — os pesquisadores esperam projetar drogas que bloqueiem as formas nocivas ou estabilizem as benéficas. Essas estratégias podem permitir que médicos tratem sepse, autoimunidade, AVC, lesão pulmonar ou câncer ao mirar não apenas a HMGB1 em si, mas o “dimmer” oxidativo que controla como essa proteína se comunica com o sistema imune.
Citação: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
Palavras-chave: HMGB1, inflamação, estresse oxidativo, morte celular, doença autoimune