Clear Sky Science · pt
UBE2M como uma ponte entre neddylation e regulação do ciclo celular no adenocarcinoma colorretal
Por que esta pesquisa é importante para o câncer intestinal
O câncer colorretal está entre os tumores mais comuns e letais no mundo, em grande parte porque as células tumorais aprendem a se dividir sem controle. Este estudo revela um interruptor de controle até então oculto que ajuda as células do câncer colorretal a atravessar rapidamente um ponto de verificação crítico da divisão celular. Ao mostrar como esse interruptor funciona em nível molecular — e demonstrar que um antifúngico já disponível pode interferir nele — o trabalho aponta para uma possível nova forma de frear ou impedir o crescimento tumoral.
Uma camada oculta de controle dentro das células tumorais
As células não se dividem ao acaso; elas percorrem um ciclo ordenado com pontos de verificação que confirmam se é seguro copiar o DNA e se separar em duas. Células cancerosas frequentemente alteram esses pontos de verificação. Os autores focalizaram um processo de marcação química chamado neddylation, que modifica sutilmente proteínas após sua síntese. Estudos anteriores sugeriam que a neddylation é mais ativa em vários cânceres, mas como ela se conectava ao ciclo de divisão das células colorretais era incerto. Usando grandes conjuntos de dados de célula única de tumores humanos, juntamente com dados de expressão gênica em amostras de mais de 1.800 pacientes, a equipe descobriu que a atividade de neddylation é especialmente alta em células malignas do intestino que estão no estágio G2/M — o portão final antes da divisão celular.
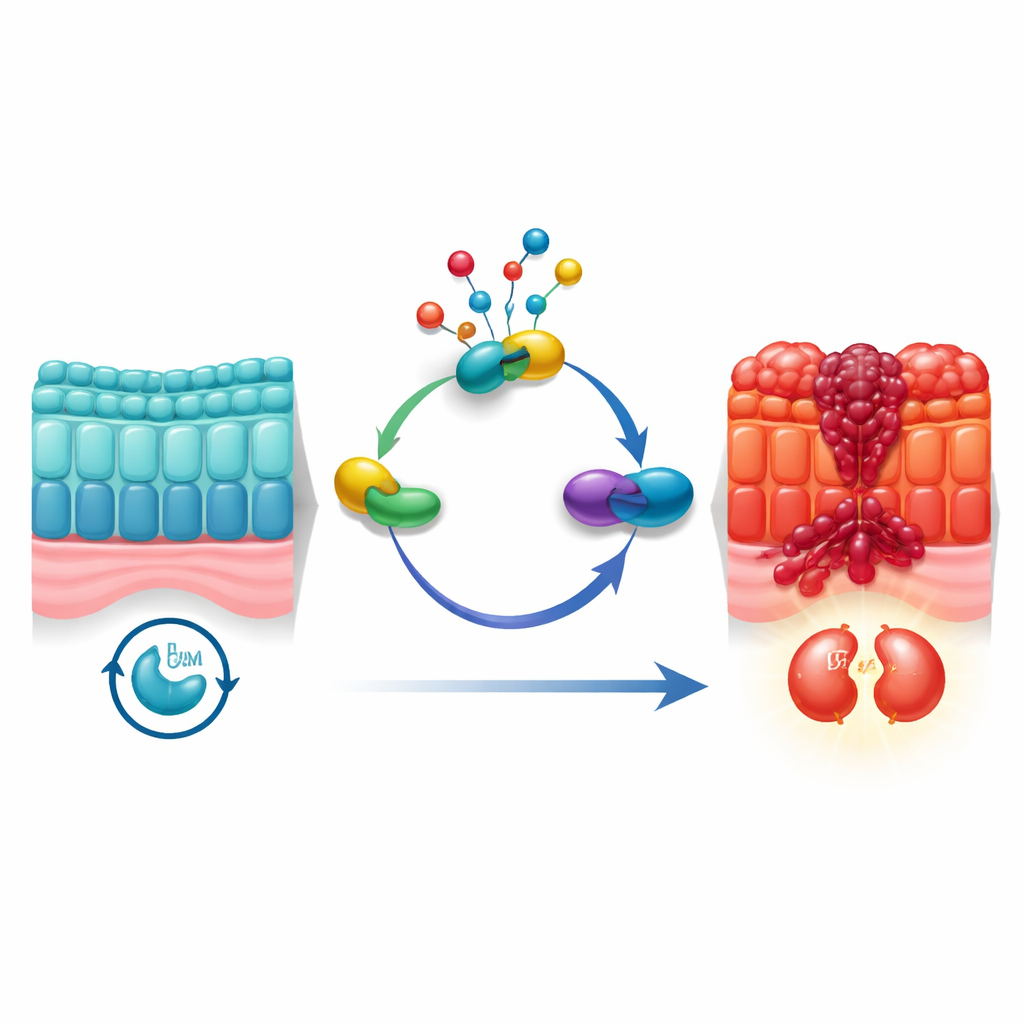
Foco em uma proteína “ponte” molecular
Para identificar quais moléculas conectam a neddylation à divisão celular, os pesquisadores usaram análises computacionais em estilo de rede para vasculhar milhares de genes. Uma proteína se destacou: UBE2M, uma enzima que ajuda a anexar a pequena etiqueta NEDD8 a outras proteínas. UBE2M não só estava fortemente associada às vias de neddylation e do ciclo celular nos dados; também foi encontrada em níveis muito mais altos em tumores colorretais do que em tecido normal adjacente. Pacientes cujos tumores apresentavam mais UBE2M tendiam a ter sobrevida pior, sinalizando-a como um possível motor do tumor e não apenas um espectador. Quando a equipe reduziu UBE2M em linhas celulares cancerígenas e em modelos tumorais em camundongos, o crescimento tumoral diminuiu, a divisão celular se reduziu e mais células passaram por morte programada. Por outro lado, forçar as células a produzir UBE2M em excesso acelerou o crescimento e o progresso do ciclo celular.
Um revezamento que protege uma proteína chave promotora do crescimento
Aprofundando-se, os cientistas investigaram como UBE2M auxilia a divisão celular. Eles descobriram que UBE2M não age sozinho, mas inicia um revezamento envolvendo outras duas proteínas, USP39 e PABPC1. Normalmente, PABPC1 é marcada para destruição por uma cadeia de ubiquitina, que a envia para a maquinaria de reciclagem proteica da célula. A equipe mostrou que UBE2M modifica quimicamente USP39 com a etiqueta NEDD8. Essa modificação aumenta a capacidade de USP39 de remover cadeias de ubiquitina de PABPC1, salvando-a da degradação e tornando-a mais estável. Com mais PABPC1 disponível, a célula fica melhor em traduzir certos RNAs mensageiros em proteína, incluindo o mRNA de CCNB1, uma ciclina que atua como acelerador no ponto de verificação G2/M. Em essência, UBE2M ajuda a estabilizar PABPC1, que por sua vez aumenta a produção de CCNB1, impulsionando as células rumo à divisão.
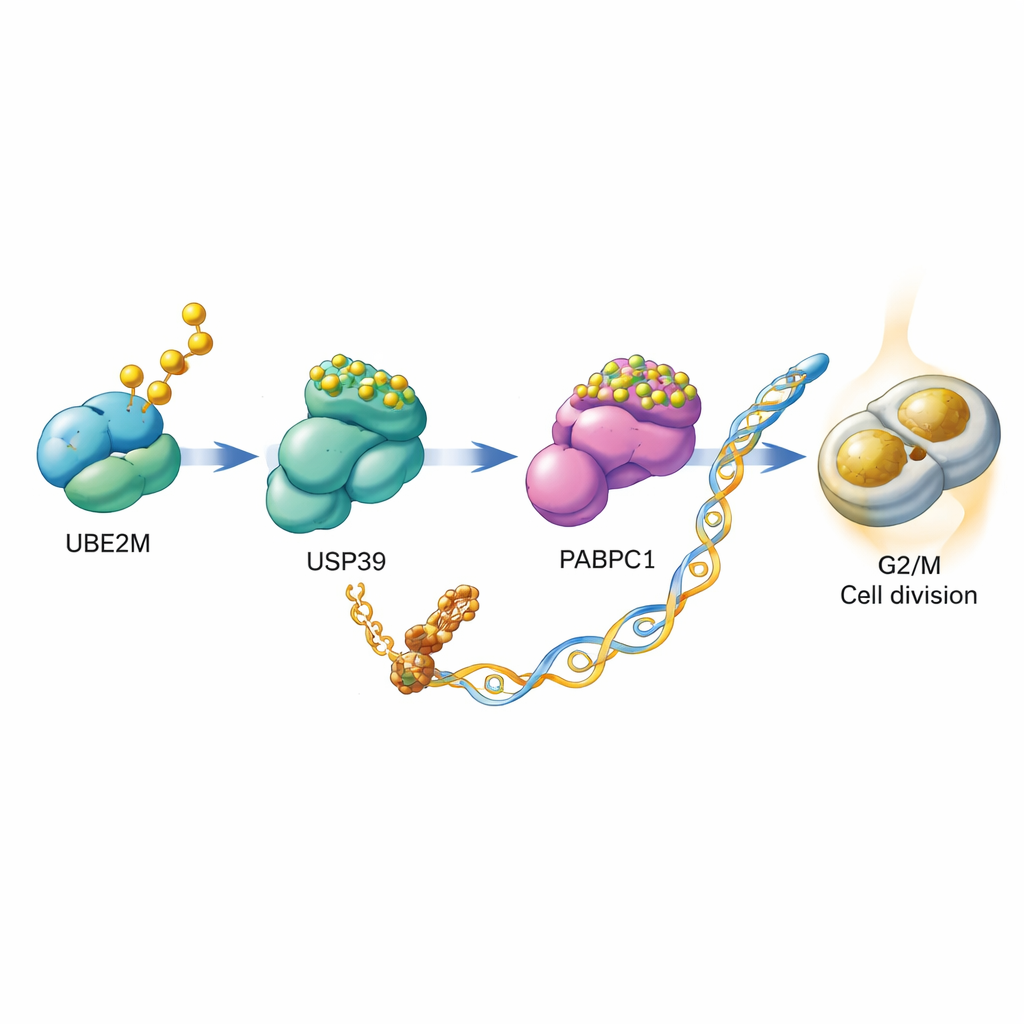
Do mecanismo molecular à oportunidade terapêutica
A descoberta dessa cadeia UBE2M–USP39–PABPC1–CCNB1 sugeriu uma nova vulnerabilidade nas células do câncer colorretal. Os autores testaram micafungina, um fármaco já usado contra infecções fúngicas e recentemente identificado como inibidor da atividade de neddylation de UBE2M. Em células de câncer intestinal cultivadas em laboratório, a micafungina enfraqueceu a neddylation de USP39, aumentou a degradação de PABPC1 e reduziu os níveis da proteína CCNB1. Como resultado, a divisão celular desacelerou, mais células ficaram retidas no ponto de verificação G2/M e a apoptose aumentou. Em camundongos implantados com células de câncer colorretal, o tratamento diário com micafungina reduziu significativamente os tumores em comparação com animais não tratados, sem necessidade de remover UBE2M diretamente.
O que isso significa para pacientes a longo prazo
Este trabalho descreve com clareza como uma única enzima, UBE2M, pode ligar um sistema sutil de marcação de proteínas à decisão de uma célula de câncer intestinal de se dividir. Ao estabilizar um fator de tradução (PABPC1) via USP39, UBE2M eleva indiretamente os níveis de um potente impulsionador do ciclo celular, CCNB1, permitindo que os tumores cresçam mais rapidamente. Embora sejam necessárias mais pesquisas e testes clínicos, os achados sugerem que bloquear esse revezamento — potencialmente com medicamentos reposicionados como a micafungina — poderia oferecer uma nova estratégia direcionada para retardar a progressão do câncer colorretal e melhorar os desfechos para os pacientes.
Citação: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
Palavras-chave: câncer colorretal, ciclo celular, neddylation, UBE2M, terapia direcionada