Clear Sky Science · pt
CDK13 impulsiona carcinoma de células claras do rim por meio da modificação m6A mediada por METTL16 no mRNA de ACLY
Por que tumores renais cheios de gordura importam
O câncer de rim de células claras frequentemente parece pálido e oleoso ao microscópio porque suas células estão repletas de gordura. Essa aparência incomum não é apenas cosmética; reflete uma reprogramação mais profunda de como essas células cancerosas gerenciam combustível. Este estudo faz uma pergunta simples, porém importante: qual chave molecular ordena que as células tumorais renais acumulem gordura, e será que essa chave pode ser desligada para frear a doença?
Um maestro oculto do crescimento tumoral
Os pesquisadores concentraram-se em uma proteína chamada CDK13, parte de uma família de enzimas que normalmente ajudam as células a se dividir. Ao analisar grandes conjuntos de dados de pacientes e amostras tumorais, eles descobriram que os níveis de CDK13 são consistentemente mais altos em cânceres renais de células claras do que no tecido renal normal. Pacientes cujos tumores carregavam mais CDK13 tendiam a ter cânceres maiores, mais avançados e prognóstico pior. Quando a equipe reduziu CDK13 em linhagens de células de câncer renal, as células cresceram mais devagar e apresentaram dificuldade em avançar pelo ciclo celular, sugerindo que o CDK13 atua como um maestro oculto que coordena tanto o crescimento quanto a sobrevivência.
Do açúcar à gordura: reprogramando a fábrica de combustível da célula
Como os tumores renais de células claras estão repletos de lipídios, a equipe examinou se o CDK13 também controla como essas células sintetizam gordura. Usando uma combinação de perfis de expressão gênica e colorações microscópicas para gordura, eles mostraram que aumentar o CDK13 intensifica o acúmulo de gotículas lipídicas dentro das células cancerosas, enquanto reduzir o CDK13 tem o efeito oposto. O CDK13 influenciou fortemente uma enzima chamada ACLY, que converte um intermediário metabólico comum em acetil-CoA, a matéria-prima para construir ácidos graxos e colesterol. Níveis elevados de CDK13 andavam de mãos dadas com níveis altos de ACLY em tumores de pacientes, e ambas as proteínas se concentravam nas mesmas regiões do tecido tumoral. Quando a ACLY foi artificialmente aumentada, ela resgatou muitas das falhas de crescimento e armazenamento de gordura causadas pela perda de CDK13, posicionando a ACLY como um efetor chave a jusante dessa via. 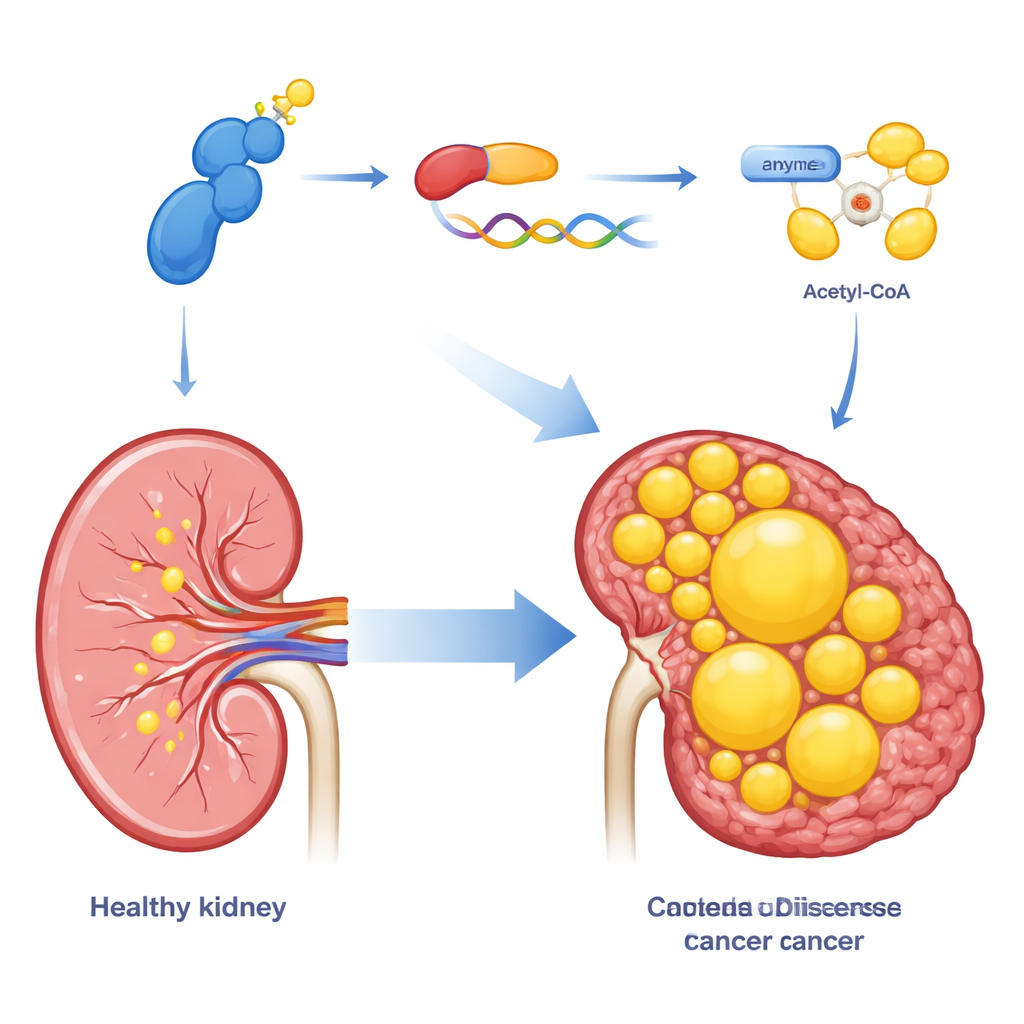
Um sistema de mensagens em camadas dentro das células cancerosas
Em vez de atuar diretamente sobre a ACLY como um interruptor simples, o CDK13 exerce seu poder por meio de um sistema de mensagens em camadas baseado no RNA, a molécula que carrega instruções genéticas do DNA para as fábricas de proteína. Os autores descobriram que o CDK13 se liga fisicamente e modifica quimicamente outra enzima, a METTL16, que marca mensagens de RNA específicas com pequenos grupos químicos chamados metil. O CDK13 adiciona uma etiqueta fosfato à METTL16 em um ponto preciso, tornando a METTL16 mais ativa. Por sua vez, a METTL16 coloca marcas de metil adicionais na fita de RNA que codifica a ACLY. Essas marcas não mudam o código genético em si, mas alteram como a célula trata aquela mensagem. Uma terceira proteína, YTHDC2, reconhece o RNA marcado da ACLY e o protege da degradação, permitindo que mais proteína ACLY seja produzida ao longo do tempo. Essa cascata — CDK13 ativando METTL16, METTL16 marcando o RNA da ACLY e YTHDC2 protegendo essa mensagem marcada — cria um ciclo potente que impulsiona a síntese de gordura. 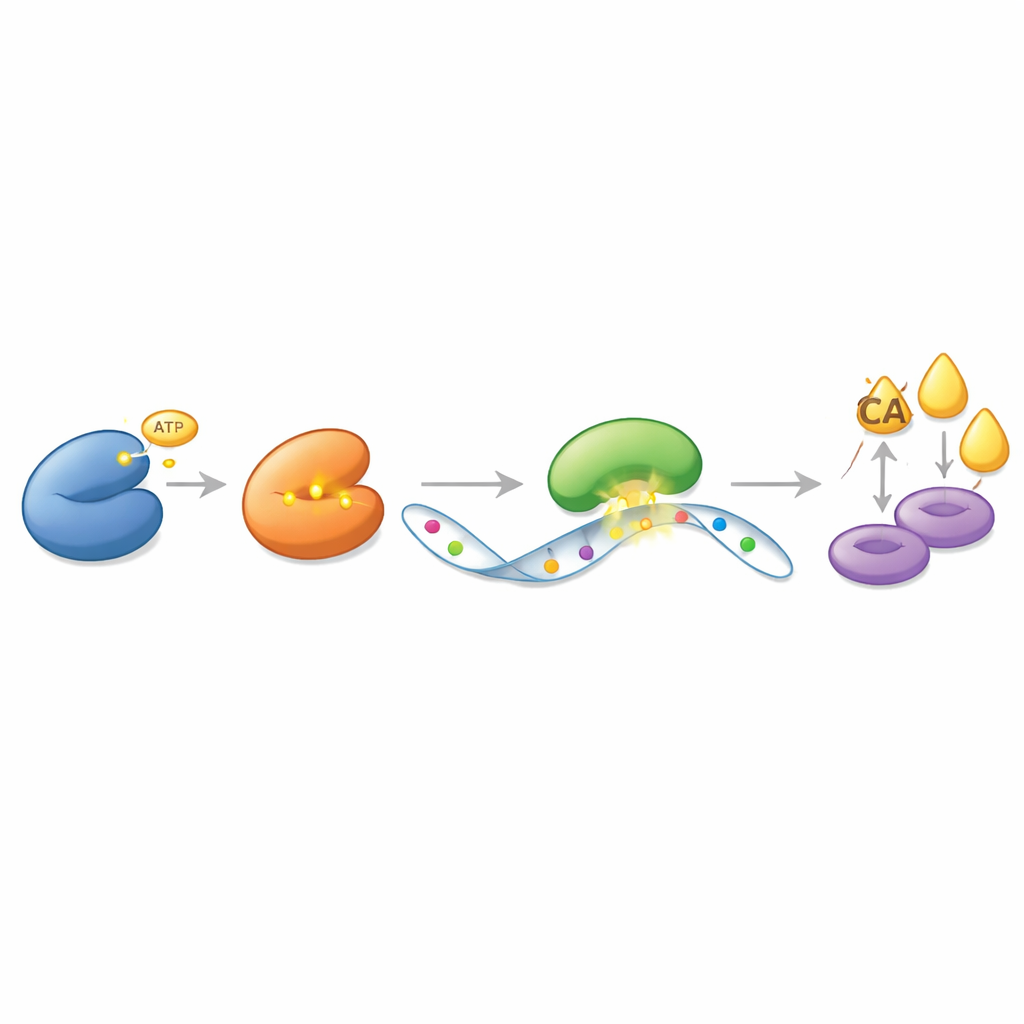
Testando a cadeia em células, camundongos e amostras de pacientes
A força do trabalho reside em quão exaustivamente os autores testaram essa cadeia de eventos. Em células de câncer renal cultivadas, interromper qualquer parte da via CDK13–METTL16–ACLY reduziu as gotículas lipídicas e desacelerou a proliferação. Em camundongos implantados com células humanas de câncer renal, bloquear CDK13 ou ACLY isoladamente encolheu tumores e reduziu as reservas de gordura dentro deles, enquanto bloquear ambos simultaneamente teve um efeito ainda mais forte. A equipe também usou um composto de pequena molécula, 1NM-PP1, que inibe a atividade do CDK13. Esse agente semelhante a um fármaco reduziu a marca ativadora na METTL16, diminuiu os níveis de ACLY e suprimiu o crescimento tumoral, especialmente quando combinado com a depleção de METTL16. Em conjuntos de dados de pacientes, CDK13, METTL16 e ACLY tendiam a subir e descer em conjunto, reforçando a ideia de que esse eixo está ativo em cânceres reais, não apenas em modelos de laboratório.
O que isso pode significar para tratamentos futuros
Para não especialistas, a mensagem principal é que este estudo revela um novo botão de controle para a “fábrica de gordura” dentro dos tumores renais de células claras. Em vez de mirar apenas nas enzimas que sintetizam lipídios, os pesquisadores expõem uma cadeia de comando em nível superior que estabiliza as instruções para essas enzimas. Ao interromper o eixo CDK13–METTL16–ACLY, pode ser possível privar os tumores das gorduras de que precisam para crescer e se espalhar, enquanto as células normais seriam menos afetadas. Embora o trabalho ainda seja pré-clínico e 1NM-PP1 ainda não seja um fármaco para câncer renal, as descobertas apontam para novas estratégias que combinam inibidores de quinase com fármacos que miram enzimas modificadoras de RNA, oferecendo uma forma mais precisa de tratar essa forma de câncer renal impulsionada metabolicamente.
Citação: Chen, J., Liu, H., Zhang, Y. et al. CDK13 drives clear cell renal carcinoma through METTL16-mediated m6A modification of ACLY mRNA. Exp Mol Med 58, 472–486 (2026). https://doi.org/10.1038/s12276-025-01634-7
Palavras-chave: carcinoma de células claras do rim, metabolismo lipídico, CDK13, metilação de RNA, ACLY