Clear Sky Science · pl
Ultraskuteczna detekcja biomarkerów choroby Alzheimera za pomocą biosensorów fotonicznych z nanosinglami
Dlaczego prosty test krwi na utratę pamięci ma znaczenie
W miarę pojawiania się nowych leków, które potrafią spowolnić postęp choroby Alzheimera, lekarze pilnie potrzebują prostych badań, które wskażą osoby zagrożone na długo zanim pojawią się oczywiste objawy. Dziś potwierdzenie choroby Alzheimera zwykle wymaga kosztownych skanów mózgu lub nakłuć lędźwiowych, które rzadko wykonuje się w rutynowej opiece. W badaniu opisano maleńki czujnik wykorzystujący światło, który potrafi wykryć kluczowe molekuły związane z Alzheimerem w kropli krwi na poziomach istotnych klinicznie, co może otworzyć drogę do szybkich, niedrogich testów możliwych do wykorzystania w zwykłych przychodniach, a nawet przy łóżku pacjenta.
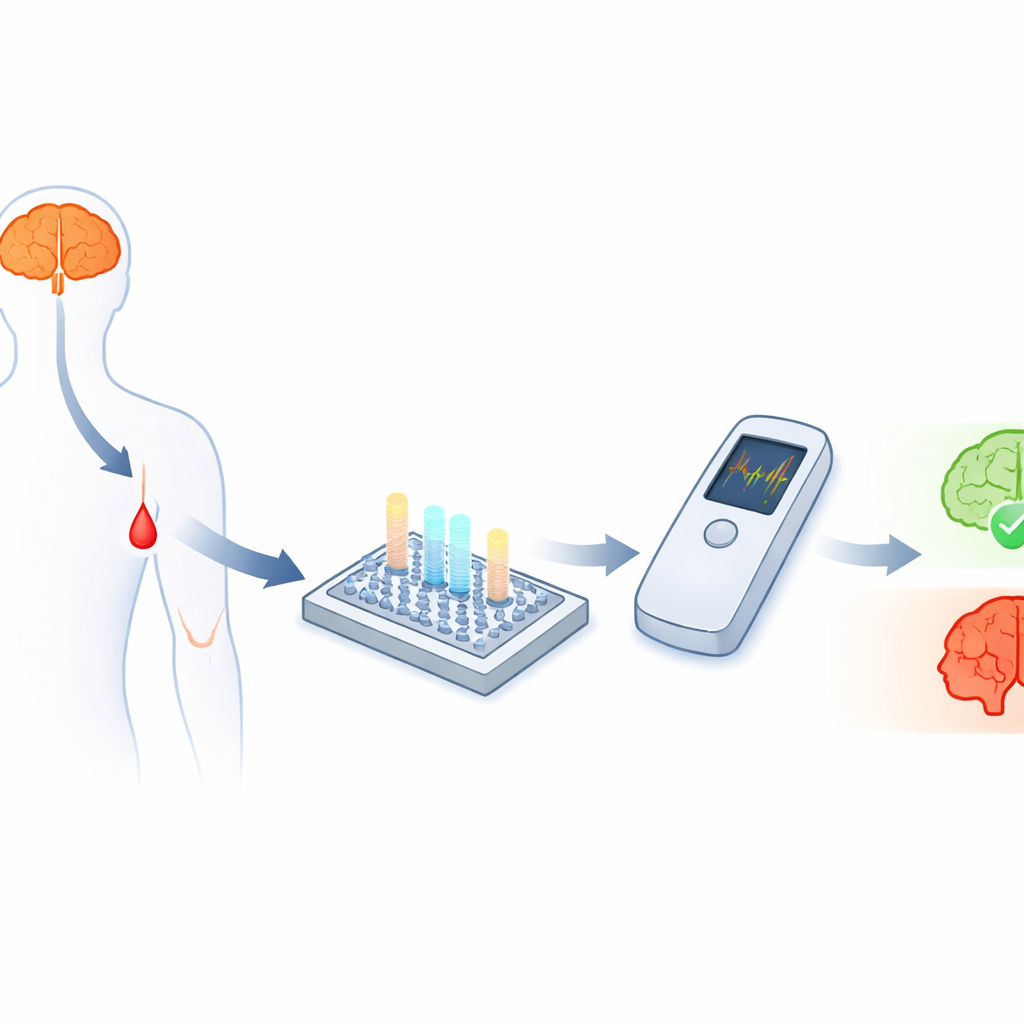
Poszukiwanie śladów we krwi
Choroba Alzheimera jest ściśle związana z małymi fragmentami białek zwanymi amyloid‑beta, w szczególności dwiema postaciami znanymi jako Aβ40 i Aβ42. Ich ilości, a zwłaszcza stosunek między nimi, niosą ważne wskazówki o obecności choroby i jej przebiegu. Problem w tym, że te fragmenty są bardzo małe i krążą we krwi na ekstremalnie niskich poziomach — trylionowych części grama na mililitr — co sprawia, że ich dokładne zmierzenie poza wyspecjalizowanymi laboratoriami jest bardzo trudne. Chociaż czujniki elektrochemiczne teoretycznie mogą wykrywać takie stężenia, przekształcenie ich w wytrzymałe, tanie testy przyłóżkowe zdolne jednocześnie śledzić kilka biomarkerów okazało się trudne.
Prowadzenie światła przez maleńkie filary
Zespół podszedł do tego problemu, stosując nanofotonikę — struktury kontrolujące światło na skali mniejszej niż długość fali. Zbudowali chip pokryty regularną siatką sparowanych, włosowatych krzemowych filarów osadzonych na szkle. Gdy światło pada na taką wzorzystą powierzchnię, zostaje uwięzione w szczególnym rezonansowym trybie bardzo czułym na zmiany w pobliżu szczytów filarów, podobnie jak brzmienie kamertonu zmienia się, gdy coś na nim zostanie dodane. Poprzez precyzyjne dostosowanie odstępów między filarami w każdej parze badacze zrównoważyli jednocześnie trzy kluczowe właściwości: jak wyraźny jest rezonans optyczny, jak silnie reaguje na otoczenie i jak duży sygnał generuje. Takie „optymalne” zaprojektowanie czyni chip szczególnie odpowiednim do wykrywania bardzo małych ilości materiału.
Uczynienie niewidocznych molekuł widocznymi
Nawet przy zoptymalizowanym projekcie same markery Alzheimera ledwie zakłócałyby światło. Aby wzmocnić efekt, badacze zastosowali strategię typu kanapka z nanocząstkami złota. Najpierw powlekali powierzchnię sensora warstwami adhezyjnej chemii, która prawidłowo orientowała specjalistyczne przeciwciała tak, by ich miejsca wiążące były skierowane do cieczy. Te przeciwciała wychwytują Aβ40 lub Aβ42 z próbki. Następnie przez chip przepuszczano nanocząstki złota, każdą ozdobioną drugim przeciwciałem rozpoznającym inny koniec tego samego fragmentu amyloidu. Gdy fragment amyloidu jest obecny, łączy powierzchnię z nanocząstką złota, „oznaczając” jego obecność. Ponieważ złoto silnie zaburza lokalne środowisko optyczne, każdy wychwycony fragment powoduje znacznie większe przesunięcie rezonansu sensora niż sam peptyd, zwiększając czułość o około jedną do dwóch rzędów wielkości przy zachowaniu klarownego sygnału optycznego.
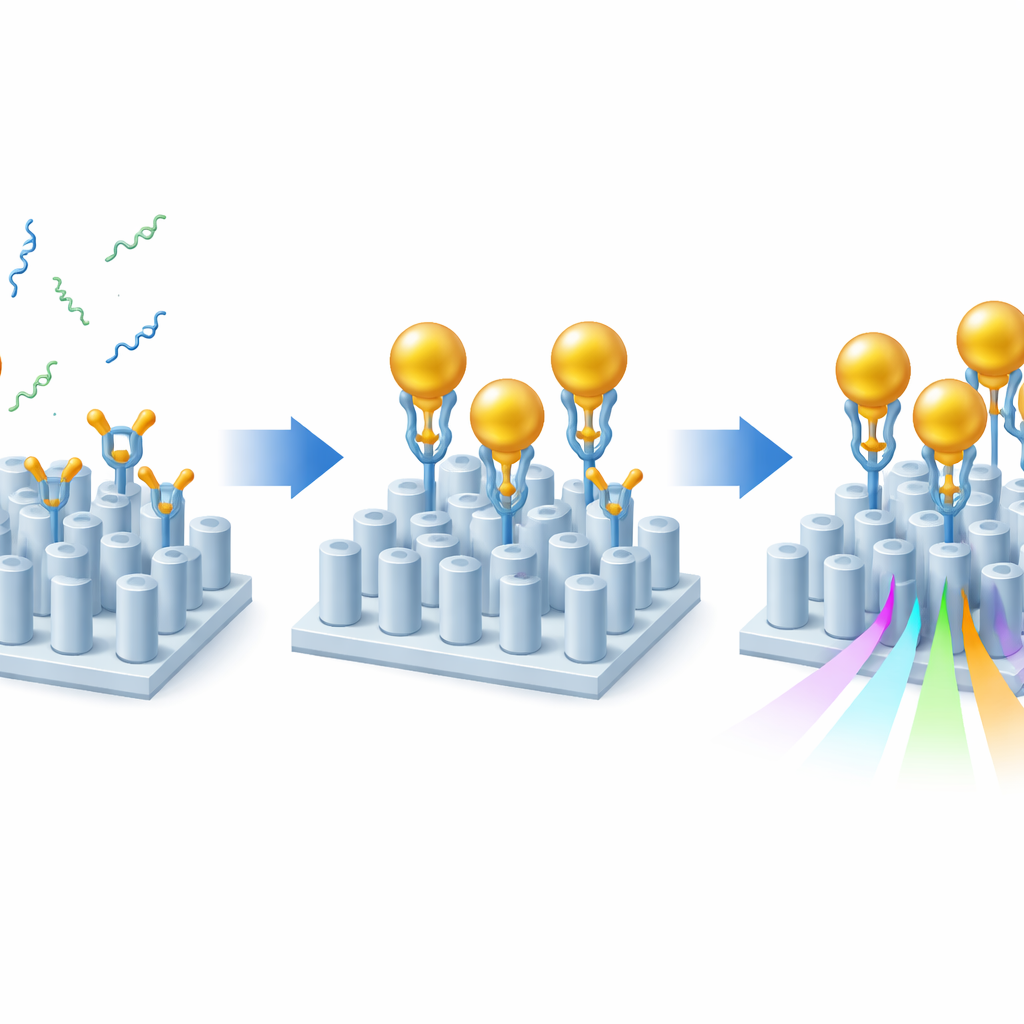
Testowanie realistycznych próbek
Aby pokazać, że podejście działa poza prostymi buforami laboratoryjnymi, zespół testował swój sensor na surowicy krwi ludzkiej. Rozcieńczali surowicę tak, by nadawała się do obsługi mikroprzepływowej, jednocześnie zachowując poziomy amyloidu reprezentatywne dla pacjentów. Co istotne, byli w stanie wykryć zarówno Aβ40, jak i Aβ42 na poziomie 0,2 pikograma na mililitr w tej rozcieńczonej surowicy — co odpowiada klinicznie istotnemu poziomowi 20 pikogramów na mililitr we krwi pełnej. Poprzez umieszczanie różnych przeciwciał chwytających w oddzielnych obszarach tego samego chipu zmierzyli jednocześnie obie formy amyloidu w jednym małym kanale, co jest kluczowym krokiem w kierunku oceny stosunku tych form z jednej małej próbki. Sygnały wyraźnie odróżniały próbki doszpikowane dodatkowymi ilościami amyloidu od tych zawierających jedynie naturalne, tła występujące nawet u zdrowych osób.
Co to może oznaczać dla przyszłej opieki
Podsumowując, te postępy pokazują, że kompaktowy, światłoczuły sensor wzmocniony nanocząstkami złota może osiągnąć czułość potrzebną do sensownych testów krwi na Alzheimeraz przy jednoczesnej możliwości obsługi więcej niż jednego biomarkera naraz. Chociaż potrzebne są dalsze prace, by przekształcić to w solidne urządzenie komercyjne i dodać inne markery, takie jak formy białka tau, technologia bazuje na skalowalnych materiałach i może być sparowana z prostą, przenośną optyką. Jeśli zostanie w pełni rozwinięta, mogłaby pozwolić klinicystom monitorować zdrowie mózgu przy użyciu jedynie niewielkiej próbki krwi, ułatwiając wczesne wykrywanie Alzheimera i śledzenie skuteczności leczenia w czasie.
Cytowanie: Guilherme S. Arruda, Katie Morris, Augusto Martins, Yue Wang, Sian Sloan-Dennison, Duncan Graham, Steven D. Quinn, Emiliano R. Martins, and Thomas F. Krauss, "Ultrasensitive Alzheimer’s disease biomarker detection with nanopillar photonic crystal biosensors," Optica 12, 1587-1596 (2025). https://doi.org/10.1364/OPTICA.566672
Słowa kluczowe: test krwi na Alzheimera, nanofotoniczny biosensor, amyloid beta, nanocząstki złota, wczesna diagnoza