Clear Sky Science · pl
Pochodzenie struktury czwartorzędowej w fibrylacji hemoglobiny sierpowatej: badanie dynamiki molekularnej
Dlaczego ta historia o krwi ma znaczenie
Choroba sierpowata zaczyna się od drobnej zmiany w jednym białku krwi, a mimo to potrafi przekształcić czerwone krwinki, zablokować naczynia i wywoływać ból przez całe życie. To badanie przygląda się z fizycznego punktu widzenia temu, jak ta pojedyncza zmiana powoduje, że hemoglobina układa się w sztywne włókna wewnątrz komórki. Dzięki zaawansowanym symulacjom komputerowym autorzy łączą atomowe szczegóły z problemami dotyczącymi całych komórek, dostarczając nowych wskazówek, jak przyszłe leki mogłyby zapobiegać zablokowaniu krążenia przez hemoglobinę.
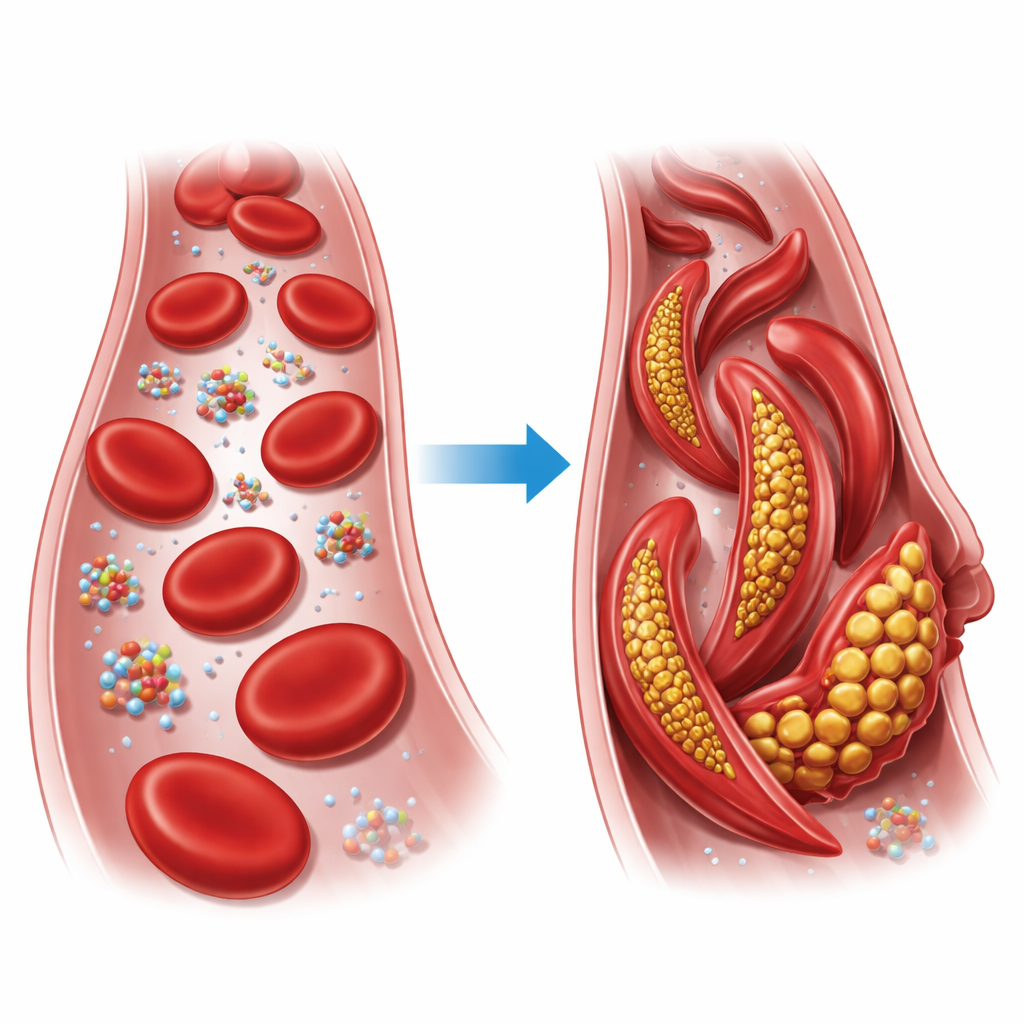
Mała wymiana o dużych konsekwencjach
Hemoglobina to białko przenoszące tlen, wypełniające czerwone krwinki. Każda jednostka hemoglobiny składa się z czterech łańcuchów, które mogą układać się w dwie główne formy ogólne, znane jako stan zrelaksowany (R) i stan spięty (T). W chorobie sierpowatej w jednym z tych łańcuchów dochodzi do zamiany pojedynczego elementu: na pozycji szóstej łańcucha beta naładowana glutamina (korekta: glutaminian) zostaje zastąpiona przez hydrofobową walinę. W warunkach niskiego nasycenia tlenem ta zmieniona wersja, nazwana hemoglobiną sierpowatą, łączy się w długie włókna, które deformują normalnie okrągłe czerwone krwinki w sztywne, sierpowate kształty, mogące zatykać drobne naczynia i pozbawiać tkanki tlenu.
Śledząc zmieniający się kształt hemoglobiny
Autorzy koncentrują się na tym, jak całe jednostki hemoglobiny rotują i upakowują się razem we włóknie. Śledzą tę zmianę dużej skali za pomocą pojedynczego kąta, który mierzy, jak dwie połowy białka skręcają się względem siebie. Korzystając z symulacji dynamiki molekularnej — wirtualnych eksperymentów obliczających ruch atomów w czasie w wodzie i soli — delikatnie przesuwają ten kąt przez szeroki zakres i obliczają, ile energii wymaga każdy kształt. Stwierdzają, że zarówno normalna, jak i sierpowata hemoglobina mogą w temperaturze ciała eksplorować wiele takich kształtów. Hemoglobina sierpowata wykazuje nieco preferowany kąt, ale same preferencje kształtów nie tłumaczą wystarczająco, dlaczego tylko forma sierpowata tworzy stabilne włókna.
Dlaczego włókna sierpowate się trzymają, a normalne rozpadają
Aby zgłębić sedno tworzenia włókien, badanie mierzy, jak mocno sąsiadujące jednostki hemoglobiny przyciągają się wzdłuż i w poprzek włókna. Zespół oblicza energię kohezji — wynikowy ciąg, który utrzymuje jednostki razem — dla wielu różnych ogólnych kształtów. Dla hemoglobiny sierpowatej energia kohezji pozostaje ujemna (co oznacza atrakcyjną) w całym zakresie przebadanych kątów, więc włókna pozostają stabilne i nie rozpadają się łatwo. W przeciwieństwie do tego, dla normalnej hemoglobiny niektóre kształty mają dodatnią energię kohezji, co czyni włókna przy tych kątach niestabilnymi i podatnymi na spontaniczny rozpad. Kluczową różnicą jest to, jak zmienione boczne grupy waliny wsuwają się w sąsiednie białka: w hemoglobinie sierpowatej te hydrofobowe łatki tworzą trwałe kontakty zarówno w kierunku poprzecznym, jak i wzdłuż osi włókna, bezpośrednio sprzyjając wzrostowi włókien.
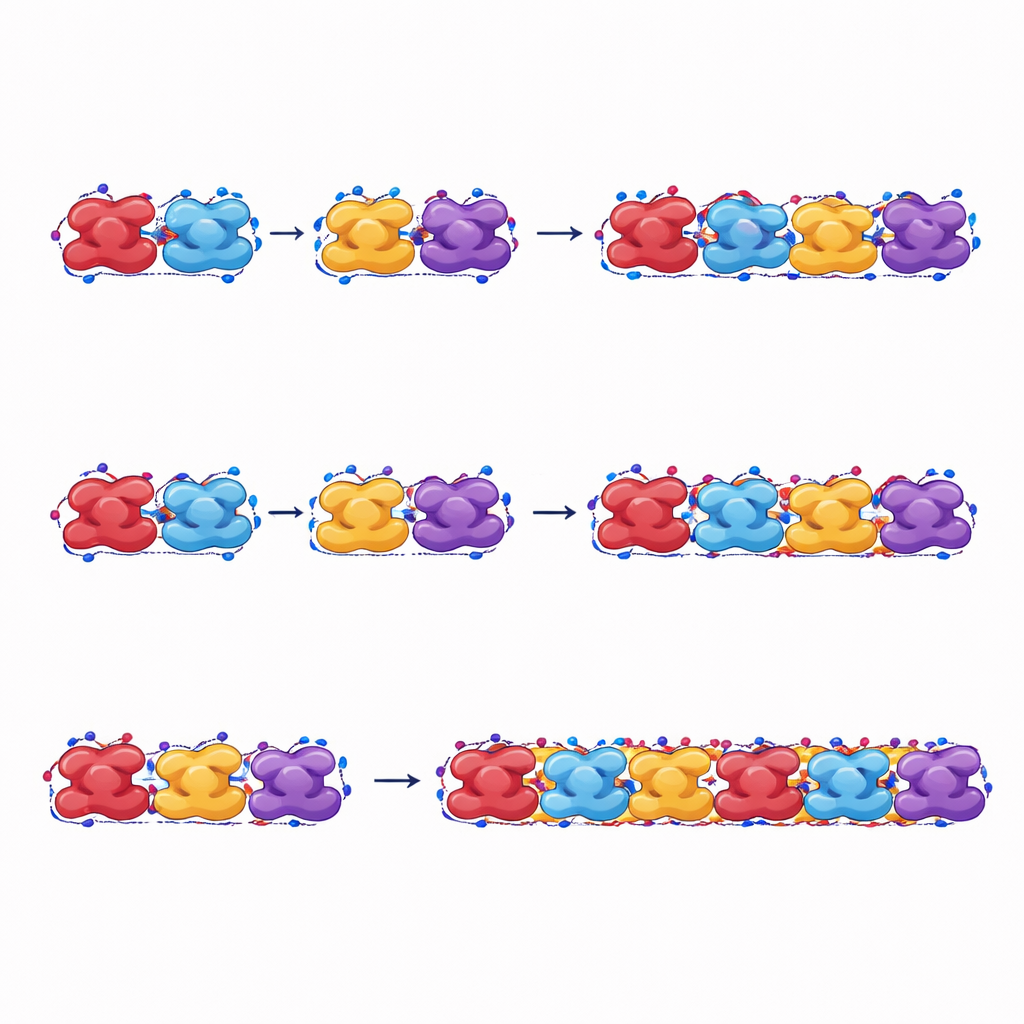
Jak te włókna przenoszą obciążenia i pękają
Autorzy rozciągają także swoje symulowane włókna, by naśladować naprężenia mechaniczne. Przy rozciąganiu wzdłuż długości włókna wykonane z hemoglobiny sierpowatej wytrzymują większe siły i odkształcenia oraz pochłaniają więcej energii przed zerwaniem niż włókna z hemoglobiny normalnej. Nawet zrelaksowana forma włókien sierpowatych, która nie jest tą, w której włókna pojawiają się najpierw, może nadal utrzymywać łańcuch dzięki plastycznym zmianom kształtu, pomagając zachować integralność włókna po jego utworzeniu. Włókna normalnej hemoglobiny natomiast łatwiej oddzielają się między sąsiednimi jednostkami i pochłaniają mniej energii przed awarią, co potwierdza, że są mniej stabilne pod obciążeniem.
Wskazówki dla przyszłych terapii i nowych materiałów
Podsumowując, symulacje pokazują, że pojedyncza zmiana aminokwasu przekształca sposób, w jaki jednostki hemoglobiny się stykają, skręcając ogólny układ w kąty sprzyjające silnemu przyciąganiu, zwłaszcza w stanie spiętym. Ta kombinacja geometrii i lepkości pozwala hemoglobinie sierpowatej tworzyć długie, sztywne włókna odporne zarówno na ruchy termiczne, jak i na naprężenia mechaniczne, które ostatecznie deformują czerwone krwinki i blokują przepływ krwi. Wskazując na konkretne cechy układu białkowego kontrolujące stabilność włókien, praca sugeruje, że skuteczne leki przeciwko sierpowatości mogłyby działać, przesuwając hemoglobinę w kierunku kształtów, w których włókna stają się energetycznie niekorzystne i mechanicznie kruche — przywracając w ten sposób śmiertelne molekularne zatory do swobodnego przepływu krwi.
Cytowanie: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
Słowa kluczowe: choroba sierpowata, włókna hemoglobiny, agregacja białek, dynamika molekularna, choroby krwi