Clear Sky Science · pl
Wypełnianie luki między obliczeniami a eksperymentem: wykorzystanie dużych modeli językowych do priorytetyzacji terapii choroby Alzheimera na podstawie porównania modeli uczących się
Dlaczego to ma znaczenie dla rodzin i pacjentów
Choroba Alzheimera odbiera ludziom pamięć, niezależność i jakość życia, a mimo to naprawdę skuteczne terapie wciąż są rzadkie. Badanie to opisuje szybszy sposób poszukiwania nowych terapii z użyciem już istniejących leków, łącząc zaawansowane modele komputerowe z dużym modelem językowym — tym samym typem AI, który dziś pojawia się w codziennych chatbotach — aby przesiać ogromne ilości danych medycznych i publikacji naukowych. Celem jest zawężenie długiej listy potencjalnych leków do małego, realistycznego zestawu, który naukowcy i lekarze faktycznie mogą przetestować u pacjentów.
Ponowne wykorzystanie starych leków w nowym celu
Opracowanie całkowicie nowego leku od podstaw może zająć ponad dekadę i kosztować miliardy dolarów, bez gwarancji powodzenia. Alternatywą jest „ponowne zastosowanie leków”, czyli poszukiwanie nowych wskazań dla preparatów już zatwierdzonych na inne schorzenia, takie jak choroba Parkinsona czy depresja. Ponieważ bezpieczeństwo tych leków jest już częściowo poznane, często można szybciej wprowadzić je do badań klinicznych w chorobie Alzheimera. Jednak nowoczesne metody komputerowe przeszukujące bazy biologiczne i literaturę medyczną generują teraz ogromne listy kandydatów — znacznie więcej, niż badacze mogą realnie ocenić ręcznie — co tworzy nowe wąskie gardło w procesie.
Łączenie wielu inteligentnych modeli
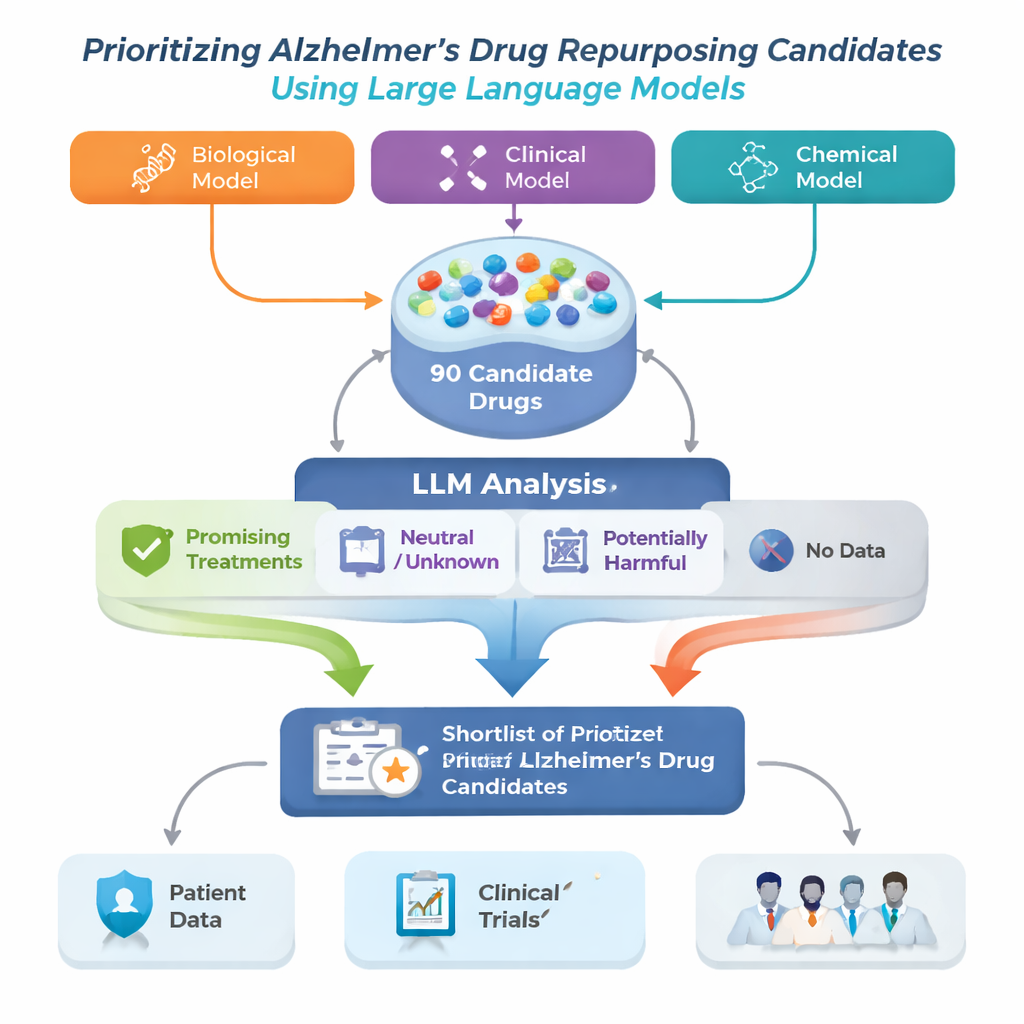
Zespół badawczy rozwiązał ten problem, tworząc ramy badawcze do ponownego zastosowania leków w chorobie Alzheimera, które zaczynały od trzech różnych zaawansowanych modeli komputerowych. Każdy model analizował duży „mapę” biomedyczną zwaną grafem wiedzy, łączącą choroby, leki, geny i inne pojęcia medyczne, i sugerował leki, które mogłyby pomóc w chorobie Alzheimera. Ponieważ każdy model rozpoznaje wzorce inaczej, ich listy nie pokrywały się w pełni. Autorzy połączyli po 30 najlepszych sugestii z każdego modelu w jedną pulę 90 kandydatów, a następnie użyli dużego modelu językowego (LLM) jako zautomatyzowanego, lecz ostrożnego recenzenta, który czytał opublikowane badania dla każdego leku i oceniał, czy dowody wyglądają na korzystne, neutralne czy szkodliwe dla choroby Alzheimera.
Jak AI czyta literaturę medyczną
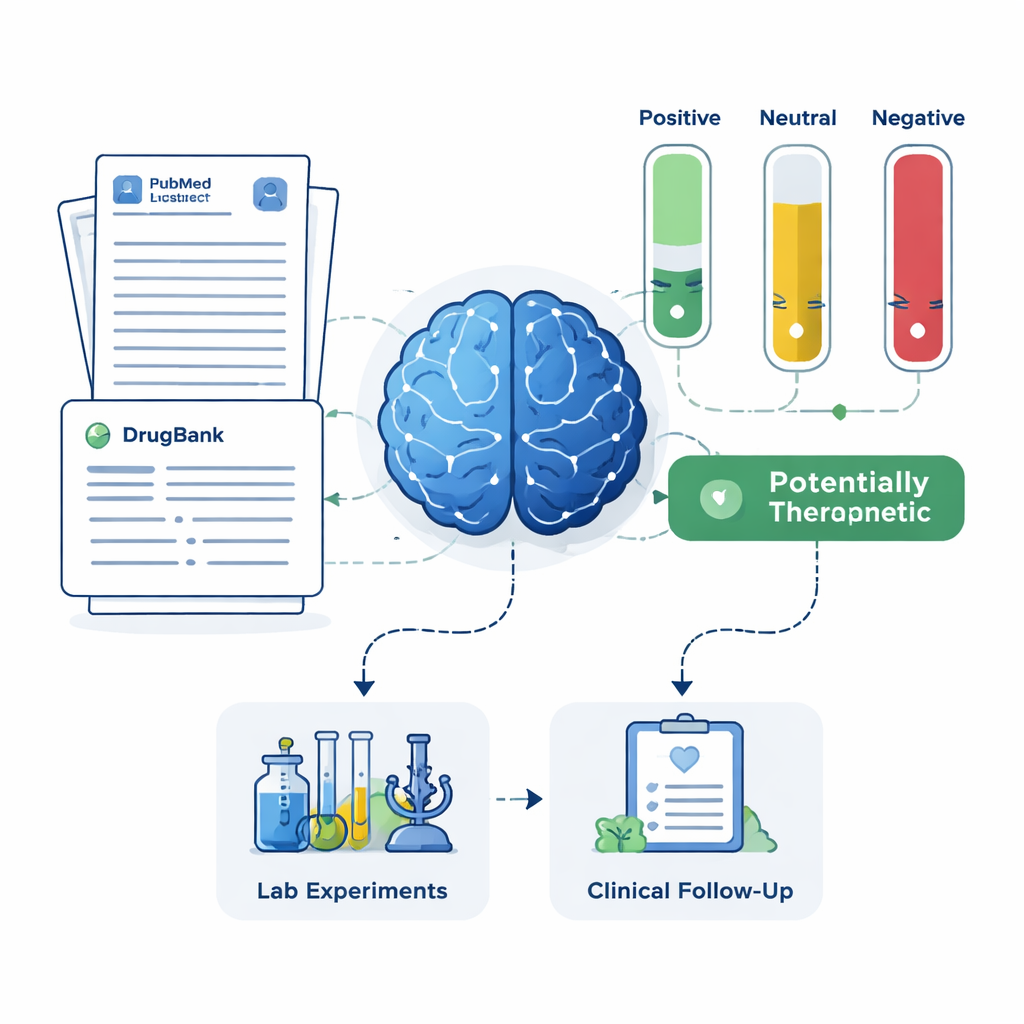
Dla każdego kandydata system pobierał do 200 streszczeń naukowych z PubMed oraz szczegółowe opisy leków z bazy farmaceutycznej. LLM otrzymał instrukcję, aby opierać ocenę wyłącznie na tekście, który mu pokazano, i oznaczać każde streszczenie jako pozytywne, neutralne lub negatywne w kontekście leczenia Alzheimera. Te etykiety przekształcono w proste punkty: udział streszczeń pozytywnych, neutralnych i negatywnych. Korzystając z dwóch zestawów reguł — surowszego wymagającego wyraźnych dowodów pozytywnych oraz łagodniejszego wyłapującego jakiekolwiek sygnały korzyści — ramy sklasyfikowały leki w cztery grupy: obiecujące terapie, potencjalnie szkodliwe, niejasne lub neutralne oraz leki bez żadnych publikacji związanych z Alzheimerem. Ta ostatnia grupa, pomimo niewielkiego stopnia badania, może skrywać szczególnie nowe możliwości.
Weryfikacja względem prawdziwych pacjentów i badań klinicznych
Aby sprawdzić, czy krótka lista AI ma sens w rzeczywistym świecie, zespół porównał jej wyniki z dwoma niezależnymi źródłami: dużym rejestrem pacjentów z chorobą Alzheimera oraz zapisami z zarejestrowanych badań klinicznych. Ramy skutecznie odnalazły memantynę, istniejący lek na Alzheimera z silnymi sygnałami ochronnymi w danych pacjentów i rozległą historią badań klinicznych, jako kandydat o wysokim priorytecie. Wyróżniono także leki takie jak magnez, minocyklina, pimawanseryna, testosteron i doksycyklina, które mają różny stopień poparcia badaniami, lecz były uważane za obiecujące przez ekspertów klinicznych. Jednocześnie system zidentyfikował leki, których literatura sugerowała możliwe szkody lub brak korzyści, rekomendując ich depopryorytetyzację lub dalsze badanie pod kątem działań niepożądanych zamiast stosowania jako terapii.
Od przewidywań komputerowych do praktycznych następnych kroków
Mówiąc prosto, te ramy działają jak ultra-szybki, uważny asystent badawczy, który czyta tysiące artykułów, sprawdza wzorce w dużych bazach medycznych i przekazuje ekspertom znacznie krótszą, lepiej zorganizowaną listę kandydatów na leki przeciwko Alzheimerowi, na których warto się skupić. Badanie pokazuje, że łącząc różne typy AI — modele oparte na grafach do generowania pomysłów oraz model językowy do oceny dowodów — badacze mogą szybciej odnaleźć zarówno dobrze uzasadnione leki, jak i intrygujące nowe opcje do testów. Choć to podejście samo w sobie nie leczy Alzheimera, oferuje potężny nowy sposób łączenia komputerowo generowanych pomysłów z ciężką pracą eksperymentów laboratoryjnych i badań klinicznych, potencjalnie przyspieszając drogę do skuteczniejszych terapii.
Cytowanie: Li, M., Niu, S., Xu, Y. et al. Bridging the computational-experimental gap: leveraging large language model to prioritize Alzheimer’s therapeutics based on comparison of learning models. npj Health Syst. 3, 20 (2026). https://doi.org/10.1038/s44401-026-00074-3
Słowa kluczowe: choroba Alzheimera, ponowne zastosowanie leków, sztuczna inteligencja, duże modele językowe, grafy wiedzy