Clear Sky Science · pl
Mutacja APP E590D zwiększa powstawanie peptydów Aβ i Aη oraz zaostrza tauopatię
Dlaczego ta rzadka mutacja ma znaczenie
Chorobę Alzheimera zwykle postrzega się jako powolne gromadzenie w mózgu dwóch szkodliwych białek — amyloidu i tau. U większości osób choroba rozwija się bez jednej oczywistej przyczyny, ale w niektórych rodzinach występują rzadkie zmiany genetyczne, które mogą radykalnie przesunąć równowagę. W artykule opisano jedną z takich nietypowych zmian w genie kodującym białko prekursorowe amyloidu (APP) i pokazano, jak może ona zwiększać wytwarzanie toksycznych fragmentów białkowych oraz nasilać proces zaplątania tau, znany jako tauopatia. Zrozumienie tego rzadkiego przypadku daje wskazówki, które mogą być dużo bardziej uniwersalne dla mechanizmów zapoczątkowujących i przyspieszających chorobę Alzheimera.
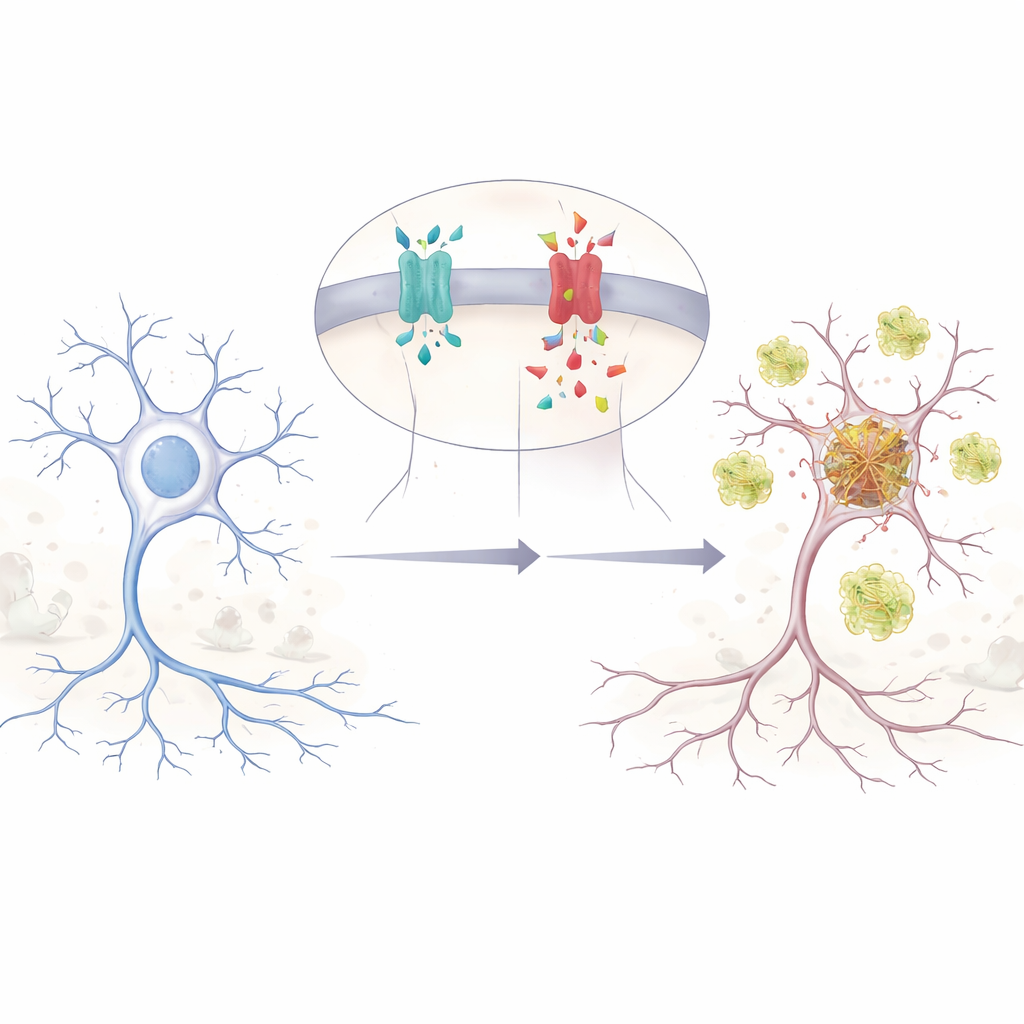
Niewielka zmiana genetyczna o dużych skutkach
Autorzy koncentrują się na zmianie jednej litery w genie APP, oznaczonej jako E590D w głównej formie APP występującej w mózgu. Mutacja została opisana tylko u dwóch osób, obie z potwierdzoną chorobą Alzheimera w stosunkowo młodym wieku i z nietypowymi, bardzo wczesnymi zaburzeniami pamięci i zachowania. Ponieważ jest tak rzadka, naukowcy nie byli pewni, czy rzeczywiście wywołuje chorobę, czy jest jedynie przypadkowym towarzyszem. Aby to sprawdzić, zespół odtworzył mutację w komórkach ludzkich i w neuronach myszy, a następnie śledził, jak APP jest rozcinane na liczne fragmenty. Odkryli, że zmutowane APP wytwarza znacznie więcej amyloidu beta (Aβ) — lepkiego peptydu od dawna związanego z Alzheimerem — niż normalne APP, gdy porówna się poziomy w sposób uczciwy.
Dwa toksyczne peptydy zamiast jednego
APP może być cięte na różne sposoby, jak pień drzewa krojony w różnych miejscach. Klasyczna ścieżka prowadzi do powstania Aβ, ale inne cięcie generuje mniej znany fragment zwany Aη. Wcześniejsze badania wykazały, że Aη może uszkadzać połączenia między komórkami nerwowymi i osłabiać zdolność mózgu do utrwalania pamięci. W swoich eksperymentach badacze stwierdzili, że mutacja E590D nie tylko zwiększa poziom Aβ; silnie podnosi też poziom Aη oraz fragmentu pośredniego, który zasila obie ścieżki. Oznacza to, że mutacja przesuwa przetwarzanie APP w kierunku podwójnego uderzenia toksycznych peptydów, co może zaburzać obwody mózgowe jeszcze zanim pojawiłyby się klasyczne płytki amyloidowe.
Jak mutacja przyspiesza wewnątrzkomórkowy transport
Aby zrozumieć, dlaczego powstaje więcej toksycznych fragmentów, zespół badał, gdzie APP lokalizuje się i porusza na powierzchni komórki. Wiele cięć prowadzących do powstania Aβ zachodzi dopiero po tym, gdy APP zostanie wciągnięte do wnętrza komórki w procesie zwanym endocytozą. Przy użyciu obrazowania i trików biochemicznych, które znakują białka na powierzchni, a następnie śledzą ich internalizację, naukowcy pokazali, że zmutowane APP jest mniej liczne na zewnątrz komórek i szybciej trafia do wnętrza niż normalne APP. Raz wczepione w wczesne endosomy, APP spotyka enzymy generujące Aβ, a zmieniony transport wydaje się dawać tym enzymom więcej okazji do działania. Jednocześnie cięcie w miejscu η na powierzchni również jest zwiększone, co wyjaśnia wzrost Aη.
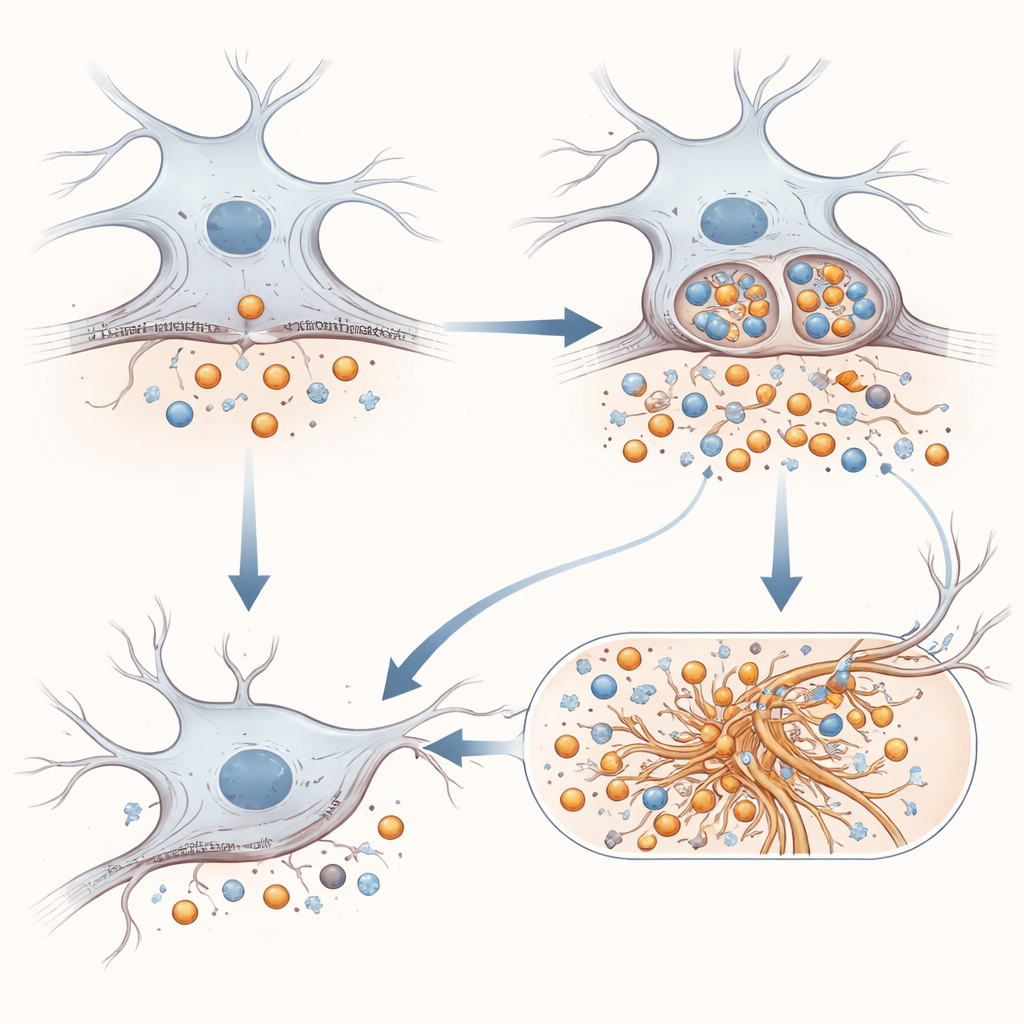
Od fragmentów białkowych do zaplątanych tau i zapalenia mózgu
Historia nie kończy się na fragmentach związanych z amyloidem. Badacze sprawdzili, czy zmutowane APP wpłynie na tau — białko strukturalne, które tworzy skręcone włókna w wielu otępieniach. W modelach komórkowych, które reagują na nasiona tau tworząc nowe skupienia, obecność APP E590D prowadziła do silniejszej agregacji niż zarówno normalne APP, jak i brak APP. W modelu myszy już podatnym na problemy z tau, wstrzyknięcie wirusa kodującego zmutowane APP do hipokampu pogłębiło splątania tau i wywołało silniejszą aktywację astrocytów i mikrogleju — komórek wspierających i odpornościowych mózgu. Co ciekawe, standardowe rozpuszczalne fragmenty amyloidu były trudne do wykrycia w tych mózgach myszy, ale charakterystyczny fragment pochodzący z APP pojawił się tylko w obecności mutacji, co sugeruje zmienione przetwarzanie w tkance żywej.
Co to znaczy dla zrozumienia choroby Alzheimera
W sumie wyniki pokazują, że ta rzadka mutacja APP nie jest obojętna. Skłania APP do wytwarzania więcej niż jednego toksycznego peptydu, przyspiesza kroki internalizacji sprzyjające szkodliwym cięciom oraz wzmacnia zaplątanie tau i stan zapalny w mózgu. Dla osób niemających specjalistycznej wiedzy kluczowy wniosek jest taki, że biologia choroby Alzheimera nie napędzana jest przez jednego złoczyńcę, lecz przez sieć współdziałających fragmentów białkowych i reakcji komórkowych. Badanie takich silnych, choć nietypowych wariantów genetycznych daje powiększony obraz tej sieci. W omawianym przypadku sugeruje to, że terapie mogą wymagać uwzględnienia zarówno amyloidu, jak i alternatywnych peptydów pochodzących z APP, takich jak Aη, oraz ich łącznego wpływu na tau, zamiast celowania tylko w jedną ścieżkę izolacyjnie.
Cytowanie: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
Słowa kluczowe: choroba Alzheimera, białko prekursorowe amyloidu, sploty tau, neurozapalenie, mutacja genetyczna