Clear Sky Science · pl
Wysokoprzepustowa, ilościowa platforma wykorzystująca 2D dysocjowane ludzkie organoidy mózgowe do modelowania neurozapalnych procesów w chorobie Alzheimera
Dlaczego infekcje mogą mieć znaczenie dla utraty pamięci
Choroba Alzheimera jest zwykle opisywana jako powolne odkładanie się lepkich białek w mózgu, ale rosnące dowody sugerują, że infekcje mogą pomóc zainicjować ten proces. W badaniu tym autorzy badają ten pomysł, korzystając z małych, hodowanych w laboratorium modeli ludzkiego mózgu, zadając proste pytanie: czy powszechny wirus powodujący opryszczkę może wywołać zmiany podobne do alzheimerowskich w ludzkich komórkach mózgowych, a czy lek przeciwwirusowy może te zmiany cofnąć?
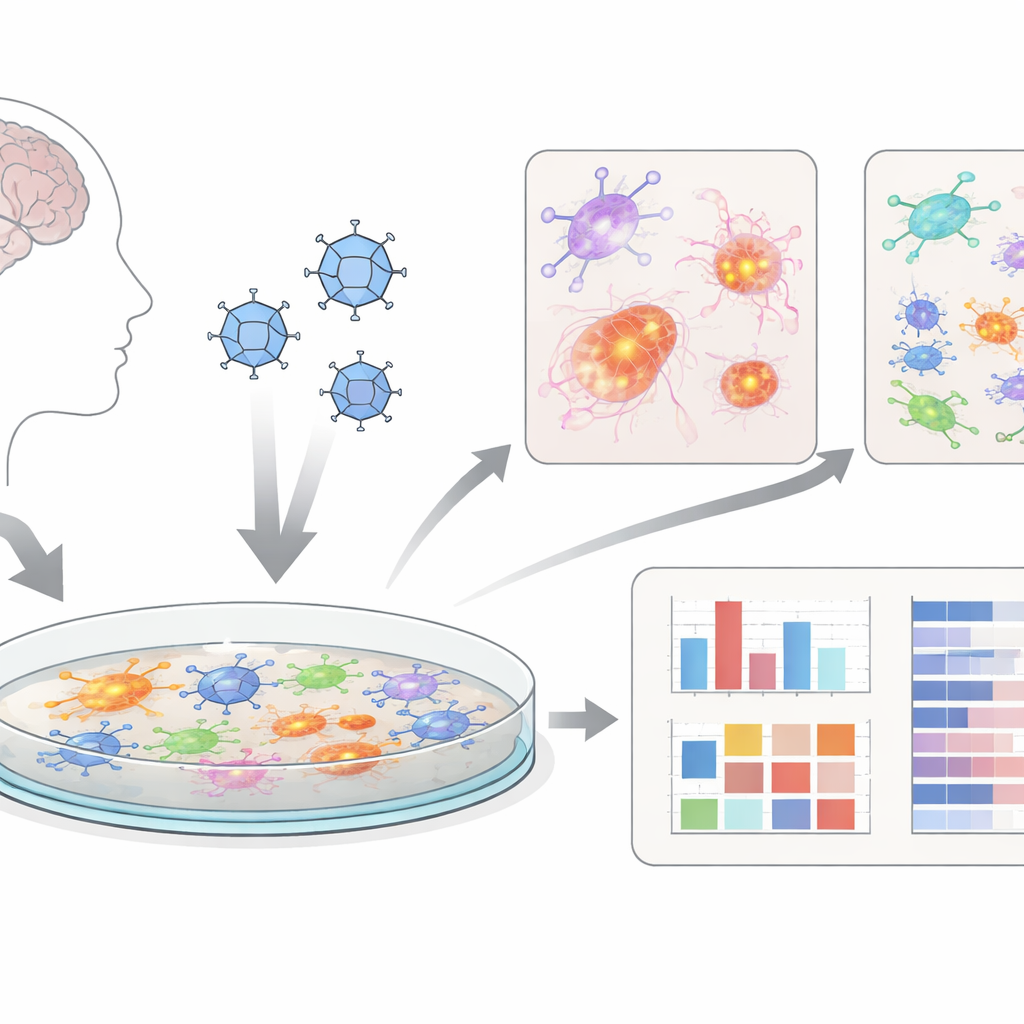
Mini-mózgi na szalce
Zamiast pracować wyłącznie na zwierzętach, badacze użyli „organoidów mózgowych” – skupisk komórek przypominających mózg, hodowanych z ludzkich komórek macierzystych. Następnie delikatnie rozdzielili te trójwymiarowe organoidy na płaskie warstwy mieszanych komórek mózgowych, w tym neuronów, komórek podporowych zwanych astrocytami oraz komórek przypominających układowe komórki odpornościowe – mikrogleju. Te dwuwymiarowe kultury, które nazwali dcOrgs, łatwiej zakażać równomiernie i testować w wysokoprzepustowy sposób, co oznacza, że można równolegle badać wiele płytek i warunków lekowych. To sprawia, że system jest atrakcyjny jako narzędzie przesiewowe nowych terapii.
Wirus opryszczki jako iskra
Zespół zakażył dcOrgs wirusem herpes simplex 1 (HSV-1), wirusem odpowiedzialnym za większość opryszczek wargowych i od dawna podejrzewanym o wkład w rozwój demencji u niektórych osób. Porównali zakażone hodowle z kontrolami traktowanymi pozorowo, z hodowlami podanymi lekiem przeciwwirusowym (acyklowirem), z hodowlami narażonymi na inny wirus (grypy A) oraz z wirusem inaktywowanym światłem ultrafioletowym. Przy użyciu zautomatyzowanej analizy komórek i sekwencjonowania pojedynczych komórek potwierdzili, że HSV-1 silnie zakaża wiele typów komórek w hodowli, podczas gdy wirus inaktywowany i wirus grypy wywołały bardzo odmienne, łagodniejsze wzorce zmian.
Zmiany przypominające Alzheimera wewnątrz i między komórkami
W dcOrgs zakażonych HSV-1 wiele komórek gromadziło wysokie poziomy tych samych form białek obserwowanych w mózgach chorych na Alzheimera: zlepiony beta-amyloid wewnątrz komórek oraz różne „zfosforylowane” postaci tau, kolejnego kluczowego białka chorobowego. Te odkładanie były najsilniej powiązane z komórkami zawierającymi białka wirusowe i były szczególnie intensywne w komórkach umierających. Jednocześnie mniej dłuższego fragmentu beta-amyloidu (Aβ42) uwalniało się do płynu otaczającego w stosunku do krótszych form, co odzwierciedla wzorce mierzone w płynie mózgowo-rdzeniowym pacjentów z chorobą Alzheimera. Zmieniały się także populacje komórek: liczba neuronów spadła, podczas gdy astrocyty i mikroglej się zwiększyły, co echo utraty neuronów i reaktywnego zapalenia obserwowanego w tkankach mózgowych pacjentów.
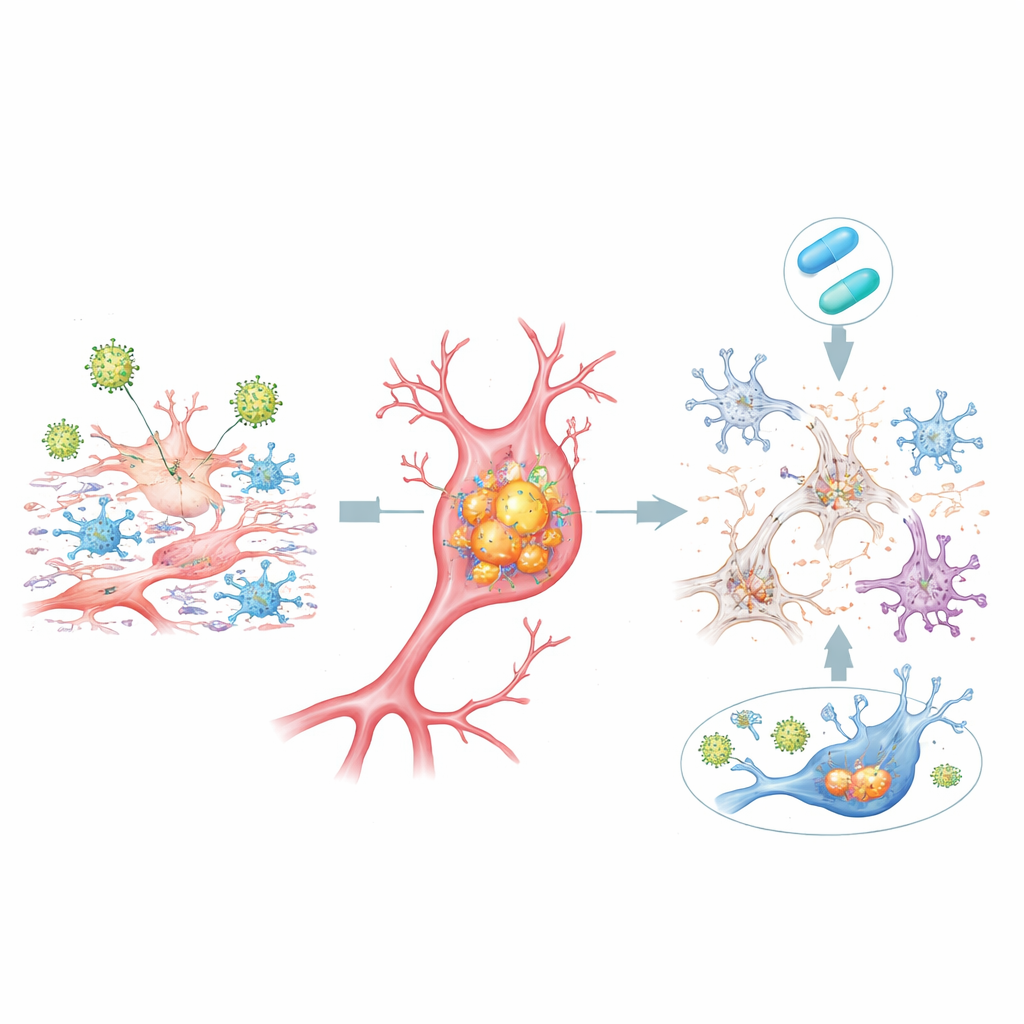
Aktywność genów łączy model z ludzkim Alzheimerem
Gdy badacze zbadali aktywność genów w całym genomie, odkryli, że zakażenie HSV-1 w dcOrgs włączało i wyłączało wiele genów wcześniej powiązanych z ryzykiem choroby Alzheimera w dużych badaniach genetycznych ludzi. Zmian tych nie obserwowano w prostszych kulturach komórek macierzystych ani w dcOrgs zakażonych wirusem grypy, co sugeruje specyficzną interakcję między HSV-1 a zróżnicowanym, przypominającym mózg środowiskiem. Sekwencjonowanie pojedynczych komórek ujawniło, że część przesunięć genów powiązanych z Alzheimerem pochodziła z komórek, które były wystawione na działanie wirusa, lecz same zawierały niewiele lub wcale materiału genetycznego wirusa, co sugeruje, że sygnały od zakażonych sąsiadów mogą rozprzestrzeniać szkodliwe programy zapalne.
Co leczenie przeciwwirusowe może, a czego nie może naprawić
Dodanie leku przeciwwirusowego acyklowiru wkrótce po ekspozycji na HSV-1 zmniejszyło ekspresję genów wirusowych, stłumiło wiele odpowiedzi zapalnych, obniżyło gromadzenie toksycznego beta-amyloidu i tau wewnątrz komórek oraz częściowo przywróciło równowagę różnych typów komórek. Dla znacznej części genów powiązanych z Alzheimerem poziomy ich aktywności przesunęły się z powrotem w kierunku normy. Jednak nie wszystkie zmiany były odwracalne: pokaźna grupa ludzkich genów pozostała bez zmian lub została nawet bardziej zaburzona przez leczenie, szczególnie gdy lek był mniej skuteczny w hamowaniu późnych genów wirusowych. Podkreśla to, że zatrzymanie replikacji wirusa może pomóc, ale może nie całkowicie cofnąć kaskady biologicznej, gdy już się zaczęła.
Co to oznacza dla zrozumienia Alzheimera
Dla osoby niebędącej specjalistą wniosek jest taki, że ludzki wirus powodujący opryszczkę, działając w realistycznym koktajlu ludzkich komórek mózgowych, może szybko wywołać wiele cech charakterystycznych dla choroby Alzheimera – od grudek białkowych i umierających neuronów po wzorce genetyczne już widziane u pacjentów. Oparty na płaskich organoidach system opracowany tutaj jest szybki, ilościowy i skalowalny, co czyni go potężnym polem do testowania leków przeciwwirusowych i innych terapii mających na celu złagodzenie zapalenia mózgu. Chociaż nie dowodzi to, że infekcje wirusem opryszczki powodują Alzheimera u każdego pacjenta, wzmacnia argument, że u podzbioru osób przewlekłe lub reaktywowane infekcje wirusowe mogą być istotnym elementem układanki – i potencjalnym celem zapobiegania.
Cytowanie: Olson, M.N., Barton, N.J., Feng, L. et al. A high-throughput, quantitative platform using 2D dissociated human cerebral organoids to model neuroinflammation in Alzheimer’s disease. npj Dement. 2, 20 (2026). https://doi.org/10.1038/s44400-026-00066-y
Słowa kluczowe: choroba Alzheimera, wirus opryszczki zwykłej, organoidy mózgowe, neurozapalność, terapia przeciwwirusowa