Clear Sky Science · pl
15 lat pomiarów genetycznych, klinicznych, poznawczych, obrazowych i biochemicznych w DIAN
Dlaczego to ma znaczenie dla rodzin i przyszłości leczenia Alzheimera
Większość osób myśli o chorobie Alzheimera jako o czymś, co pojawia się późno w życiu, często bez ostrzeżenia. Jednak w niewielu rodzinach konkretne dziedziczne zmiany genetyczne niemal gwarantują rozwój choroby w stosunkowo młodym wieku. Obserwacyjne badanie Dominantly Inherited Alzheimer Network (DIAN) przez 15 lat uważnie śledziło takie rodziny na całym świecie. Obserwując, jak choroba rozwija się na długo przed pojawieniem się problemów z pamięcią, DIAN ujawnia szczegółowy harmonogram zmian w mózgu, który może pomóc lekarzom wykrywać, zapobiegać lub opóźniać Alzheimera u znacznie większej liczby osób.
Globalne przedsięwzięcie śledzące rodziny wysokiego ryzyka
DIAN śledzi dorosłych z rodzin noszących rzadkie mutacje w trzech genach związanych z dziedziczną postacią choroby Alzheimera. Część uczestników ma mutację, część nie, ale badanie nie informuje nikogo o jego statusie genetycznym, chyba że zdecyduje się na oddzielne badania kliniczne. Projekt rozpoczął się w 2008 roku z 10 ośrodkami w trzech krajach i rozrósł do 23 ośrodków w 11 krajach, pracując w siedmiu językach. Do badania zapisało się ponad 660 osób, z których ponad 300 nadal aktywnie uczestniczy. Podczas regularnych wizyt ochotnicy przechodzą badania medyczne i testy pamięci, skany mózgu, badania płynu mózgowo‑rdzeniowego i krwi oraz, dla tych którzy wyrażą zgodę, darowiznę mózgu po śmierci. Krewni niebędący nosicielami służą jako wyjątkowo dobrze dopasowana grupa porównawcza, pomagając badaczom odróżnić normalne starzenie się od zmian związanych z chorobą.
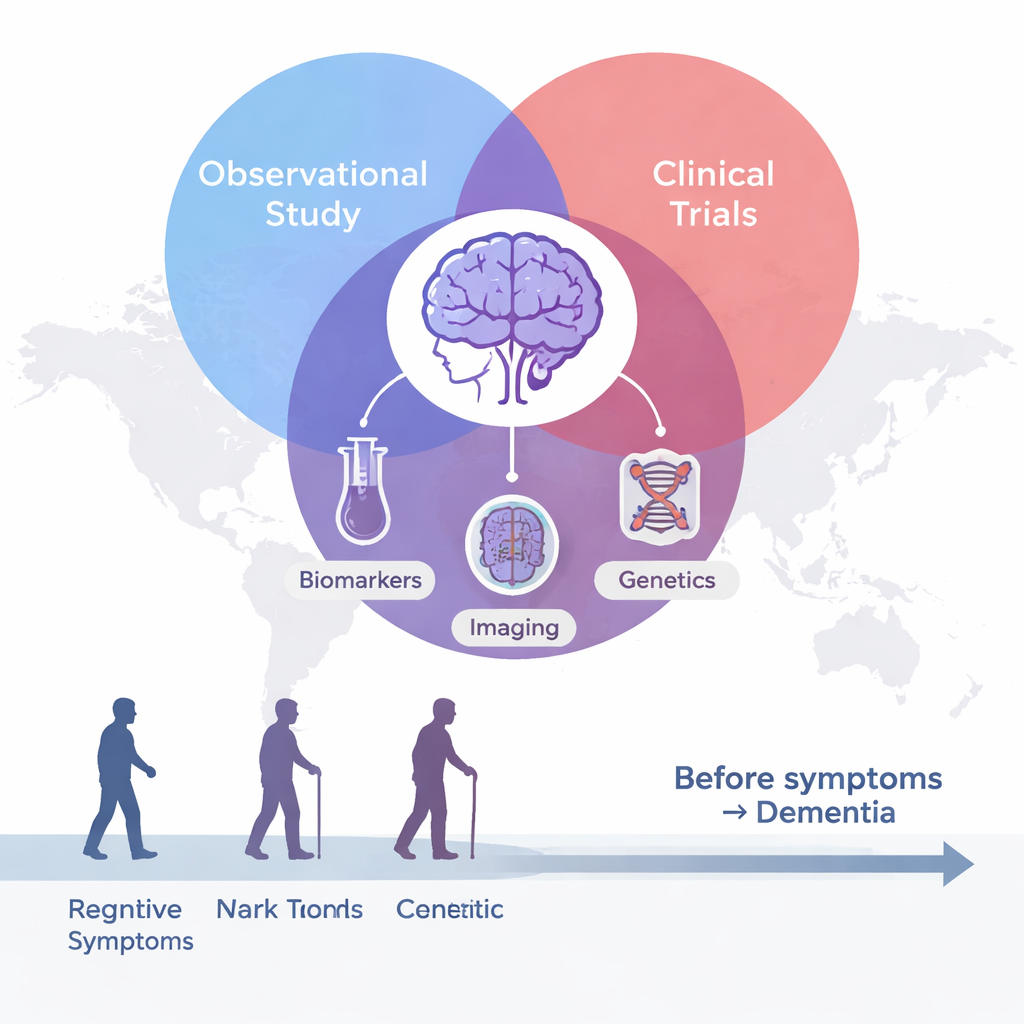
Widzieć chorobę dziesięciolecia przed objawami
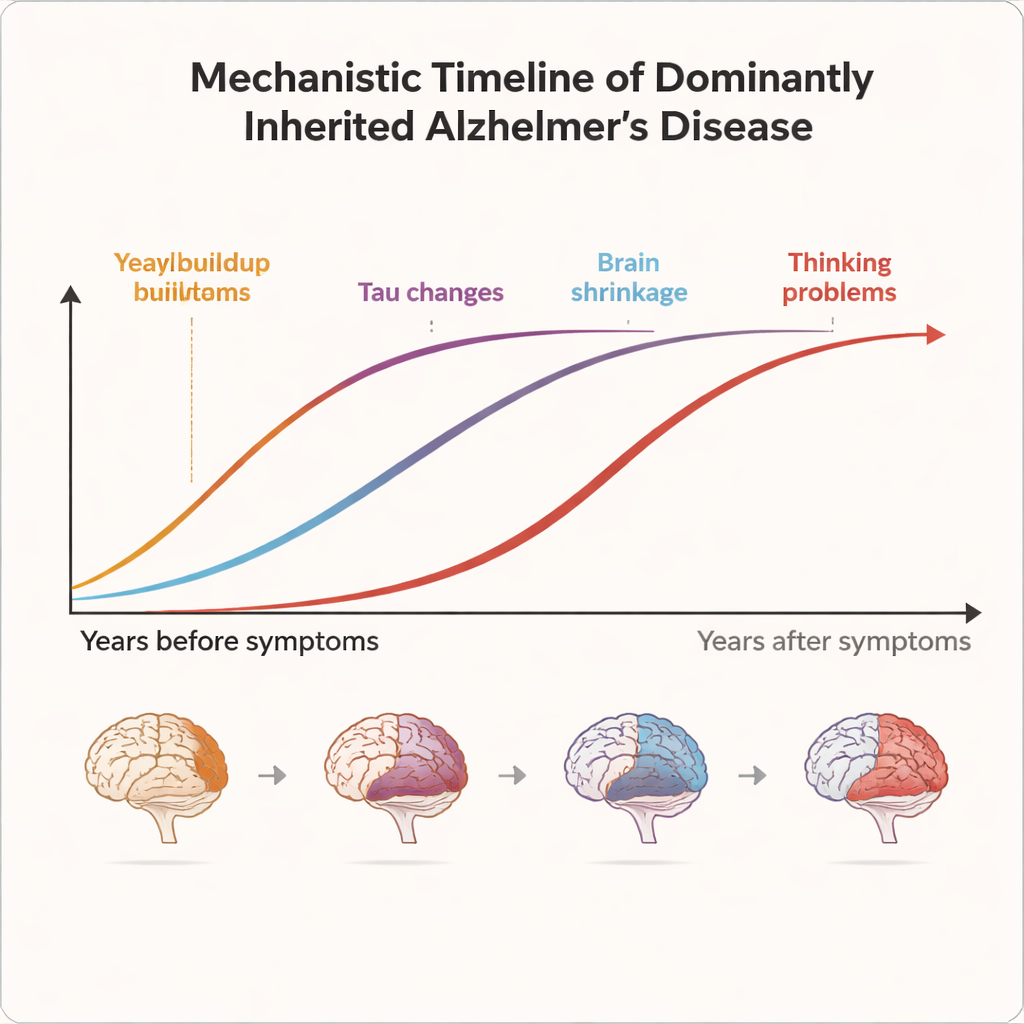
Ponieważ wiek, w którym zwykle rozpoczynają się objawy, jest stosunkowo przewidywalny w ramach każdej rodziny, badacze mogą oszacować, ile lat dzieli każdego nosiciela od prawdopodobnego początku choroby. Pozwala to ustawić osoby wzdłuż „zegara choroby”, od ponad 20 lat przed początkiem problemów do wielu lat po nim. Wyniki DIAN pokazują, że Alzheimer nie jest nagłym wydarzeniem, lecz długim procesem. Lepiące się grudki białkowe zwane płytkami amyloidowymi zaczynają gromadzić się w mózgu 15–20 lat przed objawami, wykrywalne na specjalistycznych skanach PET i odzwierciedlane przez spadek jednego z rodzajów amyloidu w płynie mózgowo‑rdzeniowym. Około 10–15 lat przed oczekiwanym początkiem pojawiają się kolejne sygnały ostrzegawcze: nieprawidłowe białka tau rosną w płynie mózgowo‑rdzeniowym, spowalnia metabolizm mózgu, a na skanach MRI pojawia się subtelne przerzedzenie kory. Dopiero kilka lat później zmiany w myśleniu i funkcjonowaniu w codziennym życiu stają się wykrywalne przy użyciu szczegółowych testów poznawczych.
Żywa biblioteka pomiarów i próbek
Aby przekształcić te obserwacje w naukę o szerokim zastosowaniu, DIAN zbudował jeden z najbogatszych zbiorów danych i tkanek związanych z chorobą Alzheimera na świecie. Osiem wyspecjalizowanych rdzeni zarządza informacjami klinicznymi, testami poznawczymi, obrazowaniem mózgu, biomarkerami płynów, genetyką, patologią mózgu, statystyką i ogólną administracją. Próbki krwi i płynu mózgowo‑rdzeniowego są przetwarzane w centralnym biobanku, gdzie zaawansowane narzędzia mierzą dziesiątki białek związanych z amyloidem, tau, stanem zapalnym i uszkodzeniem komórek nerwowych. Analizy genetyczne i „multi‑omiczne” badają DNA, RNA, białka, lipidy i inne cząsteczki we krwi, tkance mózgowej i modelach komórkowych pochodzących od uczestników. Rozwijający się program neuropatologii dokładnie bada przekazane mózgi, aby potwierdzić diagnozy i stadium choroby. Wszystkie te informacje są czyszczone, sprawdzane pod względem jakości i zamrażane w rocznych zestawach danych, o które zewnętrzni badacze mogą występować przy zachowaniu surowych zabezpieczeń prywatności.
Napędzanie badań klinicznych i narzędzi następnej generacji
DIAN to nie tylko badanie tego, co dzieje się naturalnie; jest też fundamentem towarzyszącego programu badań klinicznych testujących leki mające na celu spowolnienie lub zapobieganie dziedzicznej postaci Alzheimera. Ponieważ badania obserwacyjne i lecznicze stosują ujednolicone procedury, ich wyniki można łączyć i porównywać. Szczegółowy harmonogram zmian w mózgu opracowany przez DIAN pomógł już ukształtować międzynarodowe kryteria definiowania Alzheimera biologicznie, w oparciu o markery amyloidu, tau i neurodegeneracji, a nie tylko o same objawy. Patrząc w przyszłość, sieć rozszerza działania o zdalne oceny za pomocą aplikacji na smartfony, wizyt domowych i urządzeń noszonych, aby wykrywać bardzo wczesne zmiany poznawcze i śledzić funkcjonowanie w codziennym życiu. Inwestuje też intensywnie w testy oparte na krwi oraz głębsze profilowanie molekularne, aby znaleźć nowe cele terapeutyczne i zrozumieć, dlaczego przebieg choroby różni się między osobami i populacjami.
Co to oznacza dla osób zaniepokojonych Alzheimerem
Badanie DIAN pokazuje, że w dziedzicznej postaci Alzheimera mózg zaczyna się zmieniać wiele lat przed utratą pamięci — i że te ukryte przesunięcia można mierzyć we krwi, płynie mózgowo‑rdzeniowym i skanach. Chociaż badane mutacje są rzadkie, leżący u ich podstaw proces chorobowy wydaje się ściśle przypominać ten występujący w znacznie bardziej powszechnej postaci o późnym początku. To sprawia, że DIAN jest potężnym modelem dla całej dziedziny. Mapując krok po kroku drogę od zdrowego mózgu do otępienia i dzieląc się starannie zgromadzonymi zasobami na całym świecie, DIAN pomaga naukowcom projektować wcześniejsze i bardziej precyzyjne interwencje. Dla rodzin z ryzykiem dziedzicznym i dla milionów osób dotkniętych chorobą Alzheimera bardziej ogólnie, te wnioski oferują jaśniejszą ścieżkę ku wcześniejszemu wykrywaniu, lepszemu monitorowaniu, a ostatecznie skuteczniejszej prewencji i terapii.
Cytowanie: Daniels, A.J., McDade, E., Llibre-Guerra, J.J. et al. 15 years of longitudinal genetic, clinical, cognitive, imaging, and biochemical measures in DIAN. npj Dement. 2, 13 (2026). https://doi.org/10.1038/s44400-025-00047-7
Słowa kluczowe: choroba Alzheimera, genetyczna otępienie, biomarkery mózgowe, badanie podłużne, wczesne wykrywanie