Clear Sky Science · pl
Kodowanie krawędzi funkcjonalnych w grafach w celu modelowania przestrzennie zmiennych zależności w mikrośrodowisku guza
Dlaczego mapowanie „sąsiedztwa” raka ma znaczenie
Nowotwór nie rozwija się w izolacji. Komórki nowotworowe żyją w zatłoczonym otoczeniu komórek odpornościowych, komórek wspierających, naczyń krwionośnych i sygnałów chemicznych, wszystkie blisko siebie w przestrzeni. To, jak są rozmieszczeni sąsiedzi i jak silnie na siebie wpływają, może decydować o tym, czy rak się rozsiewa, reaguje na terapię czy pozostaje w uśpieniu. Artykuł przedstawia SPIFEE, nowe ramy sztucznej inteligencji, które przekształcają obrazy mikroskopowe i molekularne mapy guzów w sieci, pomagając badaczom wskazać, które interakcje komórkowe i szlaki są najbardziej związane z typem choroby i wynikami pacjenta.
Przekształcanie tkanki w mapę sieciową
Współczesne badania nad rakiem potrafią zmierzyć znacznie więcej niż to, jak guz wygląda pod mikroskopem. Niektóre metody uwidaczniają dziesiątki białek na pojedynczych komórkach, inne dostarczają szczegółowych barwnych skanów struktury tkanki, a nowsze narzędzia rejestrują, które geny są aktywne w tysiącach miejsc na przekroju guza. SPIFEE traktuje to wszystko jako różne spojrzenia na to samo „sąsiedztwo”. Reprezentuje każdy próbkę jako graf: węzły oznaczają kluczowe byty w mikrośrodowisku guza — takie jak typy komórek, wzorce wizualne tkanki czy szlaki molekularne — podczas gdy krawędzie opisują, jak te byty wchodzą w interakcje w przestrzeni. Co istotne, SPIFEE nie sprowadza interakcji do jednego wskaźnika, jak „odległość”. Zamiast tego każda krawędź przechowuje niewielką krzywą opisującą, jak silnie dwie jednostki mieszają się lub odpychają w zależności od zakresu odległości, zachowując znacznie bogatsze informacje przestrzenne.
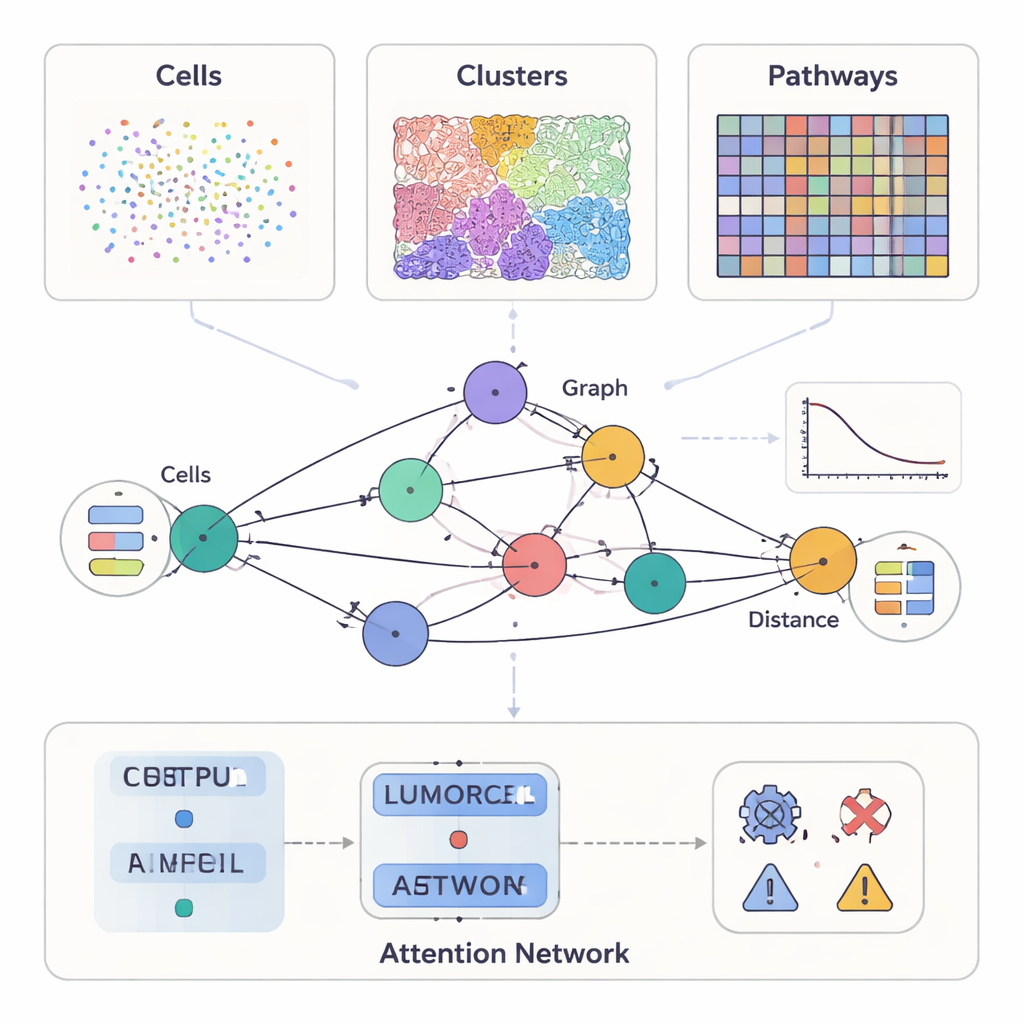
Elastyczne spojrzenie na różne rodzaje danych nowotworowych
Autorzy przetestowali SPIFEE na kilku dużych, niezależnych zbiorach danych nowotworowych obejmujących różne technologie i skale. W próbkach trzustki opatrzonych multipleksową immunofluorescencją każdy węzeł grafu reprezentował typ komórki, a cechy węzła pochodziły z sekwencjonowania RNA pojedynczych komórek, które podsumowywało, jak te komórki zwykle komunikują się między sobą. Na skanach płuc barwionych rutynową metodą hematoksyliny i eozyny węzły reprezentowały powtarzalne wzorce wizualne tkanki, odkryte automatycznie przez system uczenia samo-nadzorowanego. W trzecim przypadku standardowe skany płuc zostały przekształcone przez narzędzie deep learningowe w wirtualną transkryptomikę przestrzenną, a węzły SPIFEE reprezentowały szlaki molekularne takie jak niedotlenienie, estrogen czy sygnalizacja JAK–STAT, z cechami pochodzącymi z aktywności genów. We wszystkich tych ustawieniach ten sam framework mógł przyjmować różne typy węzłów i nadal budować porównywalne grafy przestrzenne.
Wyszukiwanie interakcji rozdzielających wyniki zdrowotne
Gdy SPIFEE buduje graf, przekazuje go przez grafową sieć uwagi (graph attention network), rodzaj sieci neuronowej, która uczy się nie tylko przewidywać wynik — taki jak podtyp nowotworu, ryzyko przeżycia czy choroba kontra zapalenie niezłośliwe — ale także podkreślać, które krawędzie miały największe znaczenie dla tego przewidywania. W tkance trzustki SPIFEE rozróżniał przewlekłe zapalenie trzustki od gruczolakoraka przewodowego trzustki z wyższą dokładnością niż wcześniejsze metody oparte na grafach. Model konsekwentnie skupiał się na interakcjach obejmujących komórki nabłonkowe (podobne do nowotworowych) oraz limfocyty T regulatorowe, komórki prezentujące antygen i pomocnicze limfocyty T, wskazując na immunosupresyjne otoczenie, które jest bardziej wyraźne w raku niż w zapaleniu. Na skanach gruczolakoraka płuca SPIFEE identyfikował konkretne wzorce między zrębem a guzem, których interakcje korelowały z lepszym lub gorszym przeżyciem, sugerując, że „strefy brzegowe” między guzem a tkanką wspierającą zawierają istotne prognostyczne wskazówki, które standardowe analizy mogą przeoczyć.
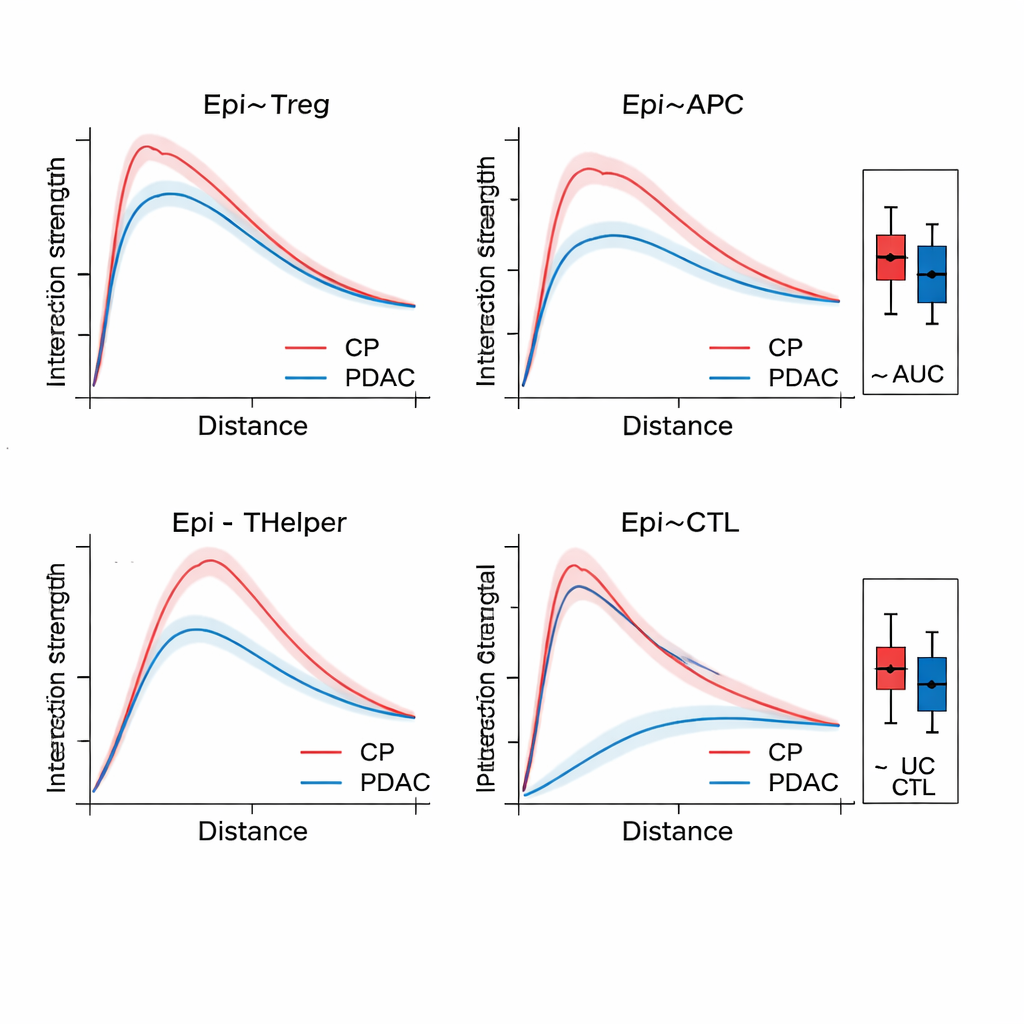
Odczytywanie molekularnej wymiany informacji ze standardowych preparatów
Być może najbardziej uderzające jest to, że SPIFEE potrafił wywnioskować istotne interakcje szlaków z zwykłych obrazów patologicznych, gdy te zostały przekładane na przewidywane mapy aktywności genów. Traktując szlaki jako węzły i ich przestrzenną współwystępowalność jako krawędzie funkcjonalne, metoda uwypukliła pary takie jak niedotlenienie z EGFR czy JAK–STAT z PI3K — kombinacje już znane z napędzania ucieczki immunologicznej i oporności na leki w raku płuca. Zidentyfikowała także szlaki związane z estrogenem w gruczolakoraku płuca oraz pewne szlaki odpornościowe i stresowe w nowotworach płaskonabłonkowych, obserwacje zgodne z wzorcami widzianymi w sekwencjonowaniu RNA z całego materiału oraz w niezależnym, rzeczywistym zbiorze danych transkryptomiki przestrzennej. To sugeruje, że nawet gdy pomiary molekularne są przybliżone, wzorce przestrzenne na rutynowych preparatach nadal niosą odzyskiwalne sygnały o tym, jak kluczowe szlaki wchodzą w interakcje w żywych guzach.
Co to oznacza dla przyszłej opieki onkologicznej
Dla osoby niebędącej specjalistą główny przekaz jest taki, że SPIFEE oferuje nowy sposób odczytywania „życia społecznego” komórek nowotworowych bezpośrednio z obrazów i map molekularnych. Poprzez kodowanie tego, jak zależności zmieniają się z odległością zamiast spłaszczania ich do pojedynczych wskaźników, oraz przez wykorzystanie sieci neuronowych opartych na mechanizmie uwagi do uszeregowania, które interakcje są najważniejsze, framework może ujawnić kombinacje komórek, wzorców tkankowych i szlaków, które rozróżniają typy nowotworów i przewidują przeżycie. Chociaż te odkrycia wciąż wymagają biologicznej i klinicznej weryfikacji, podejścia takie jak SPIFEE wskazują na przyszłość, w której rutynowe próbki guzów mogą dostarczać nie tylko statycznych zdjęć, ale dynamicznych map miejsc intensywnych interakcji, które pomagają w diagnostyce, stratyfikacji ryzyka, a w końcu w spersonalizowanym wyborze terapii.
Cytowanie: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
Słowa kluczowe: mikrośrodowisko guza, transkryptomika przestrzenna, grafowe sieci neuronowe, patologia nowotworowa, interakcje międzykomórkowe