Clear Sky Science · pl
Sieć neuronowa wykorzystująca wiedzę o metabolizmie identyfikuje szlaki wpływające na skuteczność i toksyczność kombinacji środków przeciwbakteryjnych
Dlaczego to ma znaczenie dla codziennego zdrowia
W miarę jak coraz więcej zakażeń przestaje reagować na nasze podstawowe antybiotyki, lekarze coraz częściej sięgają po kombinacje leków. Jednak mieszanie leków bywa obosieczne: odpowiednie połączenie może usunąć uporczywe bakterie, podczas gdy nieodpowiednie może uszkodzić organy takie jak nerki i wątroba. W tym badaniu przedstawiono nowe podejście komputerowe, nazwane CALMA, zaprojektowane, by pomóc naukowcom i klinicystom odnaleźć kombinacje leków jednocześnie silne wobec drobnoustrojów i łagodniejsze dla pacjentów.
Walka z zarazkami bez żmudnych prób i błędów
Tradycyjnie odkrywanie dobrych kombinacji antybiotyków oznaczało testowanie ogromnej liczby par lub trójek leków w laboratorium i u pacjentów. Liczba możliwych mieszanin rośnie wykładniczo wraz z dodawaniem kolejnych leków, co sprawia, że pełne testy eksperymentalne są nierealistyczne. Na dodatek większość istniejących narzędzi skupia się wyłącznie na tym, jak silnie kombinacje zabijają bakterie, ignorując, jak mogą uszkadzać tkanki ludzkie. Autorzy argumentują, że aby projektować lepsze terapie, trzeba uwzględniać obie strony równania: skuteczność wobec patogenów i bezpieczeństwo dla ludzi.
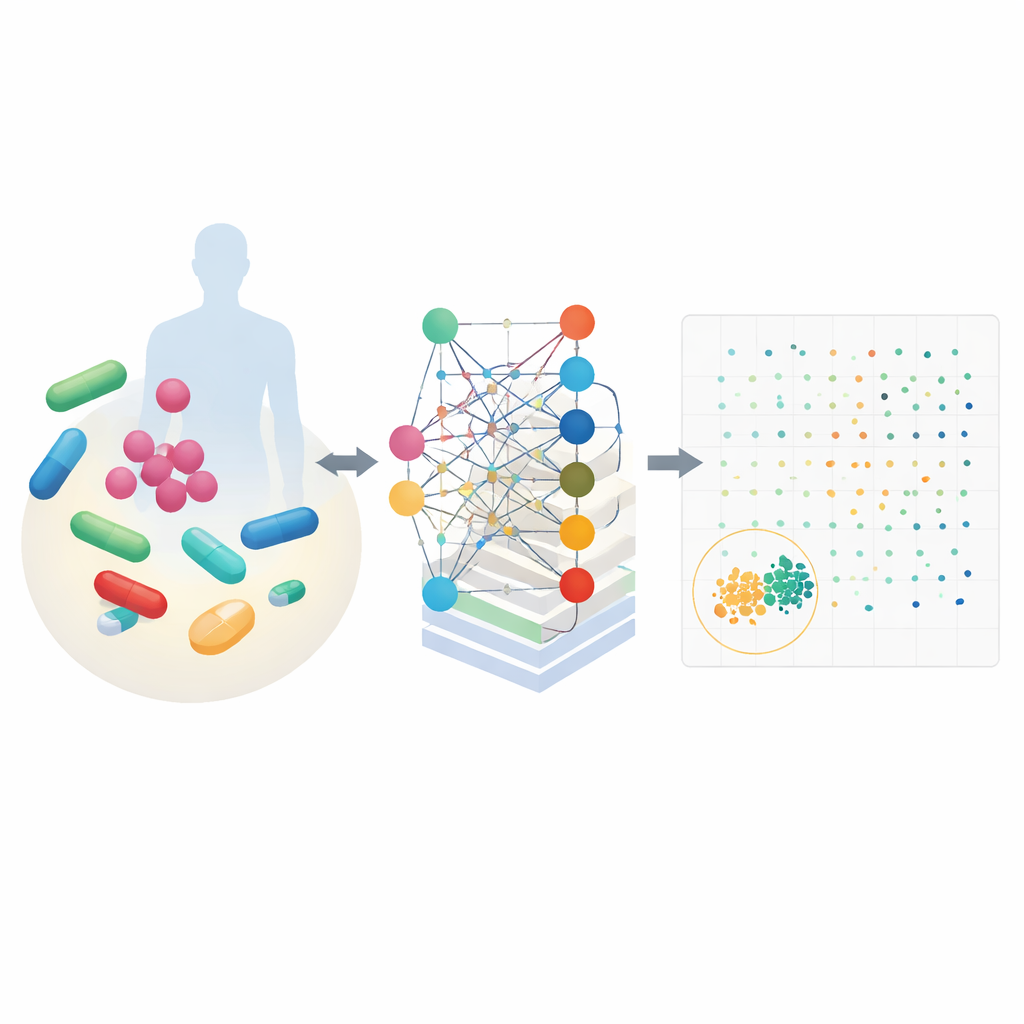
Inteligentny model, który rozumie chemię komórkową
CALMA łączy dwie mocne idee. Po pierwsze, wykorzystuje szczegółowe mapy metabolizmu komórkowego, które opisują, jak organizmy przekształcają składniki odżywcze w energię i materiały budulcowe. Te mapy, opracowane dla bakterii takich jak Escherichia coli oraz prątek gruźlicy, symulują, jak tysiące reakcji chemicznych zmienia się pod wpływem leku. Po drugie, CALMA wprowadza te symulacje do sztucznej sieci neuronowej, której struktura odzwierciedla szlaki metaboliczne. Grupując informacje według znanych dróg biologicznych — na przykład wytwarzania energii czy recyklingu nukleotydów — model uczy się wzorców łączących konkretne szlaki z efektywnym zabijaniem bakterii lub z szkodliwymi skutkami u komórek ludzkich.
Skanowanie krajobrazu mieszanin leków
Wykorzystując dane z wcześniejszych eksperymentów i duże bazy bezpieczeństwa, badacze wytrenowali CALMA tak, by przypisywała każdej kombinacji leków dwie oceny: jedną za to, jak silnie atakuje bakterie, i drugą za to, jak prawdopodobne jest, że będzie toksyczna dla ludzi. Rysując te oceny otrzymuje się krajobraz, w którym najlepsze kandydatury znajdują się w lewym dolnym rogu — silne wobec drobnoustrojów i łagodne dla komórek ludzkich. Zastosowanie CALMA do 35 klinicznie istotnych leków pozwoliło wyselekcjonować z prawie 600 możliwych par niewielki zestaw obiecujących opcji, zmniejszając przestrzeń eksperymentalnych poszukiwań o około 97 procent. Wśród najlepszych sugestii znalazły się kombinacje z udziałem powszechnych antybiotyków takich jak azytromycyna, wankomycyna, izoniazyd i trimetoprim.
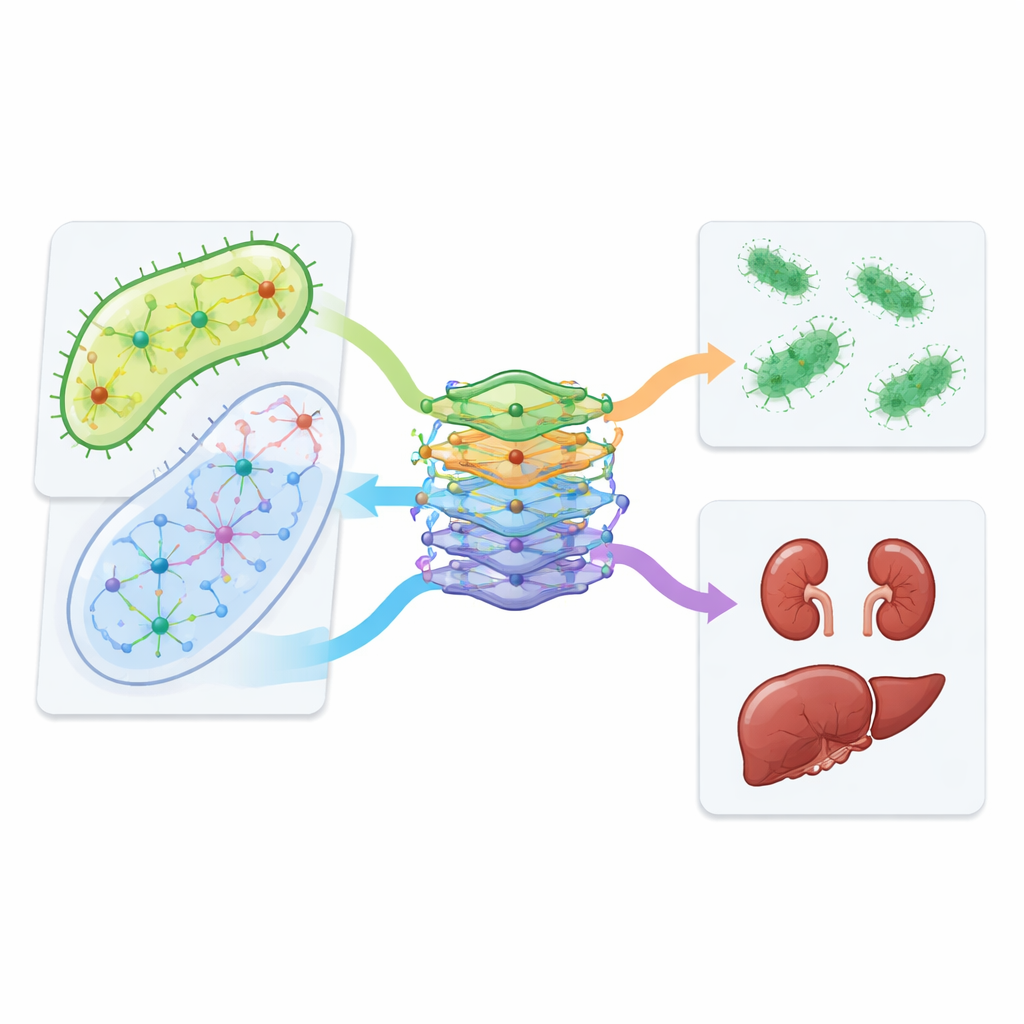
Od przewidywań komputerowych do testów laboratoryjnych i pacjentów
Zespół przeszedł od symulacji do testów kilku przewidywanych kombinacji na liniach komórkowych nerek i wątroby. Stwierdzili, że niektóre pary, w tym azytromycyna z wankomycyną oraz izoniazyd z trimetoprimem, były mniej toksyczne dla komórek ludzkich niż poszczególne leki stosowane osobno, przy jednoczesnym zachowaniu aktywności wobec E. coli. Projekt CALMA pozwolił także badaczom zbadać, które drogi metaboliczne napędzają toksyczność. Jako istotny czynnik wyłonił się szlak recyklingu budulców DNA, znany jako odzysk nukleotydów (nucleotide salvage): jego modyfikacja w eksperymentach komórkowych zmieniała, jak szkodliwe były niektóre kombinacje. Na koniec autorzy przeanalizowali rekordy zdrowotne setek tysięcy pacjentów i zaobserwowali, że osoby otrzymujące azytromycynę razem z wankomycyną miały mniej odnotowanych problemów z nerkami niż podobni pacjenci leczeni samą wankomycyną, co potwierdza wyniki laboratoryjne.
Co to oznacza dla przyszłych terapii
Dla osoby nienależącej do specjalistów CALMA można uznać za inteligentny filtr, który rozumie wystarczająco biologii, by zasugerować, które mieszanki leków warto przetestować w pierwszej kolejności. Zamiast bezrefleksyjnie łączyć antybiotyki i liczyć na najlepsze, badacze mogą skupić się na kombinacjach, które modele przewidują jako trafiające w słabe punkty bakterii przy jednoczesnym oszczędzaniu wrażliwych szlaków ludzkich. Choć metoda zależy od dostępnych danych i nie jest doskonała, oferuje bardziej racjonalną ścieżkę projektowania terapii skojarzonych. Z upływem czasu narzędzia takie jak CALMA mogą pomóc lekarzom bezpieczniej leczyć zakażenia oporne, ograniczyć metodę prób i błędów w opracowywaniu leków, a nawet zostać zaadaptowane do innych chorób, gdzie kombinacje terapii i działania niepożądane są poważnym problemem.
Cytowanie: Arora, H.S., Lev, K., Robida, A. et al. A Metabolism-Informed Neural Network Identifies Pathways Influencing the Potency and Toxicity of Antimicrobial Combinations. npj Drug Discov. 3, 11 (2026). https://doi.org/10.1038/s44386-026-00042-9
Słowa kluczowe: kombinacje antybiotyków, toksyczność leków, sztuczne sieci neuronowe, metabolizm, oporność na środki przeciwmikrobiowe