Clear Sky Science · pl
Generowanie 3D cząsteczek z ograniczeniami oddziaływań przy użyciu modelu dyfuzji umożliwia modelowanie farmakoforów oparte na strukturze dla projektowania leków
Dlaczego projektowanie lepszych leków jest takie trudne
Współczesne odkrywanie leków często polega na przekonaniu małej cząsteczki, by pasowała do białka jak klucz do zamka. Ale klucz musi robić więcej niż tylko pasować: musi tworzyć odpowiedni zestaw drobnych przyciągań — takich jak słabe siły elektrostatyczne i obszary unikające wody — aby lek pozostawał związany mocno i specyficznie. Wszechświat chemiczny jest astronomicznie rozległy, daleko poza zasobami dzisiejszych baz danych, więc badacze szukają inteligentniejszych sposobów tworzenia nowych kluczy od podstaw przy zachowaniu tych kluczowych wzorców kontaktów.
Nauczanie komputera, co naprawdę ma znaczenie
W pracy przedstawiono DiffPharma, obliczeniowe ramy generujące trójwymiarowe, podobne do leków cząsteczki bezpośrednio we wnęce wiążącej białka. Zamiast każdorazowo przeszukiwać ogromne katalogi istniejących związków, DiffPharma tworzy nowe atom po atomie, kierując się tym, jak powinny one oddziaływać z białkiem. Metoda oparta jest na nowoczesnej klasie modeli generatywnych zwanych modelami dyfuzji, które zaczynają od losowego szumu i stopniowo „odszumiają” go do postaci uporządkowanego obiektu — w tym przypadku trójwymiarowej cząsteczki umieszczonej w kieszeni białka.
Kodowanie uścisku dłoni białka
Aby powiedzieć modelowi, co jest istotne na powierzchni białka, autorzy reprezentują kluczowe kontakty jako małe „cząstki interakcyjne” rozproszone wzdłuż ścieżek między białkiem a cząsteczką referencyjną. Podkreślono dwa powszechne typy interakcji: wiązania wodorowe, które działają jak kierunkowe magnesy między konkretnymi atomami, oraz kontakty hydrofobowe, gdzie oleiste rejony gromadzą się razem, unikając wody. Oddzielne sieci neuronowe uczą się geometrii i chemii każdego typu interakcji, a także ogólnego kształtu wnęki wiążącej; specjalna architektura fuzji łączy te perspektywy w jedną, spójną reprezentację, która kieruje generowaniem cząsteczek.
Jak wiernie naśladuje rzeczywiste wzorce wiązania?
Zespół przetestował DiffPharma na 100 parach białko–cząsteczka i sprawdził, jak wiernie nowe cząsteczki odtwarzają oryginalne wzorce kontaktów, reszta po reszcie. Mierzono to przy pomocy miary podobieństwa cosinusowego w skali od 0 do 1, gdzie 1 oznacza perfekcyjne dopasowanie. Rozkład wyników DiffPharma osiągał szczyt około 0,9, co oznacza, że średnio te same reszty białkowe tworzyły te same typy kluczowych interakcji co w strukturach referencyjnych — znacznie lepiej niż sześć konkuruących metod. Co istotne, model dokonywał tego, wciąż generując różnorodne kształty molekularne, a powstałe związki zachowywały realistyczne długości wiązań, kąty i ogólną geometrię 3D typową dla rzeczywistych, stabilnych cząsteczek.
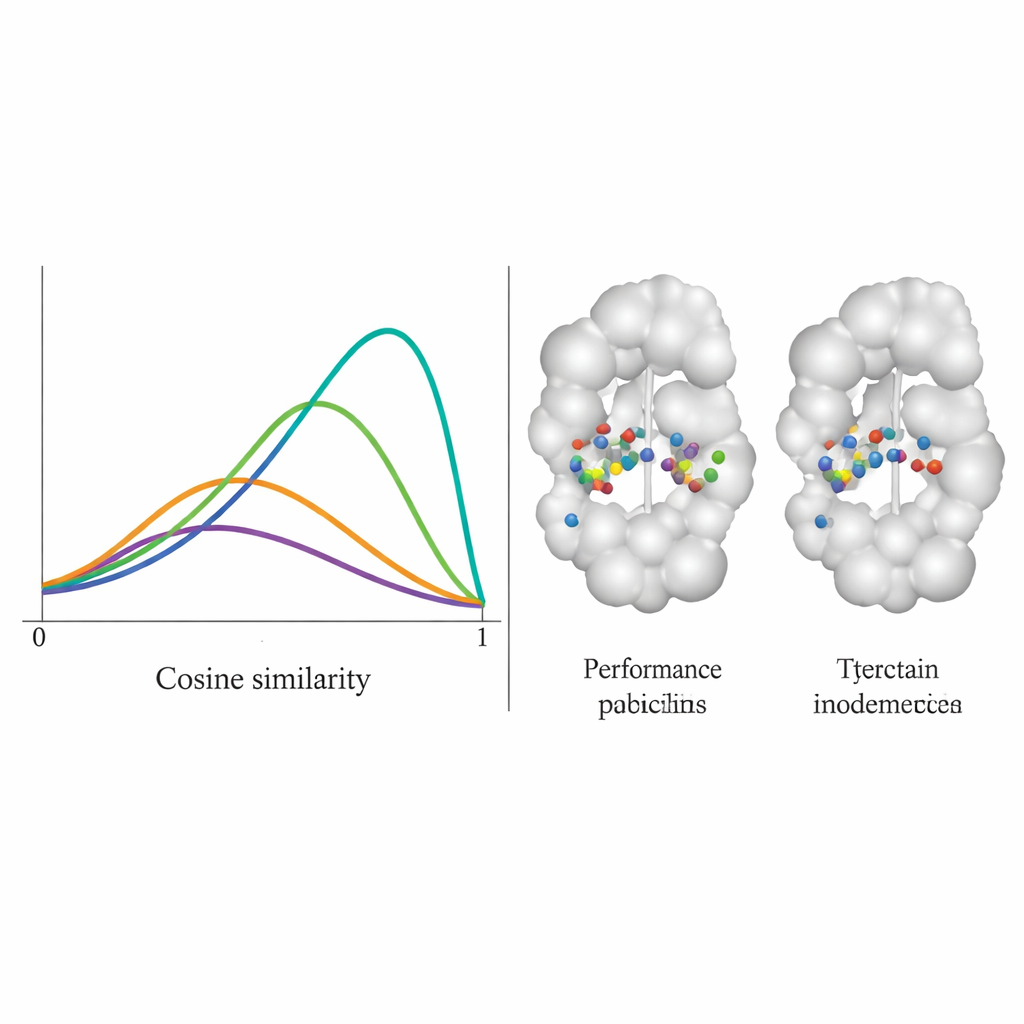
Od teorii do praktycznych kandydatów na leki
Ponad benchmarkami, autorzy zapytali, czy DiffPharma potrafi zaprojektować prawdopodobnych kandydatów na leki dla rzeczywistych celów. Dla dwóch dobrze zbadanych enzymów — kinazy AKT i β-laktamazy powiązanej z opornością na antybiotyki — metoda wygenerowała cząsteczki, które zachowały istotne wzorce interakcji znanych ligandów, często wykorzystując jednak inne szkielety chemiczne, co jest pożądanym efektem „skaffold hopingu” w chemii medycznej. W bardziej wymagającym studium przypadku dotyczącym głównego proteazu SARS‑CoV‑2, DiffPharma był kierowany za pomocą konkretnych wyborów interakcji, a następnie badany przy pomocy symulacji dynamiki molekularnej i szacunków energii wiązania. Cząsteczki generowane przy ścisłych ograniczeniach interakcji tworzyły bardziej stabilne kompleksy i czasem wykazywały korzystniejsze przewidywane energie wiązania niż znany inhibitor referencyjny. Co godne uwagi, system nawet na nowo odkrył ten związek referencyjny — mimo że nigdy nie pojawił się w treningu — wyłącznie na podstawie struktury białka i instrukcji dotyczących interakcji.
Co to oznacza dla przyszłych leków
Dla osoby niebędącej specjalistą DiffPharma można uznać za inteligentne narzędzie projektowe z uwzględnieniem 3D dla cząsteczek lekowych: znając kształt wnęki białkowej i pożądany wzorzec „uścisków dłoni”, proponuje chemicznie sensowne klucze, które pasują i oddziałują we właściwy sposób. Chociaż nie optymalizuje jeszcze wszystkich właściwości, których wymaga lek, takich jak rozpuszczalność czy metabolizm, metoda niezawodnie zachowuje kluczową mapę kontaktów na powierzchni białka i eksploruje nowe obszary przestrzeni chemicznej poza obecnymi katalogami. Takie podejście sterowane interakcjami może pomóc badaczom szybciej przejść od danych strukturalnych białek związanych z chorobami do różnorodnych, realistycznych punktów wyjścia do eksperymentalnego rozwoju leków.
Cytowanie: Sako, M., Yasuo, N. & Sekijima, M. Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design. npj Drug Discov. 3, 8 (2026). https://doi.org/10.1038/s44386-026-00040-x
Słowa kluczowe: projektowanie leków oparte na strukturze, generatywne modele molekularne, modelowanie farmakoforów, interakcje białko–ligand, główny proteaz SARS-CoV-2