Clear Sky Science · pl
Preferencyjna stymulacja HER4 zachowuje poprawę funkcji mięśnia sercowego wywołaną neureguliną
Nowa nadzieja dla serc w niewydolności
Niewydolność serca dotyka miliony ludzi na całym świecie i często pogarsza się pomimo stosowania najlepszych obecnie dostępnych leków. To badanie analizuje nowy rodzaj leku biologicznego, nazwanego JK07, zaprojektowanego tak, by pomagać sercu w naprawie, jednocześnie unikając poważnego ryzyka: potencjalnego pobudzania utajonych nowotworów. Poprzez precyzyjne modulowanie naturalnego sygnału naprawczego w sercu i odciąganie go od ścieżek powiązanych z rakiem, badacze dążą do uzyskania korzyści bez szkody.
Jak działa własny sygnał naprawczy serca
Praca koncentruje się na neuregulinie‑1 (NRG‑1), białku produkowanym w organizmie, które wspiera wzrost, przeżycie i regenerację komórek mięśnia sercowego. NRG‑1 przekazuje instrukcje przez miejsca docelowe na komórkach zwane HER3 i HER4. Gdy NRG‑1 wiąże się z tymi receptorami, łączą się one z partnerem o nazwie HER2 i uruchamiają wewnątrzkomórkowe sygnały odpowiedzialne za przeżycie i naprawę. Wcześniejsze badania na zwierzętach i ludziach z użyciem laboratoryjnie wytworzonej NRG‑1 wykazały istotne poprawy siły wyrzutu serca, lecz wiązały się też z działaniami niepożądanymi, takimi jak zaburzenia żołądkowo‑jelitowe i problemy z wątrobą. Co gorsza, wiadomo, że HER3 napędza wzrost wielu nowotworów, co budzi obawy, że długotrwałe leczenie NRG‑1 mogłoby uaktywnić utajone guzy.
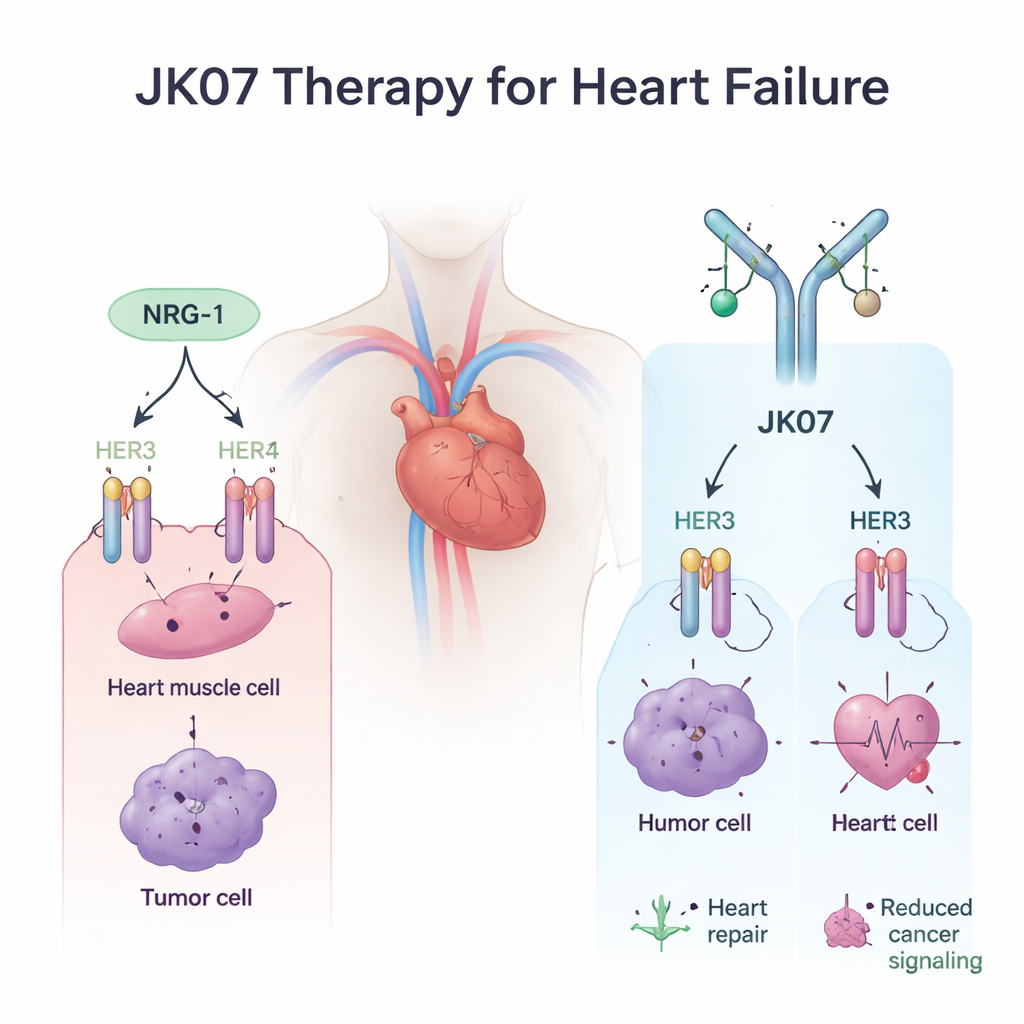
Projektowana cząsteczka z blokadą bezpieczeństwa
Aby rozwiązać ten problem, naukowcy zaprojektowali JK07, cząsteczkę fuzyjną złożoną z dwóch starannie dobranych części. Jeden koniec to w pełni ludzka przeciwciało zaprojektowane do blokowania HER3, receptora powiązanego z rakiem. Drugi koniec to aktywna część NRG‑1 wywołująca korzystne sygnały, przyłączona w podwójnej kopii, aby mogła nadal docierać do komórek serca. W eksperymentach in vitro JK07 mocno wiązał HER3 i jednocześnie utrzymywał fragment NRG‑1 w odpowiedniej strukturze i aktywnym stanie. W układach komórkowych nowotworów zależnych od HER3 JK07 wyraźnie tłumił sygnały zależne od HER3, spowalniał wzrost komórek w porównaniu z nieskorygowaną NRG‑1, a u myszy z guzami napędzanymi przez HER3 zmniejszał wielkość guzów w zależności od dawki. Wyniki te dowodzą, że część przeciwciałowa rzeczywiście działa jako blokada bezpieczeństwa na HER3.
Utrzymanie sercowego sygnału naprawczego
Kluczowe było jednak to, aby JK07 zachował korzyści wynikające z aktywacji HER4 — receptora powiązanego przede wszystkim z naprawą serca, a nie z rakiem. Z użyciem wyspecjalizowanych linii komórkowych i kardiomiocytów wyhodowanych z ludzkich komórek macierzystych zespół wykazał, że JK07 indukował parowanie HER4 z HER2 i uruchamiał kluczową wewnątrzkomórkową ścieżkę ochronną, znaną jako AKT, równie silnie jak niezmodyfikowana NRG‑1. Komórki serca szczura reagowały podobnie. Innymi słowy, JK07 nie osłabiał sygnału ratunkowego serca; jedynie przekierowywał go z HER3 na HER4.
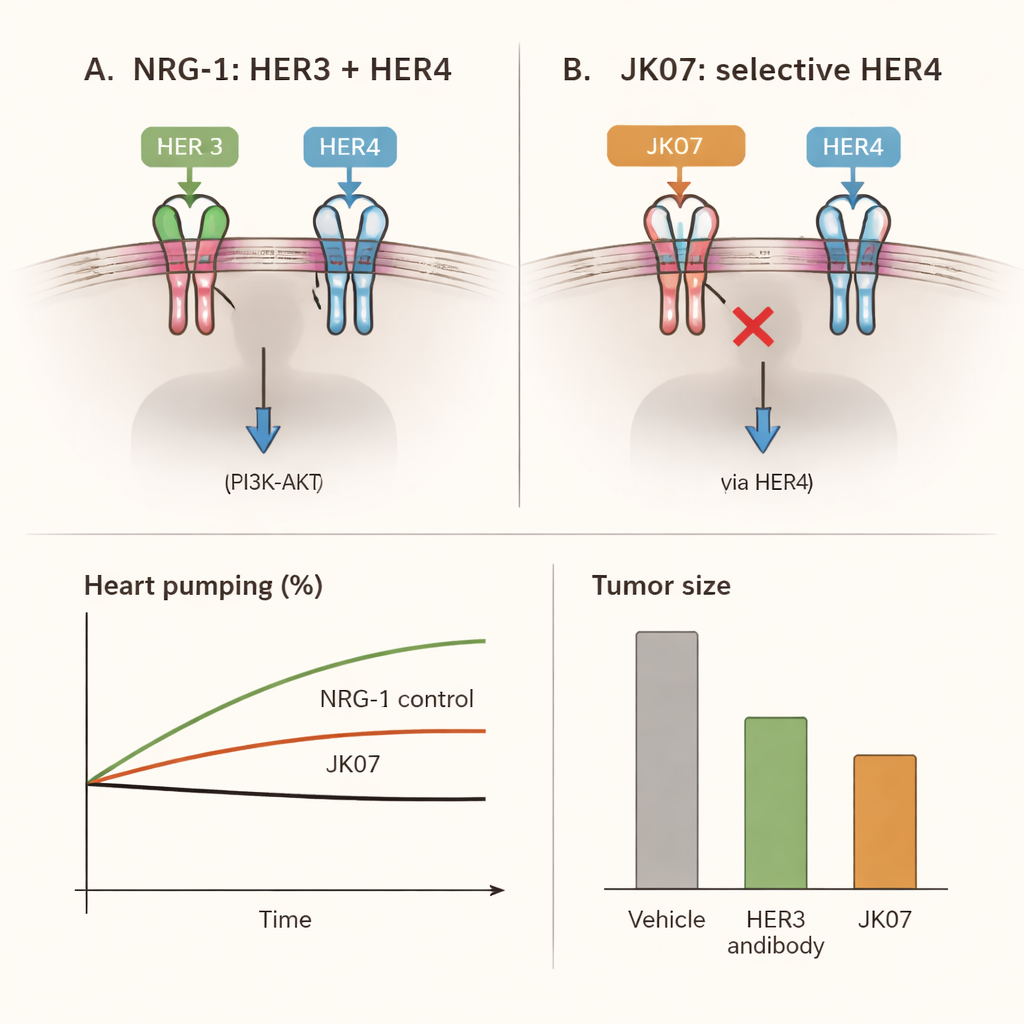
Od gryzoni do małp: wpływ JK07 na serce
Następnie badacze sprawdzili, czy ten selektywny sygnał rzeczywiście może uratować serca w niewydolności. U szczurów, którym wywołano zawał serca chirurgicznie, zdolność wyrzutu serca spadła o około jedną trzecią, co dobrze odzwierciedla ludzką niewydolność. Zwierzęta leczone JK07 wielokrotnie przez cztery tygodnie wykazały wyraźną poprawę: frakcja wyrzutu, standardowy wskaźnik objętości krwi wyrzucanej przy każdym skurczu, wzrosła maksymalnie o około jedną trzecią w porównaniu ze stanem przed leczeniem. Powiększone komory serca zmniejszyły się w kierunku normalnych rozmiarów, włóknienie związane z bliznami w uszkodzonych obszarach zmalało, a mikroskopowa struktura mięśnia sercowego wyglądała bardziej uporządkowanie i zdrowo. Te poprawy odpowiadały efektom zaobserwowanym przy kontrolnym leku opartym na NRG‑1, który nie blokuje HER3, co wskazuje, że sama aktywacja HER4 wystarcza do zapewnienia korzyści kardiologicznych.
Bliżej kliniki: wyniki u małp z niewydolnością
Aby przetestować JK07 w modelu zwierzęcym bardziej zbliżonym do ludzkiej choroby, zespół badał makaki rezus w średnim wieku, które naturalnie rozwinęły długotrwałą niewydolność serca, obejmującą zarówno typ z obniżoną frakcją wyrzutu (HFrEF), jak i typ z zaburzeniami rozkurczowymi (HFpEF). U małp z osłabioną funkcją wyrzutową dwa niezależne badania wykazały, że cotygodniowe wlewy JK07 spowodowały, iż większość zwierząt zyskała co najmniej pięć punktów procentowych frakcji wyrzutu, a niektóre osiągnęły nawet około 20‑punktowe wzrosty bezwzględne — porównywalne z efektami obserwowanymi u zwierząt leczonych znanym lekiem sacubitril/valsartanem. U małp, których głównym problemem były zaburzenia napełniania i rozluźniania serca, JK07 poprawiał stopień dysfunkcji rozkurczowej u większości zwierząt, podczas gdy sacubitril/valsartan pomagał rzadziej. W badanych dawkach nie zaobserwowano istotnych problemów z bezpieczeństwem.
Co to może znaczyć dla pacjentów
Dla osób niezwiązanych ze specjalistyczną medycyną kluczową informacją jest to, że badanie pokazuje możliwość wykorzystania własnego systemu naprawczego serca w bardziej ukierunkowany i bezpieczny sposób. JK07 jest zbudowany tak, by stymulować „dobry” receptor (HER4), wspierający gojenie serca, jednocześnie blokując „ryzykowny” receptor (HER3) związany z rakiem. Zarówno u gryzoni, jak i u małp, to selektywne podejście poprawiało wyrzut serca, zmniejszało uszkodzenia strukturalne i blizny, a w modelu nowotworowym wykazało też aktywność przeciwnowotworową. Chociaż potrzebne są jeszcze badania u ludzi, by potwierdzić korzyści i długoterminowe bezpieczeństwo, JK07 wskazuje na przyszłość, w której leczenie niewydolności serca będzie nie tylko skuteczniejsze, lecz także wiązało się z mniejszym ryzykiem pobudzania nowotworów.
Cytowanie: Murphy, S.L., Tang, W.H.W., Zhuang, X. et al. Preferential HER4 stimulation preserves neuregulin-induced improvement of myocardial function. npj Drug Discov. 3, 10 (2026). https://doi.org/10.1038/s44386-026-00038-5
Słowa kluczowe: niewydolność serca, neuregulina-1, HER4, terapia biologiczna, przebudowa serca