Clear Sky Science · pl
Opracowanie protokołu przeciwdziałającego spontanicznej in vitro aktywacji fibroblastów jelitowych przy użyciu projektowania eksperymentu
Dlaczego ważne jest utrzymanie komórek naprawczych jelita w spokoju
W przewlekłych chorobach jelit, takich jak choroba Leśniowskiego-Crohna, bliznowacenie może stopniowo zwężać światło jelita do tego stopnia, że pokarm ledwo przechodzi, co często kończy się zabiegiem operacyjnym. To bliznowacenie, zwane włóknieniem, jest napędzane przez komórki podporowe znane jako fibroblasty, które stają się nadmiernie aktywne i odkładają zbyt dużo tkanki łącznej. Aby zrozumieć i pewnego dnia zapobiec temu procesowi, naukowcy polegają na hodowlach fibroblastów w laboratorium. Jest jednak problem: zwykłe plastikowe naczynia stosowane w większości laboratoriów same w sobie pobudzają te komórki do nienaturalnej aktywacji, co utrudnia badanie najwcześniejszych zmian prowadzących ze stanu zdrowia do włóknienia jelita.
Kiedy płytka laboratoryjna wysyła fałszywy sygnał
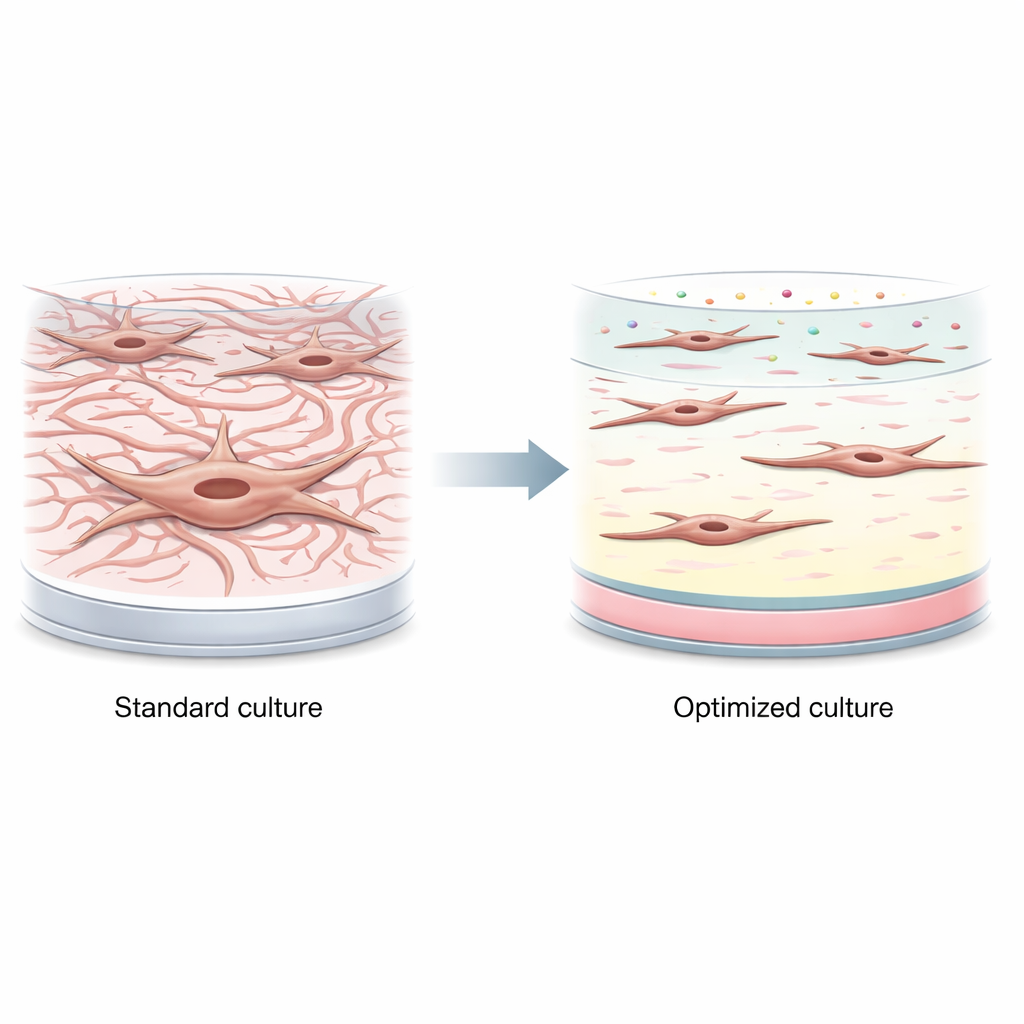
Autorzy najpierw pokazali, jak szybko fibroblasty jelitowe ulegają pobudzeniu na standardowym plastiku do hodowli tkanek. Już w ciągu 24 godzin zarówno ustalona linia komórkowa, jak i komórki pierwotne od dawców płci męskiej i żeńskiej przeszły ze stanu spokojnego do aktywowanego, mięśnio-podobnego kształtu. Wytwarzały wysokie poziomy białek związanych ze skurczem i bliznowaceniem, takich jak α-aktyna mięśni gładkich i białko aktywacji fibroblastów, nawet bez dodania czynników zapalnych. Oznacza to, że wiele istniejących modeli laboratoryjnych może rozpoczynać badania od stanu, który już przypomina zaawansowaną chorobę, a nie wczesne, odwracalne zmiany.
Testowanie pojedynczych składników to za mało
Aby uspokoić komórki, zespół badał składniki naturalnego otoczenia fibroblastów w jelicie, w tym kluczowe białka rusztowania (kolagen typu I i III oraz lamininę) oraz czynniki rozpuszczalne (witaminę D i podstawowy czynnik wzrostu fibroblastów, FGF). Próbowali ich pojedynczo, jako powłoki powierzchniowe lub dodatki do pożywki hodowlanej. Niektóre warunki obniżały markery aktywacji: na przykład umiarkowane dawki witaminy D obniżały główny marker bliznowacenia wielokrotnie, a pewne gęstości powłok miały łagodne efekty. Jednak korzyści te były równoważone przez problemy, takie jak zmniejszona przeżywalność komórek przy wyższych stężeniach witaminy D, i ogólnie pojedyncze poprawki nie utrzymywały fibroblastów w stanie niskiej aktywności w sposób niezawodny.
Pozwolenie statystyce na przeszukanie przestrzeni możliwości
Zamiast regulować jeden parametr naraz, badacze zastosowali formalne podejście „projektowania eksperymentu”, aby efektywnie przeszukać wiele kombinacji. Zmieniali pięć wejść — trzy białka macierzy oraz witaminę D i FGF — w szerokim zakresie dawek, generując 42 starannie dobrane warunki hodowli. Dla każdego z nich mierzono cztery wyniki związane z bliznowaceniem: kluczowy marker aktywacji, wydzielanie głównego białka macierzy (fibronektyny), wzrost komórek i przeżywalność. Modele statystyczne ujawniły, które czynniki i które parowania między nimi miały największy wpływ. Witamina D okazała się silnym, lecz wrażliwym na dawkę graczem, wpływającym na wszystkie odczyty, podczas gdy FGF zwykle obniżał aktywację i wspierał wzrost oraz przeżywalność komórek. Kolagen I, kolagen III i laminina kształtowały sposób, w jaki te sygnały rozpuszczalne były interpretowane, przy czym pewne kombinacje tłumiły aktywację znacznie bardziej niż jakikolwiek pojedynczy czynnik.
Budowanie przepisu na spokojne, ale zdrowe fibroblasty
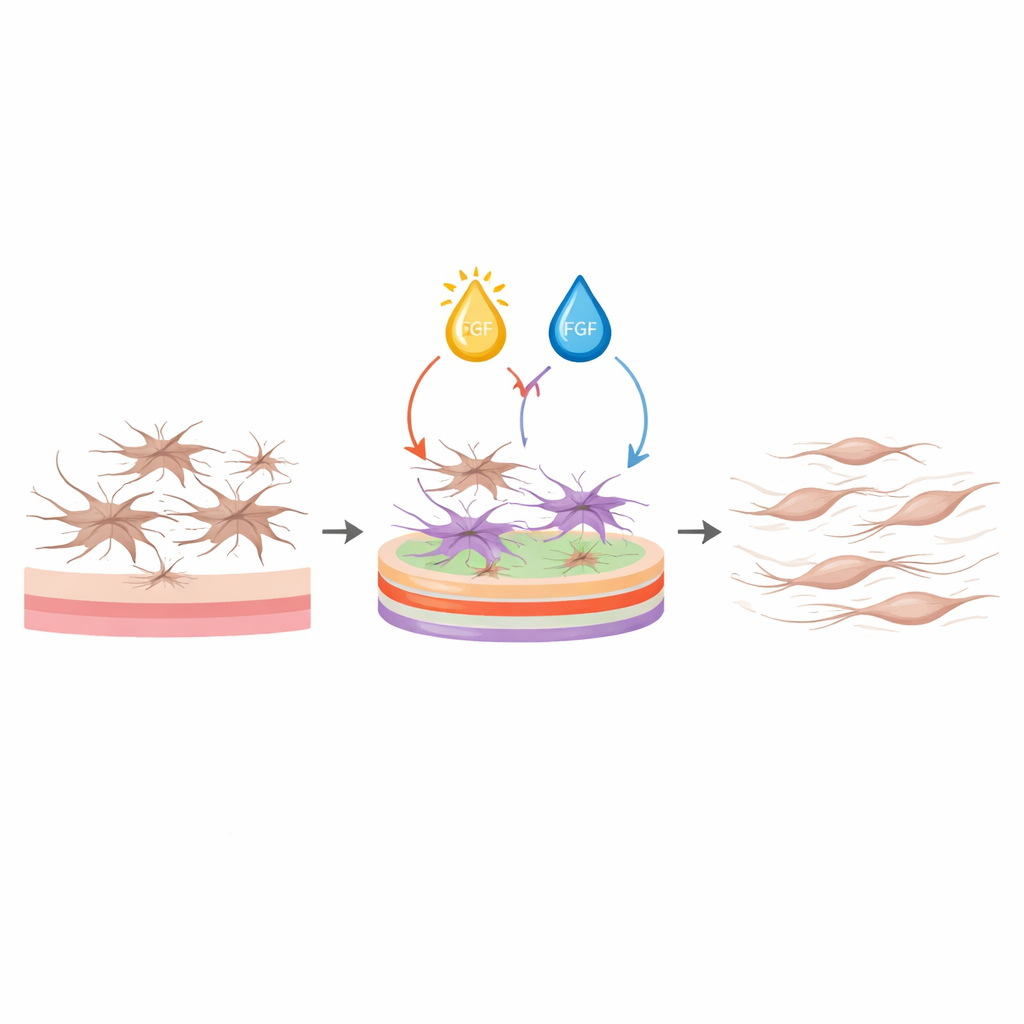
Wykorzystując te modele, zespół poprosił oprogramowanie o identyfikację warunków, które jednocześnie obniżą markery aktywacji i produkcję macierzy przy jednoczesnym utrzymaniu przeżywalności komórek, bez wymogu niskiej proliferacji. Najlepszy przepis łączył wysoką gęstość kolagenu I, niską zawartość kolagenu III oraz wysoką lamininę na powierzchni hodowli, razem z umiarkowanym stężeniem witaminy D i wysokim FGF w pożywce. W ramach tego protokołu fibroblasty pozostawały smukłe i wrzecionowate zamiast rozpostartych i gwiaździstych, wykazywały znacznie niższe poziomy genów i białek powiązanych ze skurczem i włóknieniem oraz wydzielały znacznie mniej kolagenu i fibronektyny. Jednocześnie ich żywotność pozostała tak wysoka lub lepsza niż komórek na zwykłym plastiku. Co ważne, efekty te utrzymywały się nie tylko dla modelowej linii komórkowej, lecz także dla fibroblastów pierwotnych pochodzących od dawców ludzkich obu płci, pokazując, że protokół jest odporny.
Co to oznacza dla przyszłych badań nad włóknieniem jelit
Poprzez staranne dostrojenie „sąsiedztwa” wokół fibroblastów jelitowych — zarówno powierzchni, do której się przyczepiają, jak i czynników je kąpiących — to badanie dostarcza prosty protokół utrzymujący te komórki w stanie nieaktywowanym, ale zdrowym, przy użyciu standardowych materiałów laboratoryjnych. Dla badaczy daje to czysty punkt wyjścia do dodawania konkretnych sygnałów zapalnych lub mechanicznych i obserwowania, jak zaczyna się włóknienie, zamiast pracy z komórkami, które już przypominają tkankę bliznowatą. Szerzej rzecz biorąc, praca pokazuje, jak statystyczne projektowanie może odkrywać subtelne, nieintuicyjne kombinacje składników łagodzące złożone zachowania komórek, torując drogę do lepszych modeli bliznowacenia, a w końcu do bardziej celowanych strategii zapobiegania lub odwracania włóknienia jelit.
Cytowanie: Mohammadalizadeh, Z., Sudi, S., Basto Moreno, D.A. et al. Developing a protocol to counteract spontaneous in vitro activation of intestinal fibroblasts using design of experiments. npj Biomed. Innov. 3, 25 (2026). https://doi.org/10.1038/s44385-026-00079-5
Słowa kluczowe: zwłóknienie jelit, aktywacja fibroblastów, protokół hodowli komórek, witamina D i FGF, projektowanie eksperymentu