Clear Sky Science · pl
Wnioskowanie o nieprawidłowościach szlaków sygnalizacyjnych na podstawie obrazów histopatologicznych za pomocą heterogenicznego grafu wiedzy gen‑szlak ograniczonego logiką
Widzenie ukrytych sygnałów komórkowych na preparatach nowotworowych
Kiedy lekarze oglądają nowotwór pod mikroskopem, najczęściej widzą kształty i kolory, a nie złożone molekularne „rozmowy” zachodzące w komórkach. Tymczasem niewidoczne sygnały między genami i szlakami często decydują o tym, jak guz rośnie i jak zareaguje na leczenie. W tym badaniu przedstawiono nowy system sztucznej inteligencji, który analizuje rutynowe obrazy patologiczne i wnioskuje, które drogi komunikacji komórkowej, czyli szlaki, funkcjonują nieprawidłowo — oferując możliwość zajrzenia w zachowanie molekularne bez dodatkowych badań laboratoryjnych.
Od wskazówek o pojedynczych genach do szerszego obrazu
Tradycyjne podejścia próbują przewidzieć status pojedynczych genów na podstawie obrazów tkanek: czy dany gen jest zmutowany, czy nie? To jest przydatne, ale nowotwór rzadko zależy od jednego wadliwego genu. Zamiast tego grupy genów współdziałają, zaburzając całe szlaki sygnalizacyjne kontrolujące wzrost, przeżycie i odporność. Autorzy argumentują, że skupianie się na pojedynczych genach pomija to współdziałanie i może nie wyjaśniać, dlaczego guzy wyglądają i zachowują się tak, a nie inaczej pod mikroskopem.
Budowanie mapy łączącej obrazy, geny i szlaki
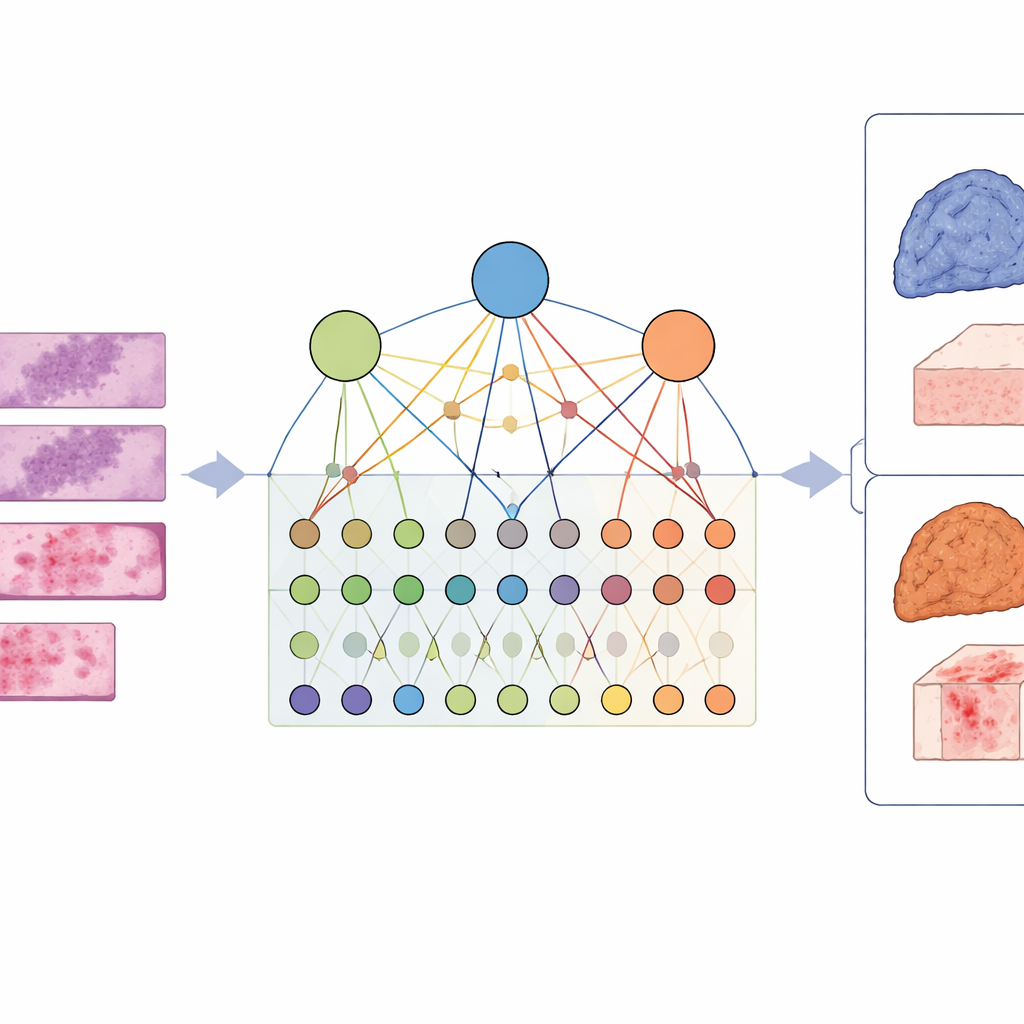
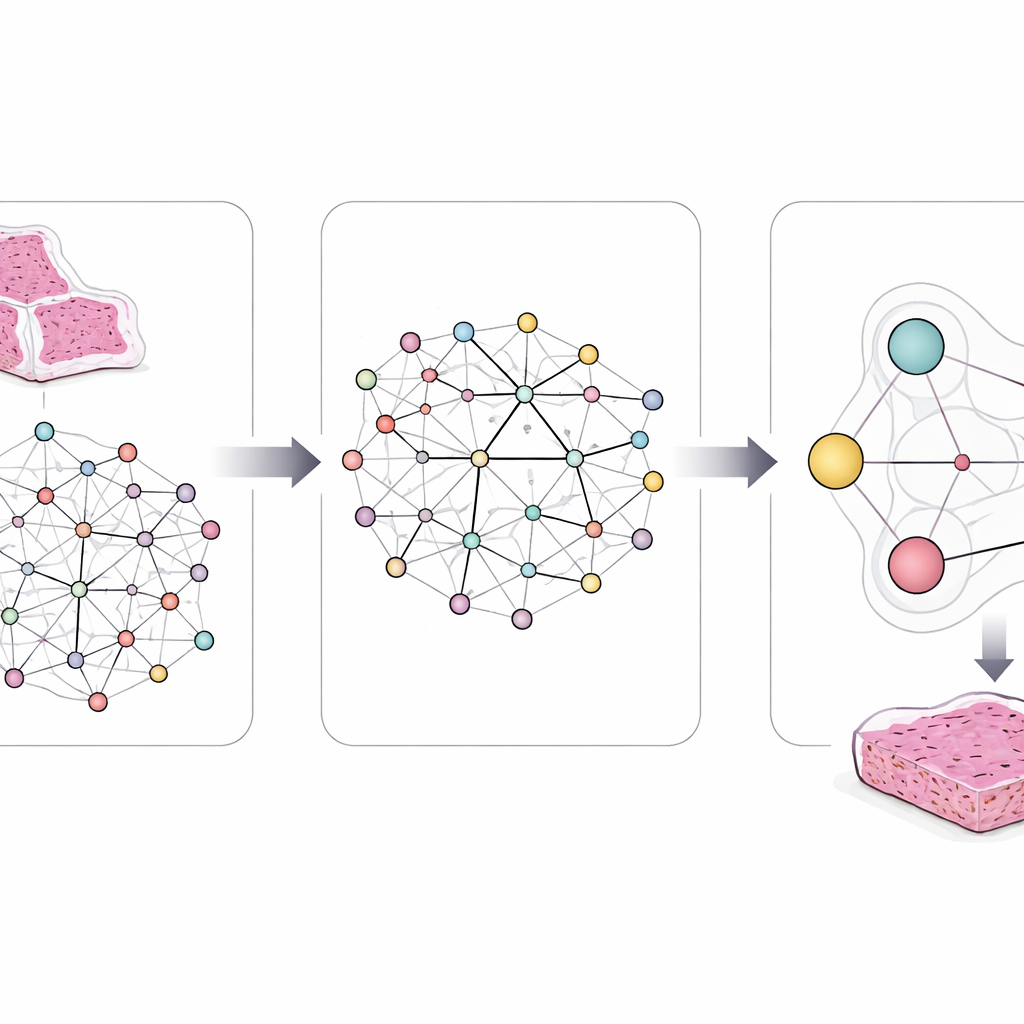
Aby uchwycić tę złożoność, badacze zaprojektowali ramę nazwaną LCG-HGNN, która łączy trzy warstwy informacji. Po pierwsze, dzielą każde całoskanowe zdjęcie gruczolakoraka płuca na wiele małych fragmentów i przedstawiają te fragmenty jako graf, gdzie sąsiednie lub podobne wizualnie regiony są połączone. Po drugie, łączą markery genowe z szlakami sygnalizacyjnymi przy użyciu utworzonych baz biologicznych, budując drugi graf kodujący przynależność genów do konkretnych szlaków. Wreszcie pozwalają modelowi AI przekazywać informacje przez połączony graf, tak aby wzorce obrazu, geny i szlaki oddziaływały na siebie zamiast być traktowane izolowanie.
Nauczanie systemu znanej biologii
Kluczową innowacją jest to, że model nie uczy się dowolnie bez wskazówek. Autorzy osadzili jasne, przypominające reguły stwierdzenia wyprowadzone z dekad badań nad nowotworami. Na przykład niektóre mutacje niemal nigdy nie występują razem w tym samym guzie, a niektóre szlaki leżą upstream lub downstream względem innych. Kodują takie reguły jako ograniczenia logiczne, które delikatnie kierują wewnętrznymi połączeniami i predykcjami AI. Jeśli model proponuje kombinację zmian genowych i szlakowych, która koliduje ze znaną biologią lub z podobieństwami między preparatami pacjentów, te reguły skłaniają go ku bardziej realistycznym alternatywom.
Testowanie dokładności w porównaniu z istniejącymi metodami
Zespół ocenił swój system na ponad 1 600 preparatach raka płuca powiązanych z danymi genetycznymi. Porównali go ze standardowymi modelami głębokiego uczenia skupiającymi się na pojedynczych genach oraz z bardziej zaawansowanymi metodami obsługującymi wiele genów jednocześnie, ale ignorującymi strukturę szlaków. W szeregu istotnych szlaków, w tym tych związanych z sygnałami wzrostu komórek i podporową strukturą tkanki, nowy model dokładniej przewidywał zmiany grup genowych i nieprawidłowości szlaków. Dodatkowo generował fragmenty obrazu, których wygląd dobrze odpowiadał rzeczywistym klinicznym przykładom związanym z konkretnymi mutacjami, co sugeruje, że skupiał się na sensownych mikroskopowych wzorcach, a nie na przypadkowych artefaktach obrazu.
Dlaczego to ma znaczenie dla pacjentów
Dla laika głównym rezultatem jest to, że takie podejście zamienia rutynowy preparat patologiczny w bogate źródło wglądu molekularnego. Zamiast zlecać oddzielne, często kosztowne testy genetyczne na każdy możliwy cel, lekarze mogliby w przyszłości używać podobnych modeli do przesiewowego wykrywania zaburzonych szlaków bezpośrednio na obrazach, które już zbierają. Metoda wciąż wymaga szerszego, praktycznego potwierdzenia i nie zastępuje jeszcze badań genomowych, ale wskazuje na przyszłość, w której widok przez mikroskop staje się też oknem na wewnętrzne okablowanie guza — pomagając prowadzić bardziej precyzyjną i biologicznie ugruntowaną opiekę onkologiczną.
Cytowanie: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
Słowa kluczowe: szlaki nowotworowe, AI w histopatologii, grafowe sieci neuronowe, gruczolakorak płuca, patologia cyfrowa