Clear Sky Science · pl
Inżynieria makrofagów do immunoterapii nowotworów: nowe wnioski i potencjał terapeutyczny
Przekształcanie komórki porządkowej organizmu w pogromcę raka
Nasz organizm jest pełen makrofagów — krążących „ekipy sprzątającej”, które pochłaniają drobnoustroje i martwe tkanki. Ten przeglądowy artykuł opisuje, jak naukowcy uczą się przekierowywać te komórki przeciwko rakowi. Ponieważ makrofagi występują licznie w obrębie guzów, także tych opornych na najnowsze immunoterapie, ich zrozumienie i inżynieria mogą otworzyć nowe możliwości dla pacjentów z trudno leczonymi nowotworami.
Wiele twarzy jednego typu komórki
Makrofagi nie są jednym, stałym typem komórki; to kameleony. Mogą pochodzić z krwiobiegu lub rezydować już w tkankach i po osiedleniu reagować na lokalne sygnały. W guzach te makrofagi związane z nowotworem mogą albo pomagać zabijać komórki rakowe, albo, co mylące, wspierać wzrost i rozprzestrzenianie się guza. Wcześniej badacze próbowali sprowadzać je do dwóch kategorii — „M1” (tryb ataku) i „M2” (tryb naprawczy lub wspierający). Nowe narzędzia genetyczne i przestrzenne mapowanie ukazują znacznie bogatsze spektrum stanów, z wieloma podgrupami i zachowaniami zależnymi od konkretnego guza i miejsca. Nawet komórki wcześniej uznawane za wyraźnie „pro‑guzowe” mogą w pewnych kontekstach pobudzać limfocyty T i wspierać odporność przeciwnowotworową.
Odczytywanie otoczenia i pożeranie komórek nowotworowych
Makrofagi nie tylko odbierają sygnały chemiczne; wyczuwają też fizyczny świat wokół siebie. Przemieszczając się przez gęstą sieć białek guza, przeciskając między komórkami i doświadczając sił płynów, wyczuwają sztywność i odkształcenia za pomocą specjalnych receptorów, takich jak Piezo1. Te mechaniczne wskazówki, wraz z klasycznymi sygnałami immunologicznymi, mogą przesuwać makrofagi w stronę bardziej zapalnych lub bardziej uspokajających ról. Funkcjonalnie makrofagi potrafią pochłaniać komórki nowotworowe, rozkładać je, a następnie prezentować fragmenty (antygeny) limfocytom T, łącząc odporność wrodzoną z nabyta. Komórki nowotworowe odpierają atak, wysyłając sygnały „nie jedz mnie”, w szczególności przez cząsteczkę powierzchniową CD47, która wiąże hamulec na makrofagach. Leki blokujące tę interakcję są badane w licznych próbach klinicznych, zwiększając usuwanie komórek nowotworowych, ale wymagając starannego dostrojenia, by nie uszkodzić zdrowych komórek.
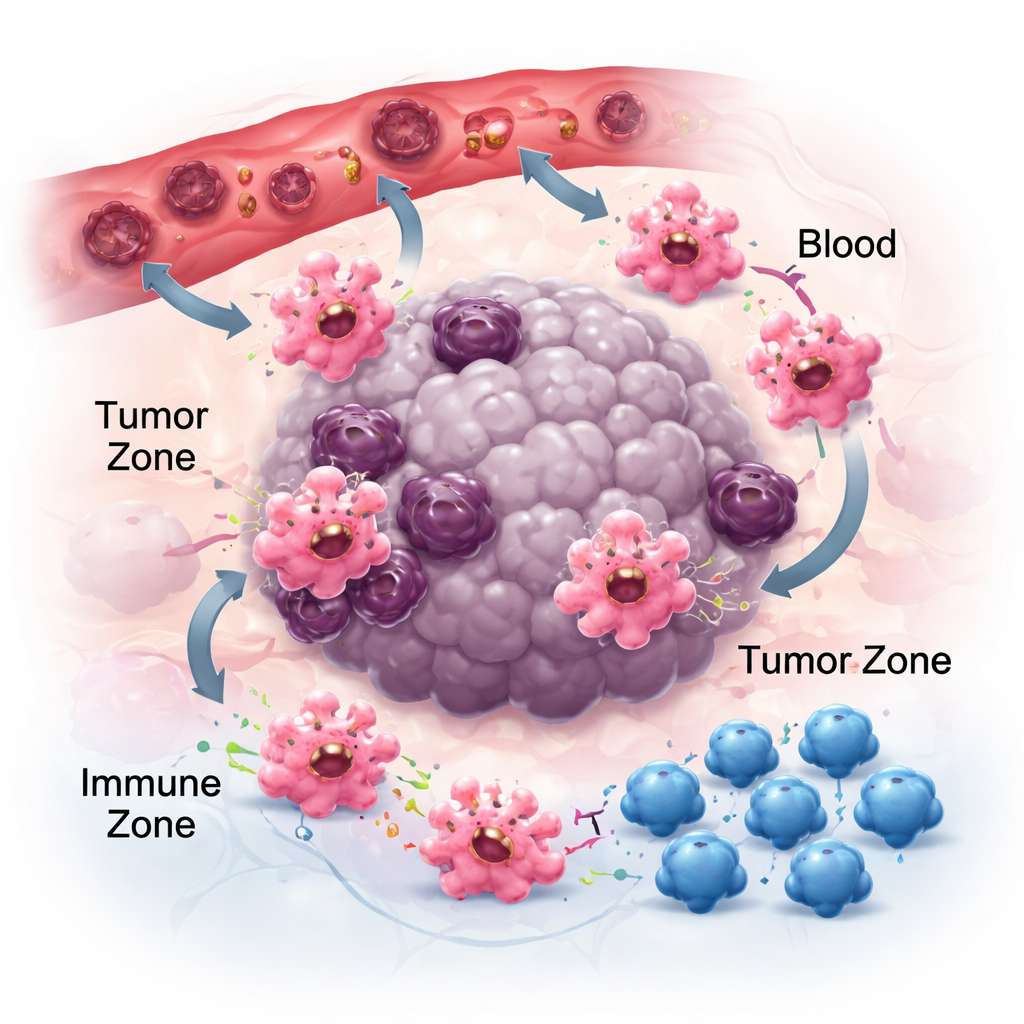
Ruch, przyczepność i komunikacja w sąsiedztwie guza
Aby miały znaczenie w nowotworze, makrofagi muszą najpierw dotrzeć do guzów, a potem ulokować się w odpowiednich niszach. Podążają za chemicznymi śladami — chemokinami i czynnikami wzrostu — uwalnianymi przez komórki nowotworowe i otoczenie. Pary takie jak CCR2–CCL2 przyciągają je do guzów, a leki blokujące te sygnały mogą zmniejszać nagromadzenie makrofagów, choć nie całkowicie, co wskazuje na inne przyciągające czynniki, jak CSF‑1 i VEGF. Po dotarciu to, jak makrofagi przylegają do lokalnej macierzy, także wpływa na ich zachowanie. Ich receptory adhezji, zwane integrynami, nie pełnią tylko funkcji kleju; wzmacniają sygnały zapalne i mogą popychać komórki w kierunku bardziej przeciwnowotworowych stanów. Jednocześnie makrofagi uwalniają maleńkie pakiety zwane pęcherzykami zewnątrzkomórkowymi, które przenoszą RNA i białka do pobliskich komórek. W zależności od typu guza te pęcherzyki mogą tłumić odporność i wspierać rozprzestrzenianie się lub wzmacniać odpowiedzi przeciwko nowotworowi, co podkreśla kontekstową naturę komunikacji makrofagów.
Reprogramowanie makrofagów za pomocą genów i materiałów
Ponieważ makrofagi naturalnie wnikają do guzów litych lepiej niż wiele limfocytów T, badacze przeprojektowują je teraz jako żywe leki. Jedna strategia genetyczna zapożycza podejście z terapii limfocytami T z chimerycznym receptorem antygenowym (CAR): dodanie syntetycznego receptora w celu stworzenia CAR‑makrofagów (CAR‑M). Te zaprojektowane komórki rozpoznają markery guza, efektywniej pochłaniają komórki nowotworowe, trawią otaczającą macierz, uwalniają sygnały zapalne i aktywują limfocyty T poprzez prezentację antygenów guza. Wczesne próby u ludzi z CAR‑M ukierunkowanymi na HER2 wykazują obiecujące bezpieczeństwo i aktywność biologiczną, choć potrzeba więcej pracy, by udowodnić silne i trwałe korzyści. Równolegle podejścia niegenetyczne wykorzystują cząstki i „plecaki” wykonane z lipidów lub polimerów. Makrofagi mogą pochłaniać nanocząstki załadowane lekami i przenosić je głęboko do guzów niczym koniki trojańskie, albo nosić na powierzchni plastry uwalniające powoli sygnały wzmacniające odporność, pomagając im utrzymać przeciwnowotworową tożsamość bez przeładowania wnętrza. Samo pochodzenie z makrofagów pęcherzyki są także testowane jako naturalne, pozakomórkowe nośniki dostarczania.
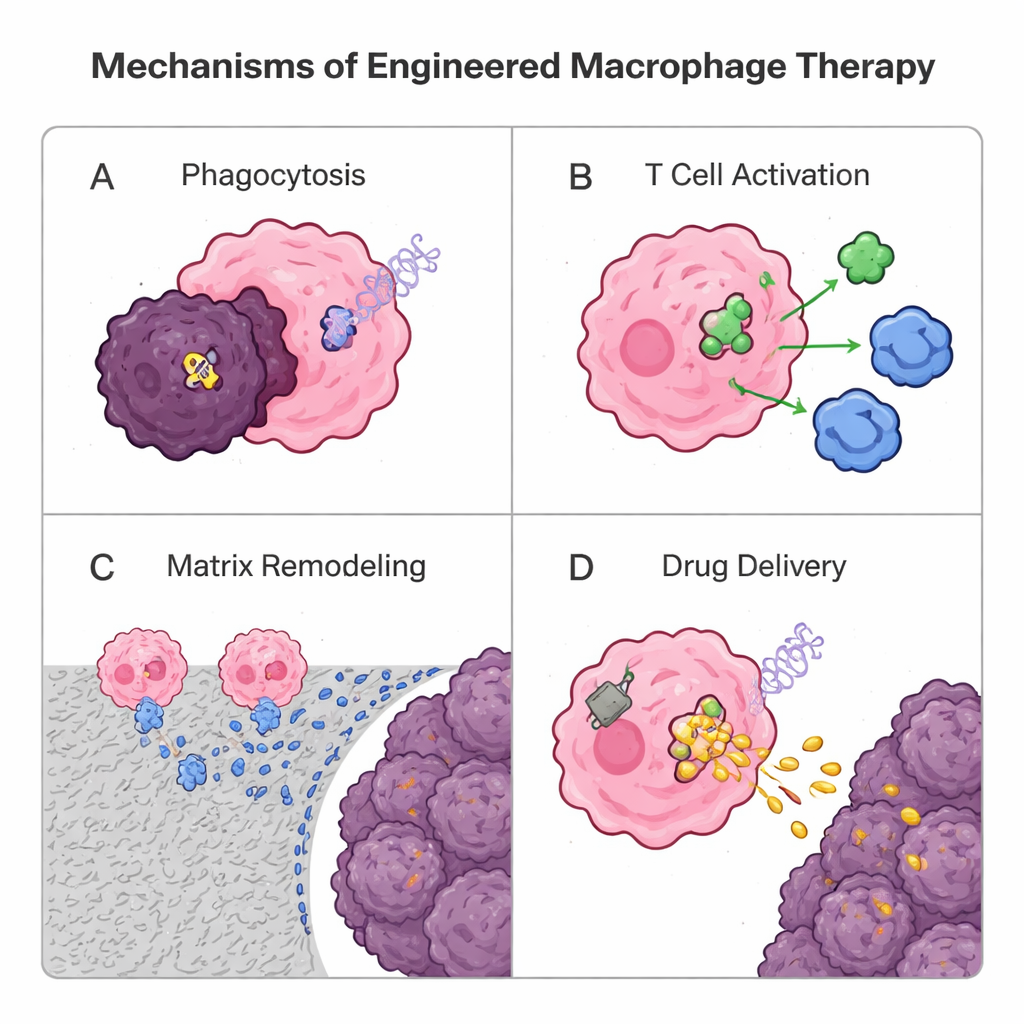
Wyzwania i powody do nadziei
Mimo obiecujących wyników terapie oparte na makrofagach muszą pokonać praktyczne przeszkody. Wytworzenie wystarczającej liczby spójnych komórek od pacjentów jest czasochłonne i kosztowne, a po winfuzji te komórki nie żyją ani nie rozmnażają się w nieskończoność. Ich wrodzona plastyczność, choć biologicznie użyteczna, utrudnia utrzymanie ich w trwałym, przeciwnowotworowym stanie w złożonym, hamującym mikrośrodowisku guza. Autorzy argumentują, że zaawansowane modele bioinżynieryjne — hodowle 3D, organoidy i systemy organ‑on‑a‑chip odwzorowujące mechanikę prawdziwych tkanek — będą kluczowe dla zrozumienia i przewidywania zachowania inżynierowanych makrofagów u pacjentów. Mimo to ich naturalna zdolność do wnikania w guzy litych, pożerania komórek nowotworowych i pobudzania limfocytów T, w połączeniu z wczesnymi dowodami bezpieczeństwa, sugeruje, że terapie oparte na makrofagach mogą stać się ważną nową bronią, zwłaszcza przeciwko „zimnym” guzom, które obecnie opierają się większości immunoterapii.
Cytowanie: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
Słowa kluczowe: immunoterapia makrofagowa, mikrośrodowisko guza, CAR makrofagi, fagocytoza, dostarczanie leków za pomocą nanocząstek