Clear Sky Science · pl
Terapeutyki oparte na kwasach nukleinowych przywracające homeostazę stawu w artrozie związanej z wiekiem i po urazach
Dlaczego bolące stawy potrzebują nowych rodzajów leków
Choroba zwyrodnieniowa stawów, najczęstsza forma zapalenia stawów, często bywa bagatelizowana jako zwykłe „zużycie”, podczas gdy w rzeczywistości to złożona choroba, w której zaburza się naturalna równowaga między uszkodzeniem a naprawą stawu. W miarę jak ludzie żyją dłużej i pozostają aktywni w późniejszym wieku, bolesne, sztywne stawy stają się poważną przyczyną niepełnosprawności, a dostępne terapie na ogół łagodzą objawy lub kończą się kosztowną wymianą stawu. Ten artykuł przeglądowy opisuje nową klasę terapii opartych na instrukcjach genetycznych — drobnych nici RNA — które mają nie tylko uśmierzać ból, lecz przywracać zdrową równowagę w uszkodzonych stawach.
Od zużytej chrząstki do uszkodzenia całego stawu
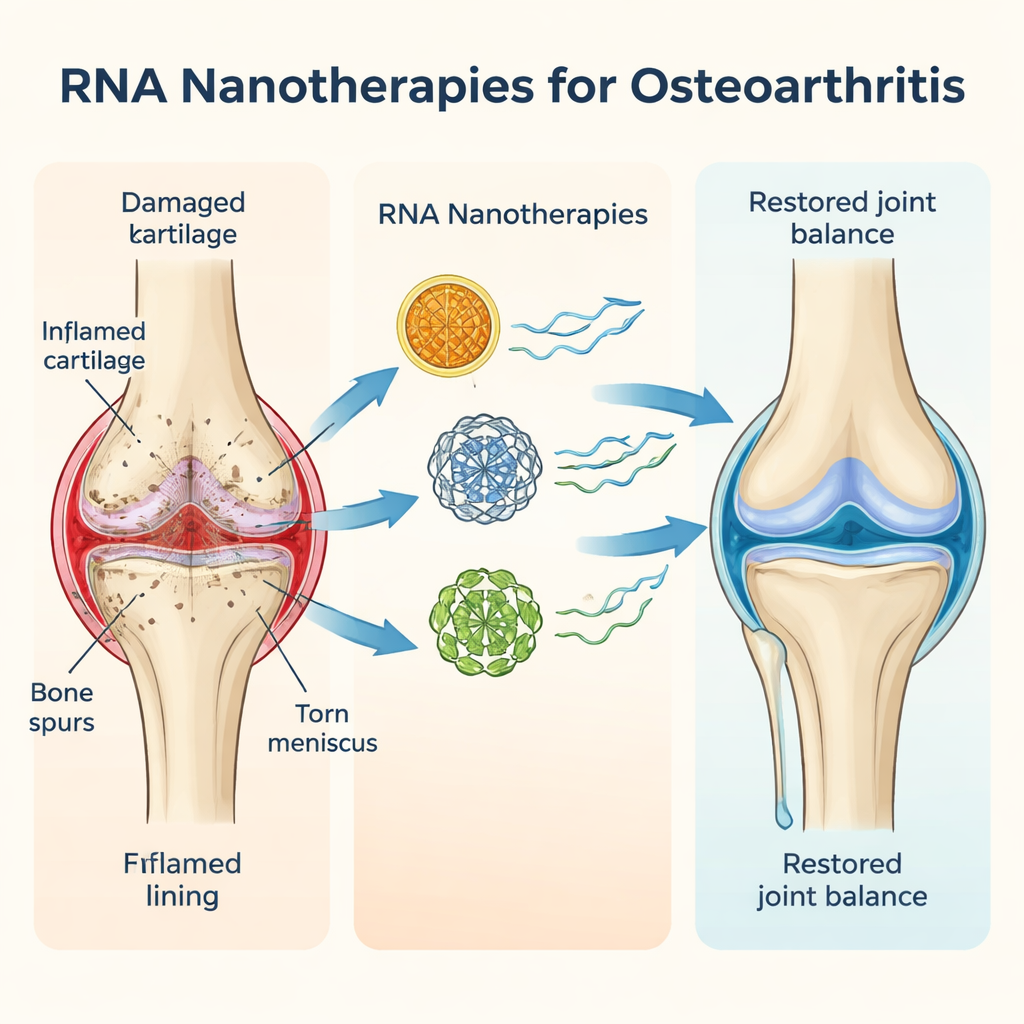
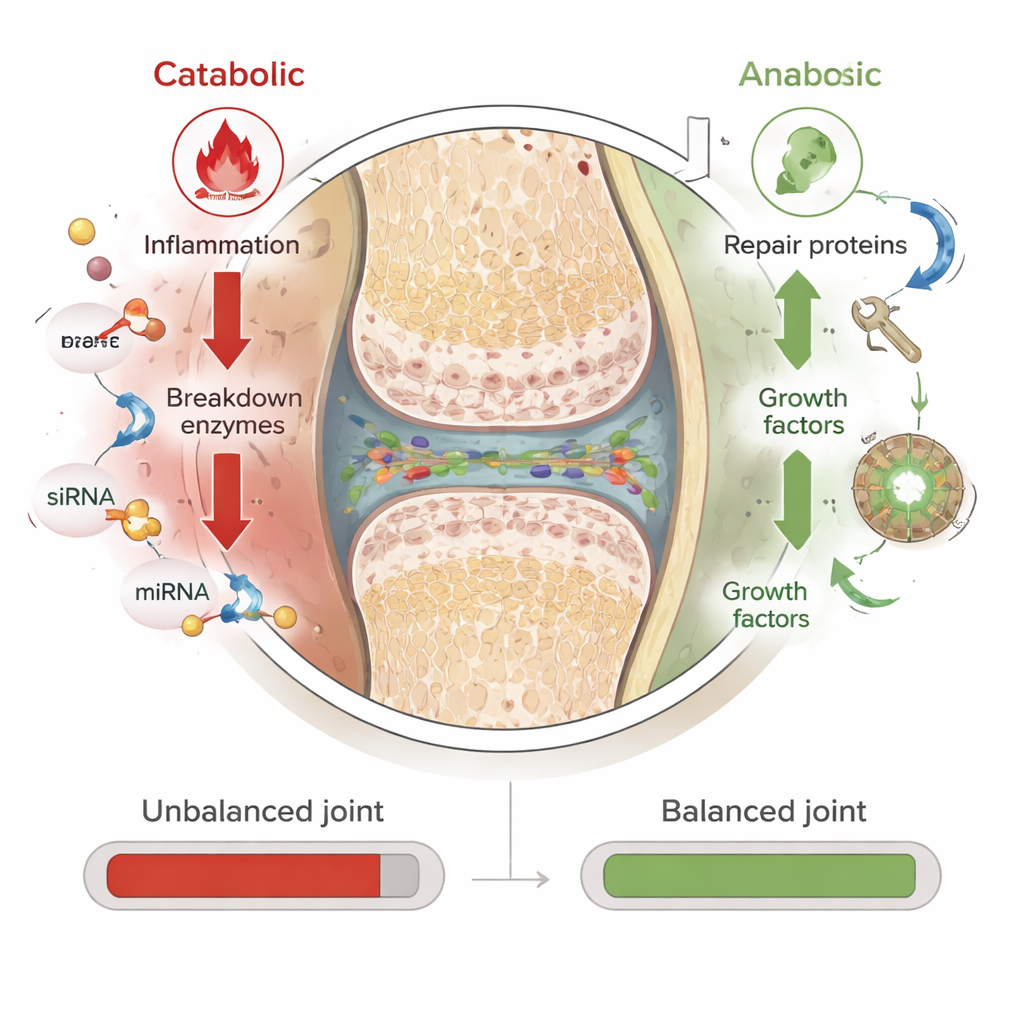
Obecnie przyjmuje się, że choroba zwyrodnieniowa stawów to zaburzenie obejmujące cały staw, a nie tylko problem przerzedzającej się chrząstki. W chorobowym kolanie gładka chrząstka amortyzująca kości ulega zużyciu, łąkotka może się postrzępić, kość pod nią pogrubieje, a błona stawowa zapali. To niskiego stopnia, przewlekłe zapalenie przez lata podtrzymuje chorobę. Autorzy opisują, jak wiek, uraz, nadmierna masa ciała i genetyka współdziałają, przechylając staw w stronę procesów „katabolicznych” rozkładających tkanki, które przytłaczają procesy „anaboliczne” naprawcze. Ponieważ u każdego pacjenta choroba jest napędzana nieco inną kombinacją czynników, reakcje na powszechne terapie — leki przeciwbólowe, zastrzyki czy nawet operacje — są bardzo zróżnicowane, a dziś żaden lek nie potrafi naprawdę zatrzymać ani odwrócić przebiegu choroby zwyrodnieniowej stawów.
Dlaczego tradycyjne terapie zawodzą
Przegląd opisuje wiele obecnych opcji — od leków przeciwbólowych dostępnych bez recepty i zastrzyków ze sterydami po fizjoterapię, ortezy i zaawansowane zabiegi, takie jak implanty chrząstki. Każde z tych rozwiązań ma zalety, ale też wyraźne ograniczenia. Środki przeciwbólowe mogą podrażniać żołądek lub serce, sterydy przy długotrwałym stosowaniu mogą uszkadzać chrząstkę, a podejścia regeneracyjne, takie jak osocze bogatopłytkowe czy komórki macierzyste, są kosztowne i pozbawione dowodów długoterminowych. Co najważniejsze, niemal wszystkie istniejące leki atakują tylko jedną stronę problemu: albo próbują uciszyć zapalenie i spowolnić rozkład, albo wzmacniają naprawę. Niewiele podejść uderza jednocześnie w obie strony tej „huśtawki”, co prawdopodobnie tłumaczy, dlaczego trudno im zmienić przebieg choroby.
Leki RNA: przepisywanie wewnętrznego scenariusza stawu
Terapie oparte na RNA działają na innym poziomie. Zamiast celować w białka po ich wytworzeniu, oddziałują na krótkotrwałe komunikaty genetyczne, które mówią komórkom, jakie białka mają produkować. Autorzy skupiają się na trzech typach. Małe interferujące RNA (siRNA) mogą precyzyjnie wyciszyć pojedynczy szkodliwy gen. MikroRNA (miRNA) mogą subtelnie regulować całe sieci genów, tłumiąc jednocześnie wiele szkodliwych szlaków. Informacyjne RNA (mRNA) robi odwrotnie: dostarcza instrukcje do syntezy przydatnych białek, takich jak czynniki wzrostu stymulujące naprawę chrząstki czy cząsteczki blokujące sygnały zapalne. Ponieważ RNA działa tylko tymczasowo i nie zmienia DNA, jego efekty są odwracalne i w zasadzie bezpieczniejsze niż trwała edycja genów. W oparciu o sukces szczepionek mRNA przeciw COVID-19, badacze testują teraz podobne pomysły w modelach zwierzęcych artretyzmu.
Nanocząstki: dostarczenie wrażliwych komunikatów do właściwych komórek
Głównym wyzwaniem jest to, że gołe RNA jest kruche i nie wnika łatwo do komórek. Przegląd opisuje, jak naukowcy pakują RNA w ochronne „nanoplatormy” — maleńkie nośniki z tłuszczów, polimerów lub krótkich peptydów. Te nanocząstki chronią RNA przed rozpadem, pomagają mu przeniknąć gęstą macierz chrząstki i zachęcają komórki wyściółki stawowej oraz chrząstki do jego pobrania. W badaniach przedklinicznych cząstki z załadowanym siRNA służyły do wyłączania genów napędzających zapalenie, stres oksydacyjny i rozkład tkanki, podczas gdy cząstki z mRNA zwiększały poziomy białek ochronnych sprzyjających smarowaniu i naprawie. Wczesne eksperymenty pokazują mniejsze uszkodzenia chrząstki i mniej bólu w modelach zwierzęcych, co sugeruje, że starannie zaprojektowane kombinacje RNA przeciwko rozkładowi i promujących naprawę mogłyby pewnego dnia działać jako prawdziwe terapie modyfikujące przebieg choroby.
Przeszkody na drodze do kliniki
Mimo obietnic, nanoleki RNA na chorobę zwyrodnieniową stawów wciąż napotykają istotne przeszkody. Układ odpornościowy może pomylić zarówno RNA, jak i jego nośnik z intruzami, wywołując niepożądane zapalenie w już podrażnionych stawach. Zastrzyki do stawu są usuwane w ciągu dni do tygodni, więc trwałe korzyści najpewniej będą wymagać inteligentnych systemów o przedłużonym uwalnianiu lub powtarzalnego dawkowania. Produkcja wysokiej jakości RNA i nanocząstek na dużą skalę jest kosztowna, a regulatorzy mają ograniczone doświadczenie w ocenianiu takich leków w przypadku powoli postępujących chorób stawów. Wreszcie, ponieważ choroba zwyrodnieniowa stawów jest tak zmienna u różnych osób, lekarze będą potrzebować lepszych metod dopasowywania konkretnych koktajli RNA do unikalnego wzorca uszkodzeń i zapalenia u każdego pacjenta.
Co to oznacza dla osób z artretyzmem
Mówiąc prosto, artykuł dowodzi, że aby naprawdę pomóc osobom z chorobą zwyrodnieniową stawów, przyszłe terapie muszą zrobić coś więcej niż tylko łagodzić ból — muszą przywrócić utraconą równowagę stawu, wyciszając geny powodujące uszkodzenia i wzmacniając geny wspierające naprawę. Leki oparte na RNA, dostarczane przez zaawansowane nośniki nanocząsteczkowe, oferują elastyczne narzędzia do osiągnięcia tego celu. Choć nie są jeszcze gotowe do stosowania klinicznego i wciąż pozostają istotne pytania dotyczące bezpieczeństwa, trwałości, kosztów i regulacji, autorzy widzą w nich realistyczną ścieżkę do spersonalizowanych, minimalnie inwazyjnych terapii, które mogłyby opóźnić lub nawet zapobiec konieczności wymiany stawu w artrozie związanej z wiekiem i po urazach.
Cytowanie: Rai, M.F., Pham, C.T., Hou, K. et al. Nucleic acid-based therapeutics to restore joint homeostasis in age-related and post-traumatic arthritis. npj Biomed. Innov. 3, 17 (2026). https://doi.org/10.1038/s44385-026-00068-8
Słowa kluczowe: choroba zwyrodnieniowa stawów, terapie RNA, nanomedycyna, regeneracja stawów, siRNA mRNA miRNA