Clear Sky Science · pl
Model bazowy do przesiewu raka piersi i płuc przy użyciu tomografii komputerowej bez kontrastu
Dlaczego jedno badanie na dwa nowotwory ma znaczenie
Przesiew raka zwykle przypomina serię osobnych kontroli: jedno badanie dla płuc, inne dla piersi — każda dodatkowa procedura zabiera czas, generuje koszty i wiąże się z dodatkowymi dawkami promieniowania. W tym badaniu badacze rozważają inną koncepcję — czy jedno, powszechnie wykonywane badanie klatki piersiowej mogłoby jednocześnie i dyskretnie przesiewać pod kątem raka płuca i raka piersi, wspomagane przez sztuczną inteligencję (AI). Jeśli podejście się sprawdzi, rutynowe skany mogłyby pełnić podwójną funkcję ochronną, zwłaszcza w zatłoczonych szpitalach i regionach o ograniczonych zasobach.
Nowy rodzaj cyfrowego zwiadowcy nowotworowego
Naukowcy opracowali system AI nazwany OMAFound, który uczy się „czytać” trójwymiarowe skany CT klatki piersiowej. W odróżnieniu od tradycyjnych narzędzi trenowanych wąsko na jednym narządzie, system ten najpierw analizuje ponad 200 000 nieoznakowanych skanów od ponad 58 000 osób, po prostu ucząc się, jak ogólnie wyglądają zdrowe i chorobowe klatki piersiowe. To szerokie wstępne uczenie pozwala AI wychwycić subtelne wzorce obejmujące całą klatkę piersiową. Zespół następnie dołącza mniejsze, oznakowane zbiory danych wskazujące, czy u pacjenta ostatecznie rozpoznano raka piersi, raka płuc czy żadnego z nich, ucząc model przekształcać ogólne rozumienie obrazu w konkretne przewidywania raka.
Uczenie jednego systemu do obserwacji dwóch narządów
Na bazie wspólnego rdzenia czytającego obrazy zespół zbudował dwie wyspecjalizowane gałęzie: jedną dostrojoną do objawów raka piersi, drugą do oznak raka płuc. Trenowali i testowali te gałęzie na skanach CT ponad 150 000 pacjentów z kilku chińskich szpitali oraz międzynarodowych zbiorów danych. Dla raka piersi stworzyli też osobny system AI analizujący mammografie, obecny standard przesiewowy, aby móc rzetelnie porównać AI oparty na CT z ugruntowaną praktyką u tych samych kobiet. W testach bezpośrednich, na kobietach mających oba rodzaje obrazów, AI do mammografii była nieco bardziej dokładna ogólnie, ale gałąź CT dla piersi była bardziej czuła — wykrywała więcej nowotworów — podczas gdy mammografia lepiej unikała fałszywych alarmów.
Od wyników narządowych do ocen całego pacjenta
Analizowanie każdego narządu oddzielnie może wprowadzać w błąd: jeśli obie gałęzie wskażą „możliwy nowotwór”, połączenie tych wyników może nierealistycznie sugerować dwa oddzielne guzy u tej samej osoby. Aby temu zapobiec, badacze stworzyli trzeci moduł AI, który miesza informacje z obu widoków (piersi i płuc) tego samego skanu CT i decyduje, czy pacjent ogólnie ma prawdopodobieństwo raka. To spojrzenie na poziomie pacjenta odzwierciedla kliniczną rzeczywistość, gdzie ludzie znacznie częściej mają pojedynczy nowotwór, jeśli w ogóle. Wśród kobiet w zestawach testowych ta zintegrowana strategia dawała najlepszy balans — wysoką czułość wobec istniejących nowotworów przy jednoczesnym opanowaniu liczby wyników fałszywie dodatnich — przewyższając proste matematyczne sposoby łączenia wyników z poziomu narządów.
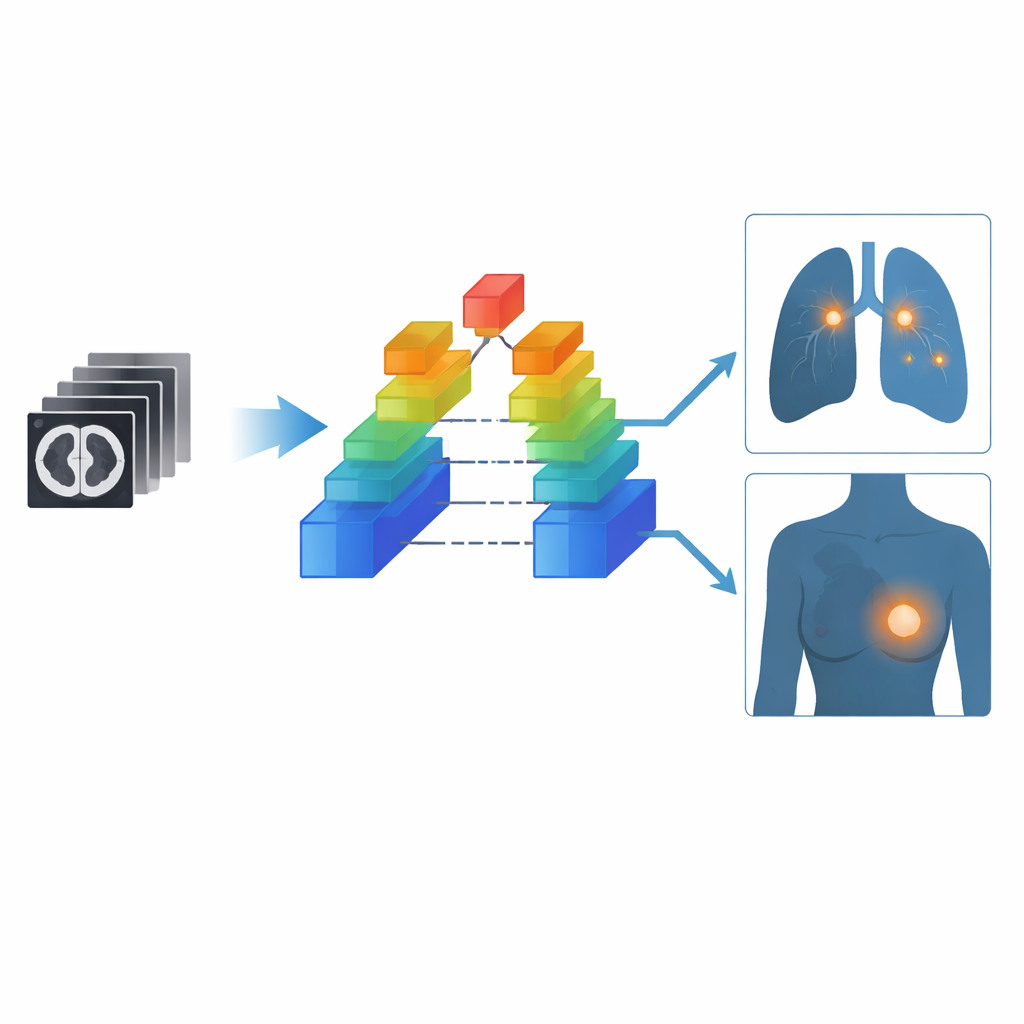
Testowanie systemu w rzeczywistym przesiewie
Aby sprawdzić, jak OMAFound działa poza laboratorium, zespół przeprowadził badanie prospektywne w czterech ośrodkach medycznych, śledząc ponad 21 000 osób zgłaszających się na niskodawkowe CT klatki piersiowej. U mężczyzn, gdzie istotny jest tylko rak płuc, system prawidłowo równoważył wykrywanie raka i fałszywe alarmy w około 86% przypadków. U kobiet osiągnięto zbalansowane dokładności około 82% dla raka piersi, 88% dla raka płuc i 83% przy decyzji, czy kobieta ma jakikolwiek nowotwór. Badacze poprosili też siedmiu radiologów ogólnych o ocenę trudnej próbki skanów, najpierw samodzielnie, a potem z ocenami ryzyka i mapami cieplnymi OMAFound wskazującymi obszary podejrzane. Z pomocą AI zdolność radiologów do wykrywania nowotworów wzrosła znacząco — szczególnie w przypadku guzów piersi — przy czym nie wzrosła ich skłonność do nadmiernego rozpoznawania przypadków niebędących nowotworem.
Co to może znaczyć dla codziennej opieki
Ogólnie rzecz biorąc, badanie sugeruje, że pojedyncze niskodawkowe CT klatki piersiowej, już szeroko stosowane do kontroli płuc, mogłoby też dostarczać dodatkowej warstwy przesiewu raka piersi przy wsparciu zaawansowanego systemu AI. OMAFound nie zastępuje mammografii ani fachowej oceny, ale mógłby wcześniej sygnalizować osoby wysokiego ryzyka i pomagać przepracowanym klinicystom skoncentrować uwagę tam, gdzie jest najbardziej potrzebna. Przekształcając jedno powszechne badanie w wielonarządowy punkt obserwacyjny, podejście to wskazuje drogę do programów przesiewowych bardziej efektywnych, bardziej dostępnych i potencjalnie ratujących więcej żyć, bez dodawania kolejnych testów, kosztów czy ekspozycji na promieniowanie.
Cytowanie: Liang, Z., Niu, Q., Wang, J. et al. A foundation model for breast and lung cancer screening using non-contrast computed tomography. Nat. Health 1, 403–415 (2026). https://doi.org/10.1038/s44360-026-00055-8
Słowa kluczowe: przesiew wielonarządowy, tomografia niskodawkowa, rak piersi, rak płuc, medyczna sztuczna inteligencja