Clear Sky Science · pl
Optymalizacja indukcji stanu zapalnego w organoidach nabłonka jelitowego pochodzących od wcześniaków
Dlaczego to ma znaczenie dla podatnych noworodków
Dzieci urodzone bardzo przedwcześnie mają do czynienia z niebezpiecznym zestawieniem: niedojrzałym jelitem i szybko zmieniającą się społecznością mikroorganizmów. Wspólnie mogą one wywołać wymykające się spod kontroli zapalenie, które uszkadza jelito i prowadzi do zagrażających życiu stanów, takich jak martwicze zapalenie jelit. Ponieważ nie możemy prowadzić eksperymentów bezpośrednio na wcześniakach, naukowcy potrzebują realistycznych modeli laboratoryjnych ich jelit, by sprawdzać, co napędza zapalenie i jak je powstrzymać. To badanie dopracowuje taki model z użyciem małych, hodowanych w laboratorium tkanek jelitowych, oferując jaśniejszy sposób badania, które sygnały mikrobiologiczne przesuwają równowagę od normalnej obrony do szkodliwego zapalenia.
Hodowla jelita wcześniaka w naczyniu
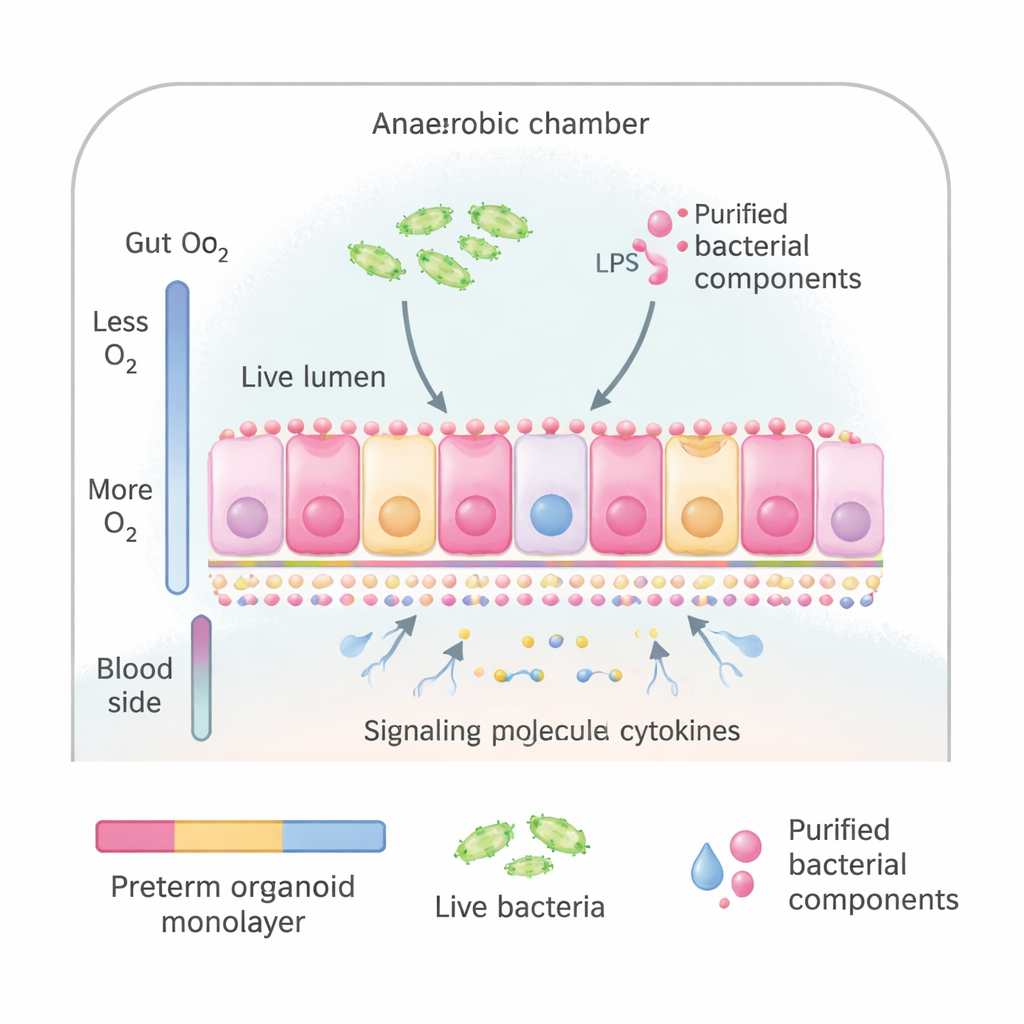
Naukowcy użyli organoidów jelitowych — miniaturowych wersji wyściółki jelita hodowanych ze komórek macierzystych pobranych od wcześniaków podczas zabiegu. Te organoidy można spłaszczyć do cienkiej warstwy komórek, która wygląda i zachowuje się podobnie do wewnętrznej powierzchni jelita cienkiego, zachowując właściwy wierzch (skierowany do światła jelita) i spód (skierowany do krwi). Zespół umieścił te warstwy w specjalnym systemie hodowlanym, który naśladuje naturalny gradient tlenu w jelicie: niskie stężenie tlenu po stronie kontaktującej się z mikrobiotą i wyższe po stronie krwi. Pozwoliło to na eksponowanie powierzchni „jelita” albo na całe bakterie pobrane od wcześniaków, albo na oczyszczone składniki bakteryjne znane z aktywowania układu odpornościowego.
Testowanie, co najlepiej uruchamia alarm zapalny
Naukowcy porównali kilka sposobów wywołania stanu zapalnego: mieszankę żywych bakterii powszechnie występujących u chorych wcześniaków; te same bakterie zabite przez działanie ciepła; oraz dwa oczyszczone sygnały bakteryjne: lipopolisacharyd (LPS) ze ścian komórkowych bakterii oraz flagelinę z wici bakteryjnych. Mierzyli uwalnianie IL‑8, białka sygnalizacyjnego przyciągającego komórki odpornościowe i służącego jako ogólny marker zapalenia, oraz wykonywali szerokozakresową analizę białek, by zobaczyć, jak zmienia się wewnętrzna maszyna komórek jelitowych. Zaskakująco, żywe lub martwe bakterie nie zwiększyły znacząco IL‑8 w tym systemie, nawet po 24 godzinach. Natomiast flagelina, a szczególnie połączenie flageliny i LPS, wywołały wyraźny wzrost IL‑8 już w ciągu trzech godzin, pokazując, że te oczyszczone sygnały mogą niezawodnie włączyć stan zapalny.
Poszukiwanie najbardziej realistycznego i efektywnego układu
Aby lepiej odzwierciedlić biologii jelita, zespół zwrócił uwagę na to, gdzie każdy sygnał działa naturalnie. LPS zwykle jest wykrywany po stronie wyściółki skierowanej ku treści jelitowej, podczas gdy flagelina jest głównie rozpoznawana po stronie tkanki. Używając znacznie niższych, bardziej fizjologicznych dawek niż we wcześniejszych eksperymentach, zastosowali LPS po stronie górnej (skierowanej ku świetle) i flagelinę po stronie dolnej (skierowanej ku krwi) arkusza organoidu. Ta prosta zmiana wywołała silną i szeroką odpowiedź w ciągu trzech godzin: z obu stron tkanki wydzielono wiele przekaźników zapalnych — w tym IL‑8, TNF i kilka chemokin. Równocześnie setki białek komórkowych zmieniły swoją obfitość, wskazując na masową aktywację szlaków obronnych.
Zapalenie, hamulce i naprawa w tym samym modelu
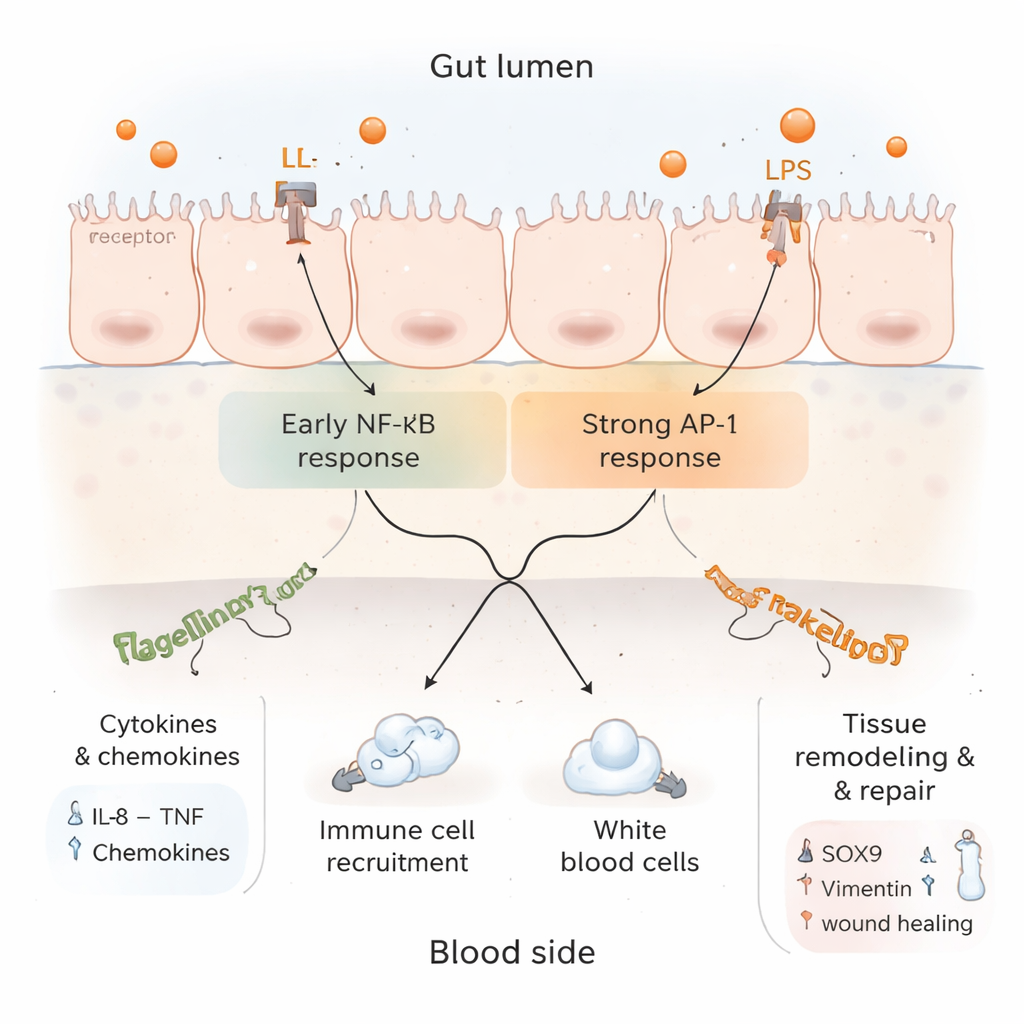
Bardziej szczegółowa analiza danych białkowych ujawniła złożony obraz. Z jednej strony wzrosły markery aktywnego zapalenia i rekrutacji komórek odpornościowych, a szlaki sygnałowe powiązane z TNF i IL‑17 — oba kluczowe dla obrony jelitowej — zostały włączone. Z drugiej strony kilka składników klasycznego szlaku NF‑κB, który napędza wiele genów zapalnych, zostało przytłumionych, podczas gdy alternatywna droga z udziałem AP‑1 pozostała aktywna. Sugeruje to, że po początkowym alarmie tkanka zaczyna wprowadzać hamulce, aby zapobiec niekontrolowanym uszkodzeniom. Równocześnie wzrosła obfitość białek związanych z regeneracją tkanek, przebudową strukturalną i kontrolowaną śmiercią komórkową, co sugeruje, że wyściółka jelita nie tylko jest objęta zapaleniem, ale też próbuje się przebudować i naprawić.
Co to oznacza dla przyszłych terapii
Porównując systematycznie różne bodźce mikrobiologiczne, dawki, pozycje i czasy ekspozycji, autorzy dochodzą do wniosku, że trzygodzinna ekspozycja na niską dawkę LPS po stronie jelitowej wraz z flageliną po stronie naczyniowej jest najpewniejszym i najbardziej powtarzalnym sposobem wywołania zapalenia w organoidach jelitowych pochodzących od wcześniaków. Ten dopracowany model odzwierciedla nie tylko napływ zapalenia, ale także wbudowane hamulce, mechanizmy tolerancji i odpowiedzi naprawcze w delikatnym jelicie wcześniaka. Dostarcza praktycznego planu dla innych laboratoriów do badania, jak konkretne mikroby, leki czy czynniki żywieniowe mogą pogarszać lub łagodzić zapalenie jelit u bardzo przedwcześnie urodzonych niemowląt — co stanowi istotny krok w kierunku bezpieczniejszych, ukierunkowanych strategii zapobiegania wyniszczającym chorobom jelitowym w tej wrażliwej grupie.
Cytowanie: Chapman, J.A., Frey, A.M., Dueñas, M.E. et al. Optimising the induction of inflammation within preterm infant-derived intestinal epithelial organoids. npj Gut Liver 3, 5 (2026). https://doi.org/10.1038/s44355-026-00054-2
Słowa kluczowe: jelito wcześniaka, organoidy jelitowe, zapalenie jelit, mikrobiom, martwicze zapalenie jelit