Clear Sky Science · pl
Nieustrojowe chemomechaniczne przetwarzanie ATP napędzające rozkład białek w proteasomie 26S
Jak maleńka maszyna utrzymuje porządek w naszych białkach
Wewnątrz każdej komórki działa mikroskopijny tryb rozdrabniający zwany proteasomem 26S, który nieustannie usuwa uszkodzone lub już niepotrzebne białka, utrzymując komórkę w zdrowiu. U podstaw tej maszyny leży pierścieniowy silnik, który spala chemiczne paliwo (ATP), by chwycić, rozwinąć i wciągnąć białka do centralnej komory, gdzie są pocięte. W artykule zastosowano zaawansowane symulacje komputerowe, aby ujawnić, jak ten silnik przekształca energię chemiczną w ruch mechaniczny, dostarczając szczegółowego, ilościowego obrazu procesu leżącego u podstaw starzenia, chorób mózgu, odporności i raka.
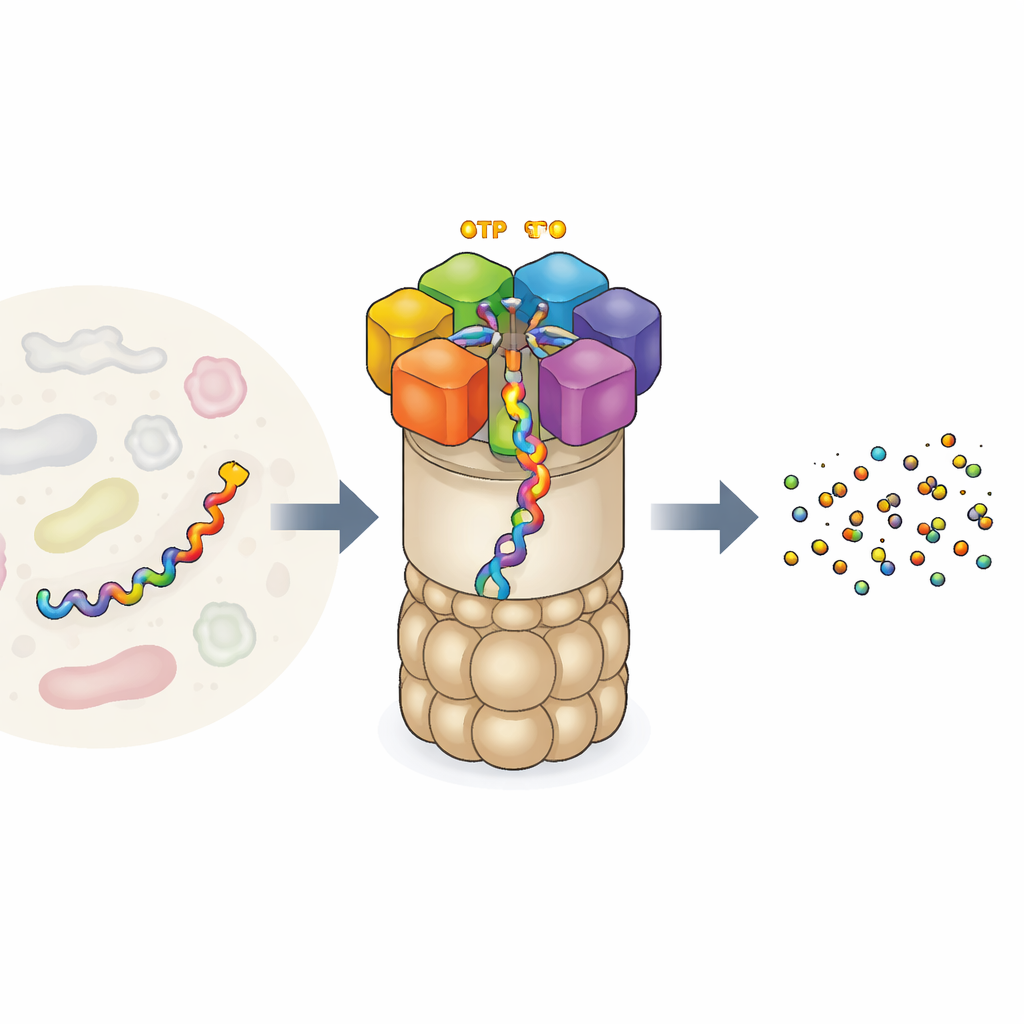
Fabryka recyklingu białek w komórce
Proteasom 26S jest jednym z największych i najbardziej złożonych maszynerii białkowych w naszych komórkach. Składa się z cylindrycznego rdzenia, który tnie białka, oraz regulatorycznej nasadki, która rozpoznaje, które białka trzeba zniszczyć. U wejścia znajduje się pierścień złożony z sześciu różnych jednostek napędowych. Każda z nich może związać ATP, uniwersalną walutę energetyczną komórki, i użyć tej energii, by chwycić łańcuch białkowy i wciągnąć go do rdzenia w celu rozkładu. Ten mechanizm nie działa przypadkowo: wcześniejsze eksperymenty sugerowały, że sześć jednostek współpracuje w skoordynowany sposób „ręka po ręce”, przekazując białko jak wspinacze po linie. Jednak eksperymenty dostarczały tylko kilku migawkowych obrazów tego działania, pozostawiając pytania o pełną sekwencję ruchów i o to, jak dokładnie spalanie paliwa łączy się z pracą mechaniczną.
Symulowanie molekularnej przeciągania liny
Autorzy stworzyli probabilistyczny model komputerowy, który traktuje silnik jako system przeskakujący między wieloma możliwymi kształtami, podczas gdy cząsteczki ATP i jego produktów wiążą się i odłączają. Zdefiniowali 30 głównych konformacji pierścienia, w których jedna, dwie lub trzy podjednostki tracą uchwyt białka, oraz specjalny, ścisle zamknięty stan, w którym wszystkie sześć trzyma. Używając standardnego algorytmu do symulacji losowych zdarzeń chemicznych, śledzili setki tysięcy kroków, w których zachodzi wiązanie ATP, rozkład ATP i zmiany kształtu silnika. Z tych przebiegów mogli przewidzieć, jak szybko białko jest wciągane przy różnych warunkach, takich jak zmienne stężenia ATP, jego zużytej formy ADP oraz nieulegającego rozkładowi analogonu ATP często używanego w eksperymentach.
Kiedy zbyt dużo paliwa spowalnia silnik
Symulacje odtworzyły kilka zagadkowych obserwacji eksperymentalnych. Wraz ze wzrostem poziomów ATP z niskich wartości, silnik ciągnie białka szybciej, ponieważ wiązanie paliwa jest krokiem najszybszym ograniczającym tempo. Ale powyżej około 1 milimola ATP szybkość osiąga szczyt, a następnie spada: pierścień spędza więcej czasu w zablokowanej, nietranslokującej konformacji, w której wszystkie sześć podjednostek jest zajętych ATP, a mimo to białko nie porusza się. Dodanie ADP lub nieulegającego rozkładowi analogonu ATP stopniowo spowalnia silnik, ponieważ te cząsteczki konkurują z ATP o miejsca wiążące, ale nie mogą wykonać pełnego skoku napędowego. Model przewiduje też, jak silnik zachowuje się w zetknięciu z bardzo silnie pofałdowanymi regionami białka, które działają jak przeszkody. W takich przypadkach silnik spędza więcej czasu walcząc z oporem, a ogólna szybkość degradacji spada, co odpowiada pomiarom wykonywanym na sztucznie stabilizowanych domenach białkowych.
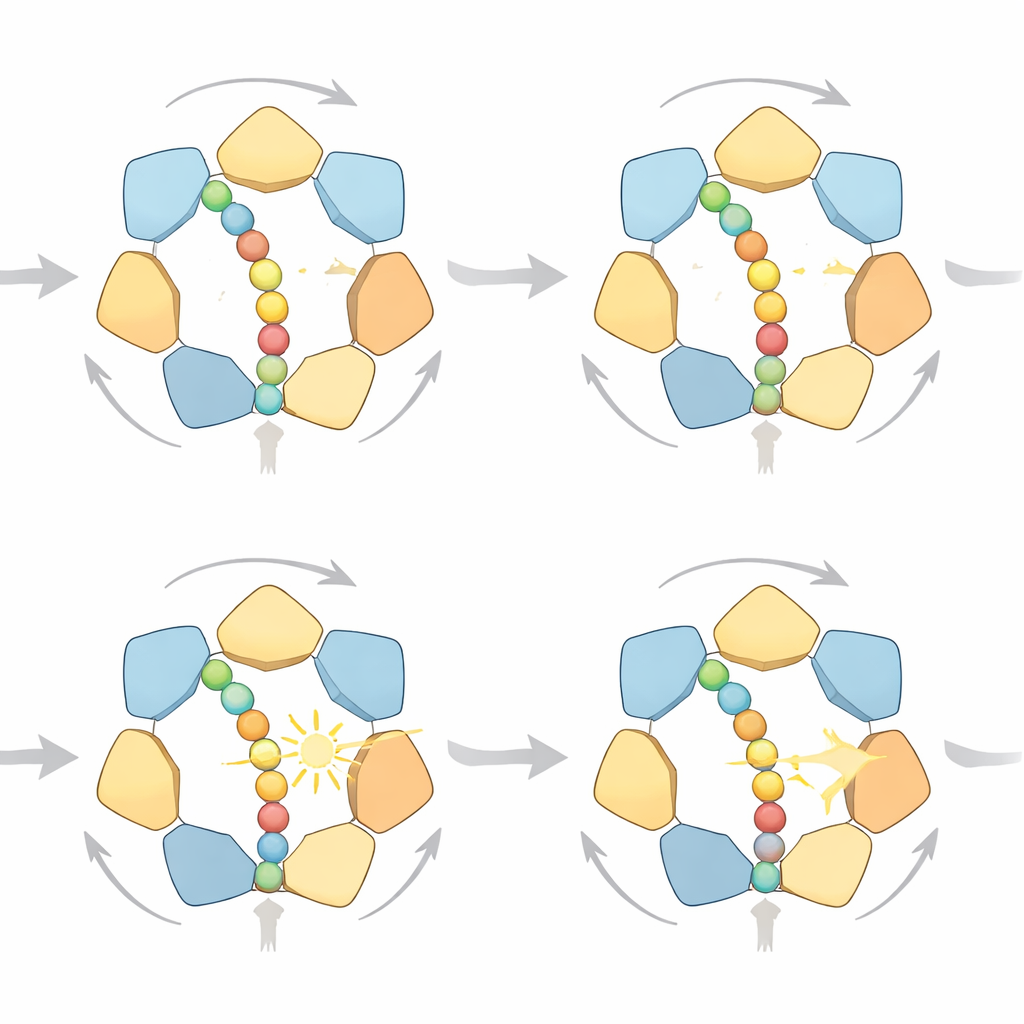
Wiele sposobów na wykonanie kroku
Analizując szczegółowo trajektorie z symulacji, badacze odkryli, że pierścień nie podąża jedynie jednym sztywnym cyklem. Zamiast tego istnieje wiele ścieżek o wysokim prawdopodobieństwie, które wszystkie respektują tę samą kierunkową zasadę „ręka po ręce”: podjednostki bliskie wyjścia pierścienia zwalniają białko po rozpadzie ATP, przesuwają się na szczyt spiralnych stopni podjednostek i ponownie chwytają łańcuch wyżej. Czasami białko postępuje o jeden mały krok, czasami o dwa, w zależności od tego, ile podjednostek zwalnia jednocześnie. Przy obfitym paliwie dominują ruchy jednokrokowe, ponieważ marnują mniej pracy przeciwko siłom przeciwnym; gdy paliwa brakuje, model przewiduje częstsze skoki dwukrokowe. Symulacje łączą też obciążenie mechaniczne ze stanem chemicznym silnika: w miarę wzrostu oporu i zatrzymania białka, ADP ma tendencję do gromadzenia się w większej liczbie z sześciu kieszeni wiążących — dokładnie to, co obserwują badania strukturalne o wysokiej rozdzielczości.
Wykorzystanie energii i wspólne zasady projektowe
Model pozwala autorom odwzorować, jak energia silnika rośnie podczas rozkładu ATP i spada, gdy ta energia przekształcana jest w ruch. Obliczają krzywą wydajności pokazującą, że silnik działa najlepiej przy umiarkowanej sile przeciwnej: zbyt mały opór powoduje marnotrawne spalanie ATP; zbyt duży i mechanizm niemal zatrzymuje się. Gdy zespół porównał swoje przewidywania z danymi z pokrewnych maszyn niszczących białka u bakterii i drożdży, znalazł bardzo podobne trendy w tym, jak nieulegający rozkładowi analogon ATP spowalnia te silniki. Sugeruje to, że wielu członków tej samej rodziny pierścieniowych enzymów prawdopodobnie dzieli wspólny, zachowany mechanizm ciągnięcia za białka.
Dlaczego to ma znaczenie dla zdrowia i chorób
Przekształcając rozproszone migawki strukturalne i pomiary biochemiczne w jedną, testowalną ramę, praca ta pokazuje w ilościowych szczegółach, jak maleńki silnik molekularny tłumaczy chemiczne paliwo na siłę, by recyclować białka komórki. Model nie tylko wyjaśnia szeroki zakres istniejących eksperymentów, lecz także formułuje przewidywania, jak zmiany poziomu paliwa, obciążenia mechanicznego czy mutacje silnika mogą wpływać na degradację białek. Ponieważ podobne maszyny działają w całym królestwie życia i odgrywają kluczową rolę w schorzeniach od neurodegeneracji po raka, zrozumienie ich działania na tym poziomie może ostatecznie ukierunkować projektowanie leków, które modulują, wzmacniają lub selektywnie blokują te mikroskopijne rozdrabniacze.
Cytowanie: Wu, D., Ouyang, Q., Wang, H. et al. Nonequilibrium chemomechanical transduction of ATP-driven protein unfolding in the 26S proteasome. npj Biol. Phys. Mech. 3, 4 (2026). https://doi.org/10.1038/s44341-026-00034-w
Słowa kluczowe: proteasom, silnik AAA+ ATPazy, degradacja białek, maszyny molekularne, sprzężenie chemomechaniczne