Clear Sky Science · pl
Bioassay wzmocniony plazmonicznie do wykrywania i ilościowego oznaczania RNA SARS-CoV-2 bez amplifikacji
Dlaczego ważne są szybsze, prostsze testy na wirusy
Pandemia COVID-19 ujawniła, jak bardzo zależymy od badań laboratoryjnych, które są czasochłonne, kosztowne i trudne do szybkiego skalowania, gdy miliony osób potrzebują odpowiedzi. Opisane tutaj badanie przedstawia nowy rodzaj testu laboratoryjnego, który potrafi wykrywać i zliczać bardzo małe ilości materiału genetycznego koronawirusa bez standardowego etapu amplifikacji używanego w PCR. Podejście to ma na celu przybliżenie dokładności na poziomie szpitalnym do prostszych, tańszych testów, które można by szerzej wdrożyć podczas przyszłych epidemii.
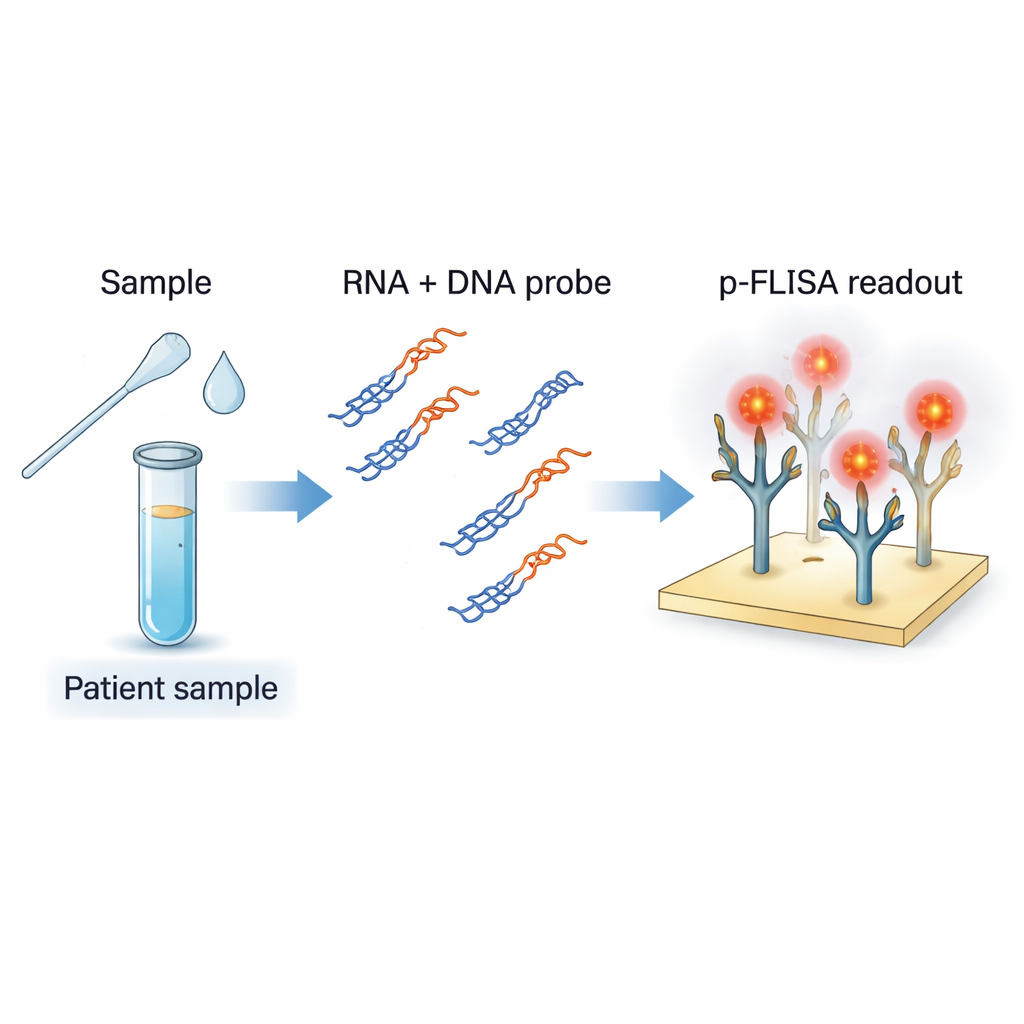
Nowy sposób wykrywania śladów genetycznych wirusa
Standardowa diagnostyka COVID-19 wykorzystuje RT‑PCR, która tworzy wiele kopii fragmentów RNA wirusa, aby można je było wykryć. Chociaż bardzo czuła, PCR wymaga skomplikowanego sprzętu, wyszkolonego personelu i czasu, a zwykle daje odpowiedź „tak/nie” zamiast precyzyjnego pomiaru ilości wirusa. Autorzy postawili sobie za cel zbudowanie testu działającego bardziej jak znacznie ulepszona wersja testu ELISA: proste, płytkowe rozwiązanie, ale dostrojone do bezpośredniego wykrywania RNA wirusa i ilościowego określania jego zawartości. Metoda celuje w RNA SARS‑CoV‑2 w próbkach takich jak wymazy z nosa i ślina, ale zaprojektowano ją tak, by można ją było łatwo dostosować do innych wirusów RNA.
Przekształcanie RNA w łatwy do wychwycenia cel
Zespół wykorzystuje krótkie fragmenty DNA zaprojektowane tak, by pasowały do określonych regionów genomu SARS‑CoV‑2. Po zmieszaniu z RNA wyekstrahowanym z próbki pacjenta i delikatnym podgrzaniu oraz schłodzeniu, sondy DNA łączą się z dopasowanym RNA wirusa, tworząc hybrydy DNA–RNA, jak mały zamek błyskawiczny z jedną nicią RNA i jedną nicią DNA. Specjalne przeciwciało S9.6 działa jak „łapacz”: rozpoznaje i mocno wiąże te hybrydy, ale nie wiąże zwykłego jednoniciowego czy dwuniciowego DNA ani niespowinowaconego RNA. Pokrywając dno płytki S9.6, test selektywnie wyłapuje tylko te hybrydy zawierające interesujące sekwencje wirusowe, odsiewając resztę genetycznego „szumu” próbki.
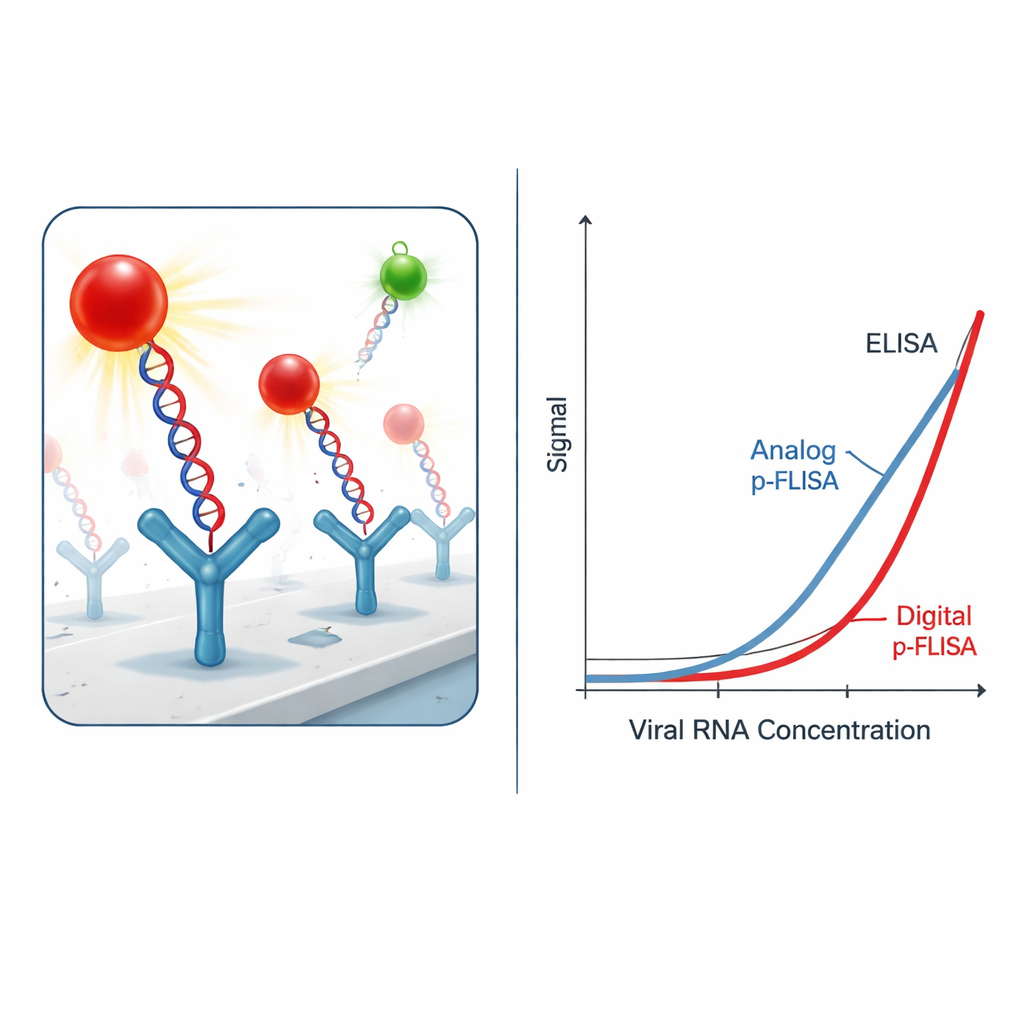
Uczynienie sygnału ultrajasnym
Samo wychwycenie hybryd wirusowych nie wystarcza; wyzwaniem jest ich dostrzeżenie ponad tłem. Zamiast konwencjonalnych barwników fluorescencyjnych, badacze używają nanonaklejek „plasmonic‑fluor” — zaprojektowanych nanocząstek działających jak maleńkie anteny optyczne. Każda etykieta łączy nanorod metalowy z wieloma cząsteczkami fluorescencyjnymi i powłoką umożliwiającą przyczepienie się do znaczników biotyny na DNA lub przeciwciele. Te plazmoniczne etykiety emitują światło ponad tysiąc razy silniejsze niż standardowe barwniki w tych samych warunkach. W praktyce oznacza to, że potrzeba znacznie mniej hybryd wirusowych, aby uzyskać wykrywalny blask, co dramatycznie poprawia czułość testu i obniża minimalne stężenie RNA wirusa, które można zmierzyć.
Z przejścia od analogowego blasku do cyfrowego zliczania
W najprostszej, „analogowej” formie test mierzy sumaryczną jasność z każdej studzienki płytki, podobnie jak klasyczny test fluorescencyjny. Nawet w tym trybie system wzmocniony plazmonicznie poprawia granicę wykrywania i najniższy niezawodnie ilościowy poziom RNA SARS‑CoV‑2 o jeden do trzech rzędów wielkości w porównaniu z tradycyjną ELISA wykorzystującą enzymy lub standardowe fluorofory. Autorzy posunęli pomysł dalej, przechodząc do formatu „cyfrowego”: zamiast uśredniać światło po całej studzience, obrazują powierzchnię mikroskopem fluorescencyjnym i zliczają pojedyncze jasne nanonaklejki przy użyciu opracowanego oprogramowania do analizy obrazów. Podejście liczenia pojedynczych cząstek daje dodatkowy, dziesięciokrotnie do trzydziestokrotnie lepszy zysk w czułości, prowadząc łącznie do około 2300‑krotnego polepszenia granic wykrywania i 460‑krotnego polepszenia granic ilościowych w porównaniu z ELISA.
Próba testu na rzeczywistych próbkach
Aby sprawdzić, czy metoda sprawdza się poza kontrolowanymi mieszaninami laboratoryjnymi, badacze testowali RNA wyekstrahowane z wymazów z nosa i śliny pacjentów z COVID‑19, w tym zakażeń różnymi wariantami wirusa, takimi jak alfa/beta i delta, a także próbek od osób z innymi wirusami układu oddechowego. Ich test wzmocniony plazmonicznie wykrył RNA SARS‑CoV‑2 we wszystkich próbkach pozytywnych w PCR, przy braku sygnału powyżej tła w próbkach negatywnych w PCR lub tych zawierających inne wirusy, co wskazuje na doskonałą czułość i swoistość kliniczną porównywalną z RT‑PCR. Co więcej, zmierzone stężenia RNA wykazywały odwrotną zależność od wartości progu cyklu PCR: próbki wymagające mniejszej liczby cykli PCR (co wskazuje na wyższe obciążenie wirusowe) miały wyższe poziomy RNA w nowym teście, zgodnie z oczekiwaniami biologicznymi i sugerując, że test może dostarczać sensownych, ilościowych informacji o ładunku wirusowym.
Co to może oznaczać dla przyszłych epidemii
Dla osób niezwiązanych ze specjalistyczną diagnostyką najważniejszym przesłaniem jest to, że test oferuje sposób odczytu, ile wirusa jest obecne, bez dodatkowego etapu powielania, który sprawia, że PCR jest wolny i wymaga zaawansowanego sprzętu. Poprzez połączenie selektywnego przeciwciała dla hybryd RNA–DNA z ultrajasnymi nanoskalowymi źródłami światła i cyfrowym zliczaniem, metoda zbliża się do wydajności PCR, zachowując jednocześnie prosty, płytkowy przebieg pracy. Po dalszej walidacji i dopracowaniu inżynieryjnym takie testy wzmocnione plazmonicznie mogłyby zostać dostosowane do wielu celów RNA i być potencjalnie przekształcone w szybkie testy przyłóżkowe, pomagając klinicystom nie tylko w diagnozie zakażeń, ale też w ocenie stadium choroby i zakaźności na podstawie bezwzględnego pomiaru RNA wirusa.
Cytowanie: Liu, L., Seth, A., Liu, Y. et al. Plasmon-enhanced bioassay for amplification-free detection and quantification of SARS-CoV-2 RNA. npj Biosensing 3, 13 (2026). https://doi.org/10.1038/s44328-026-00078-x
Słowa kluczowe: Wykrywanie RNA SARS-CoV-2, plazmoniczne nanoprostowniki, cyfrowy test immunologiczny, diagnostyka bez amplifikacji, ilościowe oznaczanie obciążenia wirusowego