Clear Sky Science · pl
Bioczujnik mikroprzyorganiczny w mikrofluidyce do ciągłego monitorowania poziomu glukozy in vivo
Dlaczego to ma znaczenie dla osób z cukrzycą
Dla osób żyjących z cukrzycą typu 1 współczesne systemy „sztucznej trzustki” wciąż wymagają stałej uwagi — zgłaszania posiłków, obsługi alarmów i troski o nocne epizody niskiego poziomu cukru. Badanie to bada radykalnie inny rodzaj czujnika glukozy, który nie opiera się na pojedynczym enzymie ani na równaniu komputerowym, lecz wykorzystuje mały żywy fragment mechanizmu kontroli cukru w organizmie: skupiska komórek trzustkowych zwane wyspami. Pozwalając tym mini‑organom robić to, do czego ewolucja je zoptymalizowała, autorzy dążą do stworzenia mądrzejszych, bezpieczniejszych monitorów glukozy, które pewnego dnia mogłyby działać bardziej niezależnie w tle.
Maleńki organ jako żywy czujnik
Większość obecnych bioczujników wykrywa związki chemiczne przy użyciu oczyszczonych cząsteczek lub jednolinii komórkowych. Reagują one na jedną, konkretną substancję, a surowy sygnał jest następnie interpretowany przez oprogramowanie. Autorzy argumentują, że takie podejście pomija potężny wbudowany „komputer”: mikro‑organy, jak wyspy trzustkowe, które naturalnie wyczuwają wiele sygnałów jednocześnie i przekształcają je w skoordynowaną odpowiedź. Każda wyspa zawiera kilka typów komórek produkujących hormony, które stale komunikują się ze sobą. Razem utrzymują poziom glukozy we krwi w wąskim, bezpiecznym zakresie, reagując nie tylko na glukozę, lecz także na aminokwasy, hormony jelitowe i stresu oraz na niedawną historię wahań cukru. Jak sugerują autorzy, ta wbudowana złożoność mogłaby zostać wykorzystana do dostarczania bogatszych, bardziej wiarygodnych informacji niż prosty czujnik oksydazy glukozy.
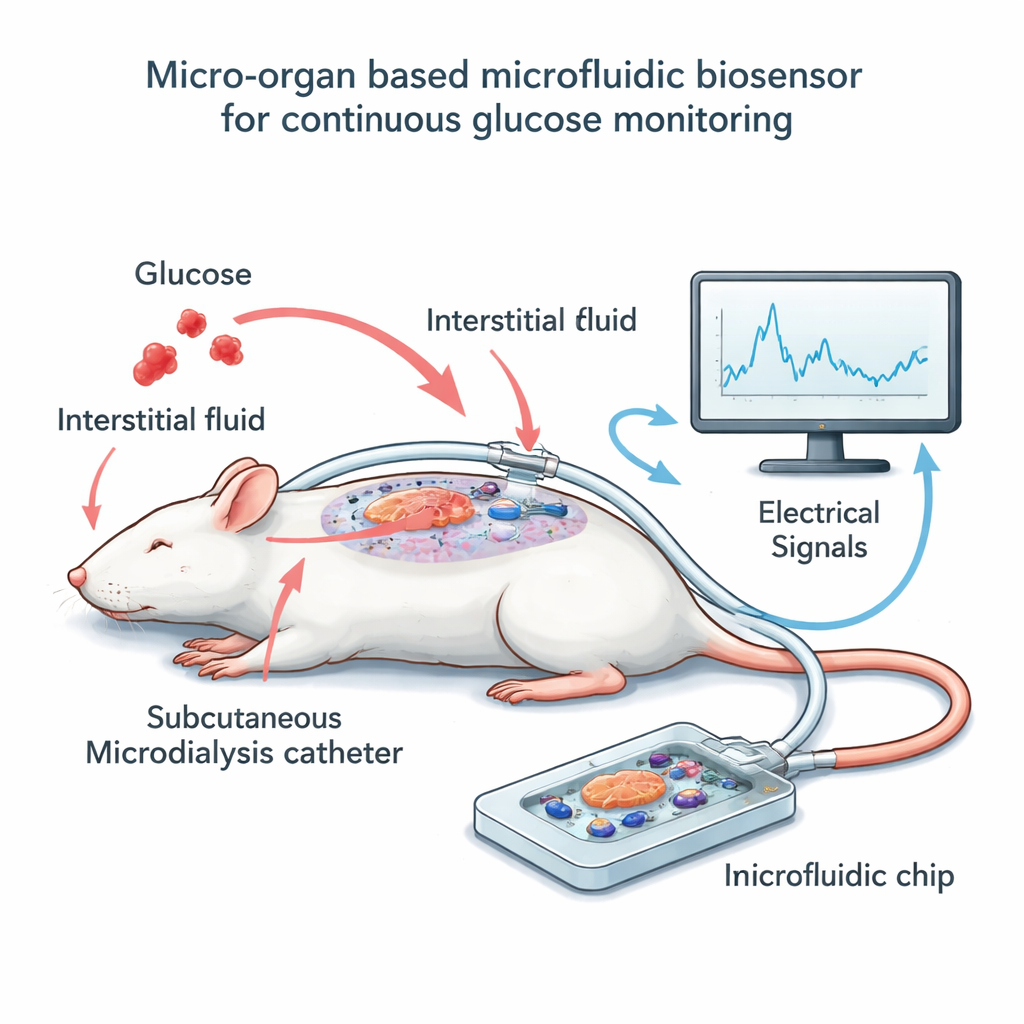
Budowa układu chip‑cewnik
Aby przetestować ten pomysł, zespół zbudował niewielkie urządzenie poza organizmem, w którym umieścił kilkadziesiąt wysp mysich na siatce mikroskopijnych elektrod. Zamiast bezpośredniego wystawiania tych komórek na kontakt z krwią, zastosowano technikę zwaną mikrodializą: cienki, elastyczny cewnik umieszczono tuż pod skórą u uśpionych szczurów, który powoli pobiera otaczający płyn tkankowy — ściśle odzwierciedlający poziom glukozy we krwi, choć z krótkim opóźnieniem. Niski, stały przepływ przenosi ten płyn przez wąski kanał nad wyspami na chipie. Gdy poziomy glukozy w dializacie rosną i maleją, wyspy zmieniają swoją aktywność elektryczną, którą elektrody rejestrują jako powolne, falowe sygnały. Równolegle badacze okresowo mierzyli glukozę we krwi szczurów i w dializacie, co pozwoliło dopasować odczyt elektryczny do rzeczywistych poziomów cukru w czasie.
Jak żywy czujnik reagował na zmiany poziomu cukru
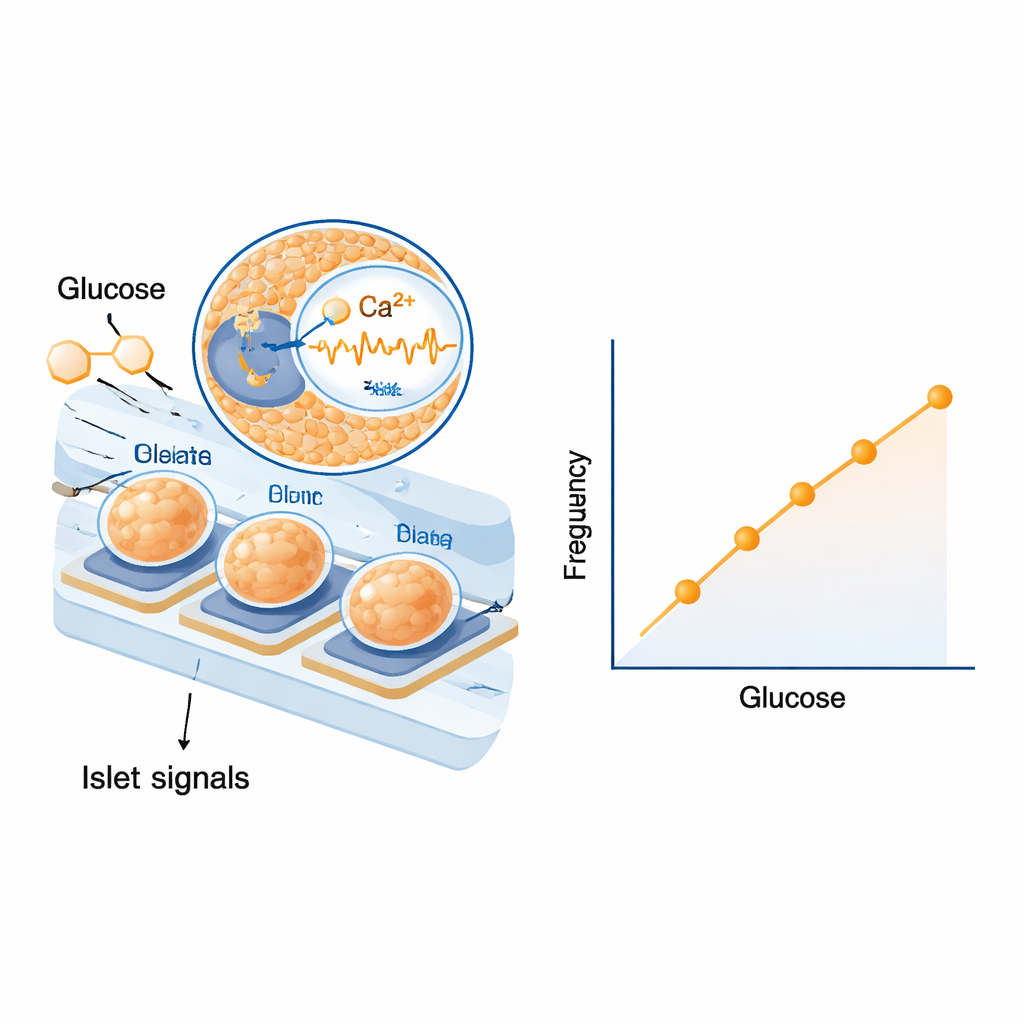
Pierwsi naukowcy sprawdzili, czy wyspy na elektrodach potrafią reagować na składniki krwi, a nie tylko na proste roztwory laboratoryjne. Ekspozycja na surowicę ludzką i szczurzą o różnych poziomach glukozy wywołała wyraźne, stopniowe zmiany zarówno w częstotliwości, jak i w amplitudzie ich fal elektrycznych. Odpowiedzi były wystarczająco silne, by rozróżnić małe kroki w stężeniu cukru w zakresie istotnym dla cukrzycy. Następnie przeprowadzono eksperymenty na szczurach — podano wstrzyknięcie glukozy, aby podnieść poziom cukru, a później podano insulinę, by go obniżyć. Po uwzględnieniu czasu potrzebnego na przenikanie glukozy z krwi do płynu tkankowego i przez przewody, stwierdzono, że częstotliwość powolnych sygnałów elektrycznych wysp wzrastała i malała niemal synchronicznie z poziomem glukozy we krwi. Analiza statystyczna przeprowadzona na kilku zwierzętach wykazała niezwykle ścisły, powtarzalny związek między częstotliwością sygnału a stężeniem glukozy, podczas gdy amplituda sygnału, choć informatywna, była nieco bardziej zmienna.
Wbudowane mechanizmy bezpieczeństwa od biologii
Istotną zaletą użycia całych wysp, zamiast pojedynczej cząsteczki, jest to, że ich zachowanie już zawiera mechanizmy bezpieczeństwa ukształtowane przez ewolucję. Wcześniejsze prace i wskazówki z tego badania pokazują, że wyspy reagują silniej, gdy glukoza spada, niż gdy rośnie — forma „histerezy”, która pomaga chronić przed niebezpieczną hipoglikemią. Wzorce elektryczne kształtowane są także przez sąsiadujące typy komórek, które wzmacniają lub tłumią uwalnianie insuliny w zależności od potrzeb organizmu. Ponieważ chip jedynie nasłuchuje tych zintegrowanych sygnałów bez dodawania barwników czy modyfikacji genetycznych, może rejestrować przez dni bez uszkadzania komórek. Autorzy wskazują na wyzwania techniczne przed nimi, takie jak unikanie pęcherzyków powietrza, zapewnienie długotrwałej wydajności mikrodiaplizy oraz decyzja, jaki typ wysp pochodzących od ludzi lub z komórek macierzystych powinien być ostatecznie użyty. Mimo to symulacje komputerowe z użyciem ustalonego modelu cukrzycy sugerują, że taki sensor oparty na wyspach mógłby dorównać lub nawet przewyższyć dzisiejsze monitory glukozy w trudnych warunkach.
Co to może znaczyć dla przyszłej opieki nad cukrzycą
Ta praca pokazuje, że garstka mikro‑organów trzustkowych, utrzymana przy życiu na małym chipie i połączona z organizmem cienkim cewnikiem, potrafi na żywo śledzić poziom cukru u zwierząt dzięki swojej naturalnej elektrycznej „gadaninie”. Dla czytelnika niebędącego specjalistą kluczowy przekaz jest taki: zamiast prosić prosty czujnik chemiczny o zmierzenie glukozy i zmuszać komputer do odgadywania, co to znaczy dla organizmu, podejście to słucha bezpośrednio tego samego typu żywej tkanki, która normalnie decyduje o tym, ile insuliny uwolnić. Jeśli zostanie dopracowane i uczynione praktycznym dla ludzi, takie żywe bioczujniki mogłyby stać się rdzeniem naprawdę autonomicznych systemów sztucznej trzustki — urządzeń, które cicho przewidują potrzeby organizmu i zmniejszają codzienny ciężar zarządzania cukrzycą.
Cytowanie: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
Słowa kluczowe: ciągłe monitorowanie glukozy, sztuczna trzustka, wyspy trzustkowe, mikrofluidyczny bioczujnik, cukrzyca typu 1