Clear Sky Science · pl
Przegląd narracyjny wpływu apolipoprotein na miażdżycowe blaszki wieńcowe
Dlaczego tłuszcze we krwi wciąż mają znaczenie
Zawały serca i udary często zaczynają się od cichych zmian w naczyniach odżywiających serce. Artykuł wykracza poza znane pojęcia „dobrego” i „złego” cholesterolu, skupiając się na białkowych osłonkach przenoszących tłuszcze w krwiobiegu — apolipoproteinach. Śledząc, jak cztery z tych białek kształtują rozwój, skład i leczenie blaszek wieńcowych — tłuszczowych złogów zatykających tętnice serca — autorzy pokazują, dlaczego niektórzy ludzie pozostają w wysokim ryzyku chorób serca, nawet gdy ich wyniki cholesterolu wyglądają idealnie.
Ukryci gracze na powierzchni cholesterolu
Większość z nas słyszała o cholesterolu LDL i HDL, lecz każda z tych cząstek jest otoczona jedną lub kilkoma apolipoproteinami, które wpływają na to, dokąd cząstka trafi i jak niebezpieczna może być. Ten przegląd koncentruje się na czterech kluczowych typach: apolipoproteinie(a), apolipoproteinie A‑I, apolipoproteinie B oraz apolipoproteinie C‑III. Razem regulują one, jak powstają cząstki tłuszczowe, jak długo krążą oraz jak łatwo wnikają i uszkadzają ścianę tętnicy. Nowoczesne narzędzia obrazowania — ultradźwięk wewnątrznaczyniowy, wysokorozdzielcze skany optyczne i tomografia komputerowa z angiografią — pozwalają lekarzom zobaczyć nie tylko stopień zwężenia naczynia, ale też, czy blaszki są miękkie i podatne na pęknięcie, czy gęste i zwapniałe. 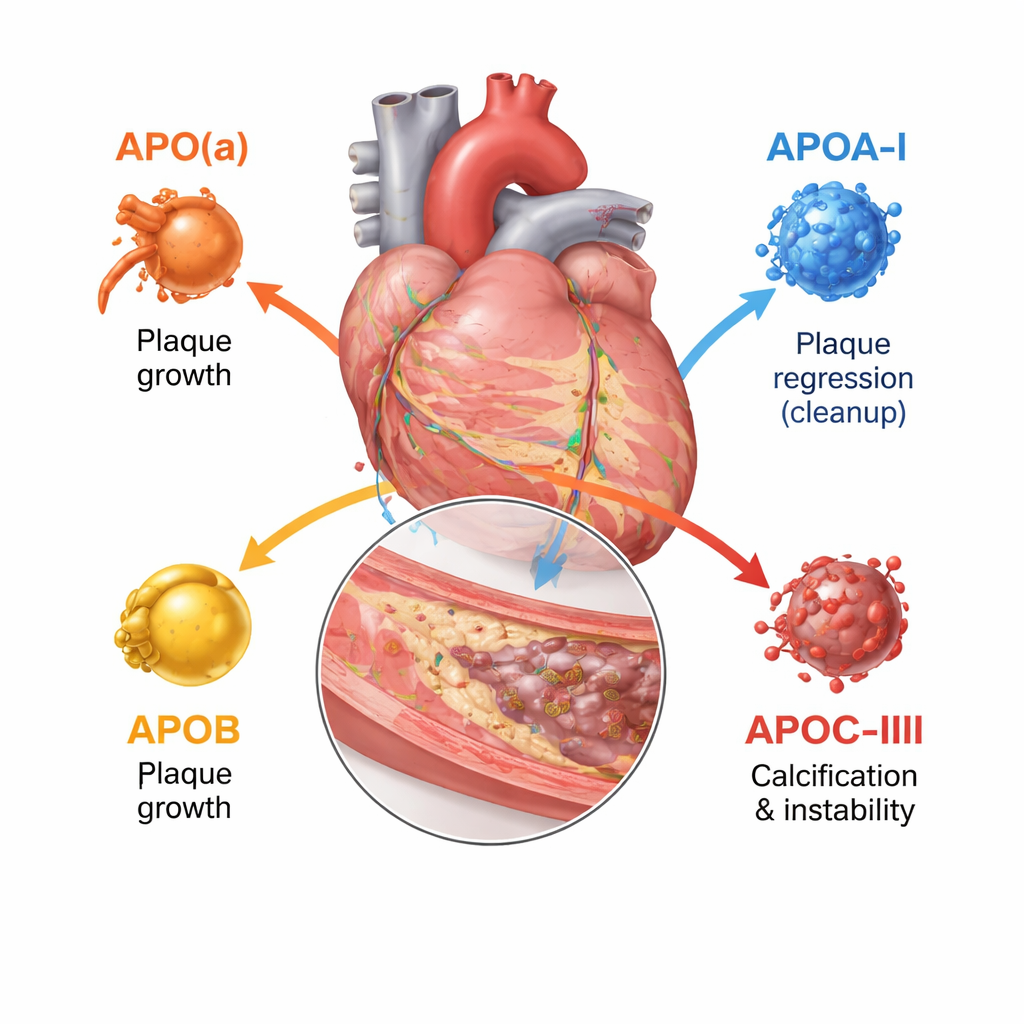
Jak cztery białka kształtują niebezpieczne blaszki
Apolipoproteina B występuje na każdej cząstce LDL i podobnych cząstkach i w praktyce odzwierciedla liczbę cząstek aterogennych — zatykających tętnice — we krwi. Im więcej cząstek niosących ApoB i im dłużej krążą, tym większe ogólne obciążenie blaszkami w tętnicach wieńcowych. Badania obrazowe wykonywane wewnątrz naczyń serca pokazują, że wyższe poziomy ApoB idą w parze z większymi blaszkami, dłuższymi zmianami, większą liczbą miękkich, martwiczych jąder i mniejszą ilością stabilizujących złogów wapnia. W przeciwieństwie do tego apolipoproteina A‑I, główne białko na HDL, pomaga usuwać cholesterol z komórek blaszek i transportować go z powrotem do wątroby. Wyższa funkcjonalna aktywność ApoA‑I i korzystny stosunek cholesterolu HDL do ApoA‑I wiążą się z wolniejszym wzrostem blaszek i większą zawartością tkanki włóknistej, bardziej stabilnej, chociaż samo podniesienie stężenia HDL w osoczu nie przełożyło się na mniejszą liczbę zdarzeń klinicznych.
Szczególne białko ryzyka i promotor stwardnienia
Apolipoproteina(a) tworzy cząstkę zwaną lipoproteiną(a), czyli Lp(a), gdy łączy się z rdzeniem podobnym do LDL. Lp(a) jest w dużej mierze zdeterminowana genetycznie i zwykle nie reaguje na dietę. Badania obrazowe przeprowadzone na tysiącach pacjentów pokazują, że osoby z wysokim poziomem Lp(a) mają więcej ogólnych blaszek, więcej obszarów o niskiej gęstości i bogatych w lipidy oraz więcej ogniskowych blaszek „wysokiego ryzyka” podatnych na pęknięcie, nawet gdy cholesterol LDL jest intensywnie leczony. Przegląd dochodzi do wniosku, że Lp(a) stanowi znaczące „pozostałe ryzyko”, którego standardowe terapie obniżające cholesterol nie eliminują w pełni. Apolipoproteina C‑III, występująca głównie na cząstkach bogatych w trójglicerydy, spowalnia ich usuwanie i pobudza stan zapalny. Osoby z wyższym poziomem ApoC‑III mają więcej wapnienia wieńcowego i bardziej złożone, zwapniałe guzki w obrębie blaszek, cechy związane z zaawansowaną chorobą i usztywnieniem naczyń.
Nowe leki celujące we właściwe mechanizmy
Ponieważ te białka precyzyjniej odzwierciedlają ryzyko niż sam cholesterol, stają się bezpośrednimi celami terapeutycznymi. W przypadku Lp(a) kilka wstrzykiwanych preparatów genetycznych — leki antysensowne i małe interferujące RNA — wstępnie redukuje poziomy o 80–95%, a doustny inhibitor montażu cząstki także wykazuje duże obniżenia. W odniesieniu do ApoC‑III niedawno zatwierdzone terapie mogą znacząco obniżyć trójglicerydy i samą ApoC‑III, a wstępne dane sugerują, że mogą zmniejszać ryzyko zapalenia trzustki i wpływać na wapnienie blaszek. 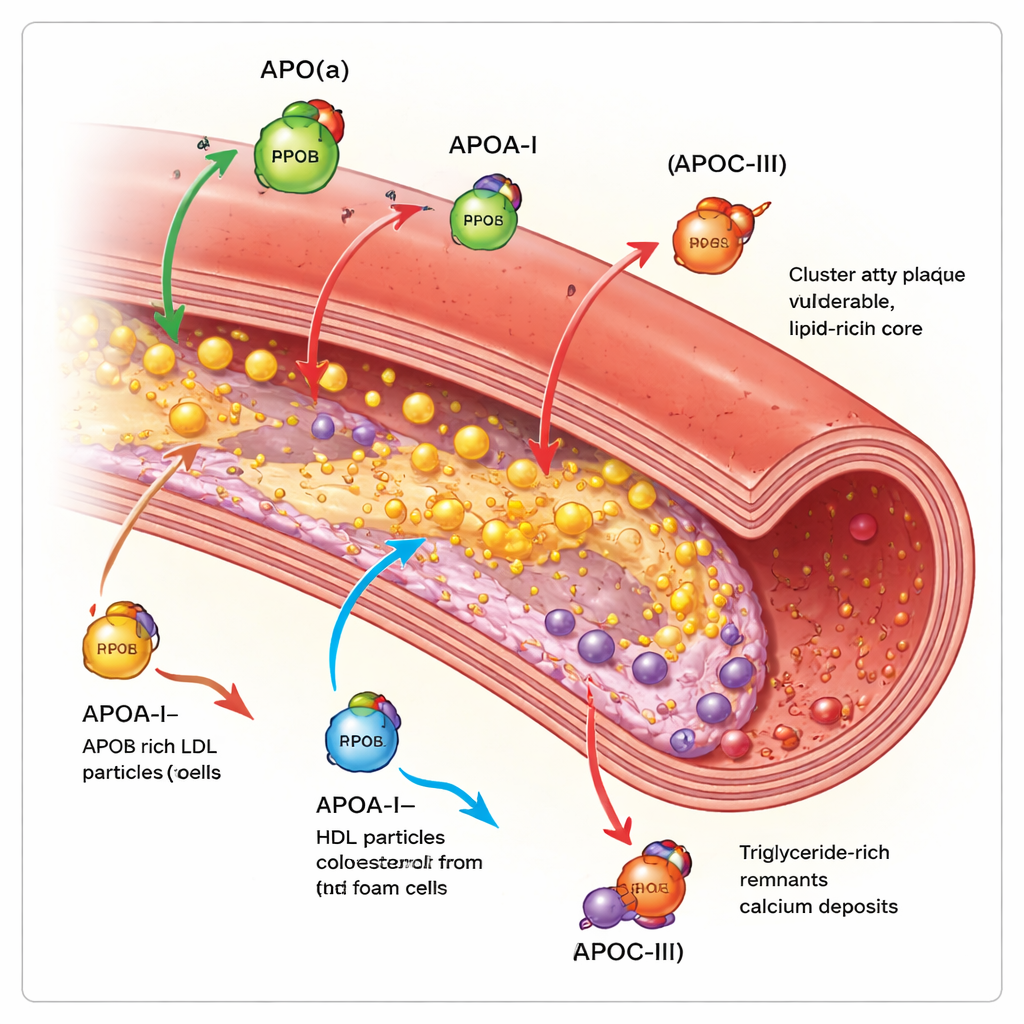
Co to oznacza dla ochrony serca
Mówiąc prosto, ten przegląd argumentuje, że to nie tylko poziomy cholesterolu decydują o tym, kto dozna zawału, lecz miks i zachowanie białkowo‑pokrytych cząstek przenoszących ten cholesterol. ApoB odzwierciedla, ile „złych” cząstek bombarduje ścianę tętnicy, ApoA‑I obrazuje system usuwania cholesterolu, Lp(a) dodaje dodatkowe, genetycznie uwarunkowane ryzyko, a ApoC‑III sprzyja stwardniałym, zapalnym blaszkom. Nowe leki celujące w redukcję Lp(a) i ApoC‑III oraz dokładniejsze stosowanie oznaczeń ApoB i ApoA‑I w rutynowych badaniach mogą pozwolić lekarzom dopasować profilaktykę do indywidualnej biologii blaszek u pacjenta, wychwytując ukryte ryzyko, które standardowe panele lipidowe pomijają.
Cytowanie: Fukase, T., Dohi, T. A narrative review of impacts of apolipoproteins on atherosclerotic coronary plaques. npj Cardiovasc Health 3, 4 (2026). https://doi.org/10.1038/s44325-026-00104-x
Słowa kluczowe: lipoproteina(a), apolipoproteina B, apolipoproteina A‑I, apolipoproteina C‑III, obrazowanie blaszek wieńcowych