Clear Sky Science · pl
Rezonans magnetyczny kombinacyjnej immunoterapii w przedklinicznym modelu raka nabłonkowego jajnika
Dlaczego to ma znaczenie dla zdrowia kobiet
Rak nabłonkowy jajnika często jest wykrywany późno i pozostaje jednym z najbardziej śmiertelnych nowotworów dotykających osoby z jajnikami. Wiele guzów nawraca nawet po operacji i chemioterapii, dlatego badacze pilnie testują nowe sposoby wspierania układu odpornościowego w walce z tą chorobą. W niniejszym badaniu przeanalizowano eksperymentalne, trzyskładnikowe leczenie i wykorzystano zaawansowane skany MRI do obserwacji w czasie rzeczywistym, jak komórki odpornościowe przemieszczają się do guzów jajnika u myszy. Praca sugeruje, że lekarze mogliby kiedyś ocenić, czy immunoterapia działa, znacznie wcześniej niż pokaże to zmniejszenie guza na obrazie.
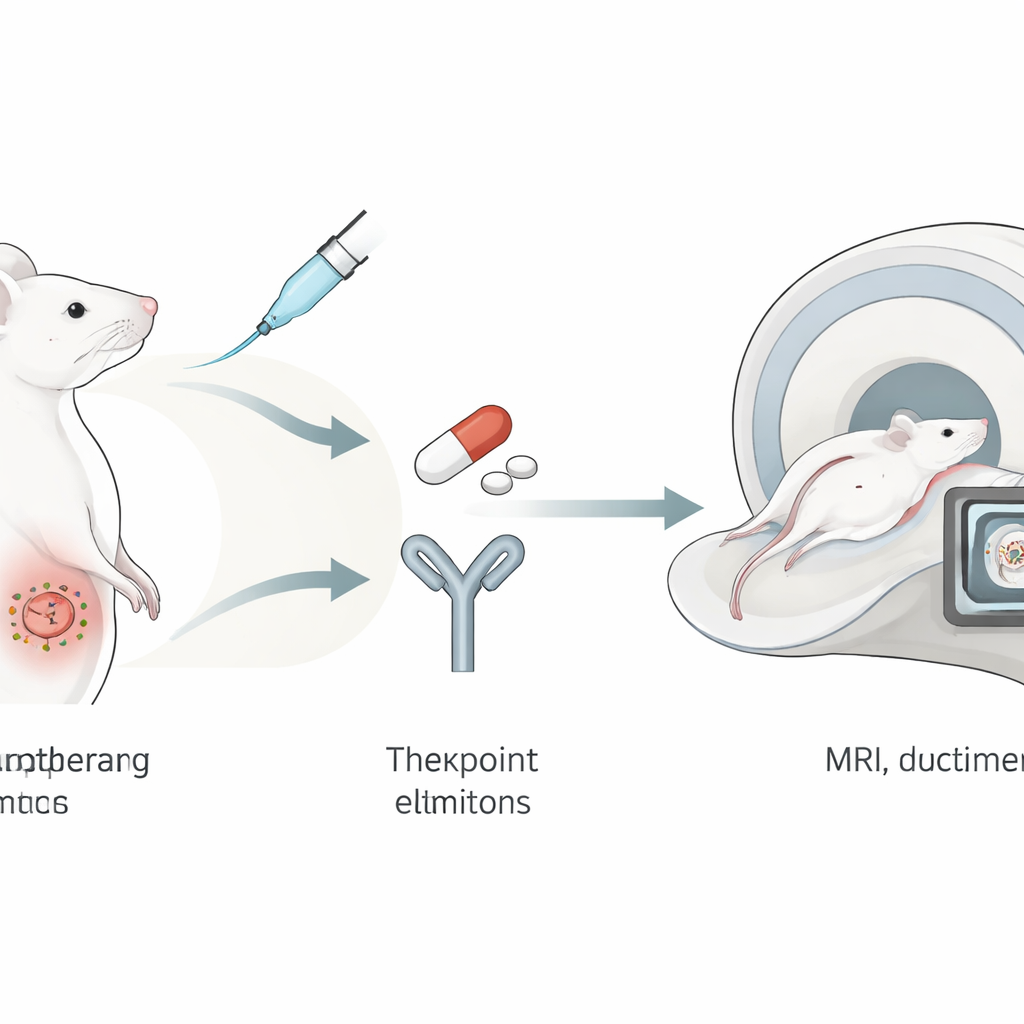
Atak trzech leków
Naukowcy przetestowali „potrójną terapię” w modelu myszy zaprojektowanym tak, by naśladować ludzki rak jajnika. Pierwszym składnikiem był DPX-Survivac, preparat przypominający szczepionkę, który uczy komórki odpornościowe rozpoznawania surviviny — białka pomagającego komórkom nowotworowym unikać samozniszczenia, obecnego w wielu guzach. Drugim był inhibitor punktu kontrolnego immunologicznego blokujący PD-1, molekularny hamulec, którego guzy często używają do wyłączania limfocytów T. Trzecim był przerywany, niski dawką podawany lek cytotoksyczny cyklofosfamid, który może zmniejszać populacje komórek supresyjnych utrudniających odpowiedź immunologiczną. Razem te środki miały uwolnić, wyszkolić i ukierunkować układ odpornościowy przeciwko guzom jajnika.
Obserwacja wzrostu i kurczenia się guzów
Ponieważ guzy jajnika rosną głęboko w ciele, trudno je monitorować bez obrazowania. W badaniu zespół użył wysokorozdzielczego MRI do pomiaru objętości guza u każdej myszy kilka tygodni po chirurgicznym wszczepieniu komórek nowotworowych na jajniku. W trzech terminach skanów guzy u leczonych myszy pozostawały mniejsze niż u zwierząt nieleczonych, a na końcowym punkcie czasowym różnica w wielkości i tempie wzrostu była statystycznie istotna. Chociaż przeżywalność w krótkim okresie badania nie różniła się, wszystkie zwierzęta musiały zostać humanitarnie uśmiercone w ustalonym czasie w celu analizy tkanek, więc długoterminowych korzyści nie dało się w pełni ocenić. Niemniej jednak wyniki obrazowania pokazują, że potrójna terapia spowolniła rozrost ustalonych guzów jajnika.
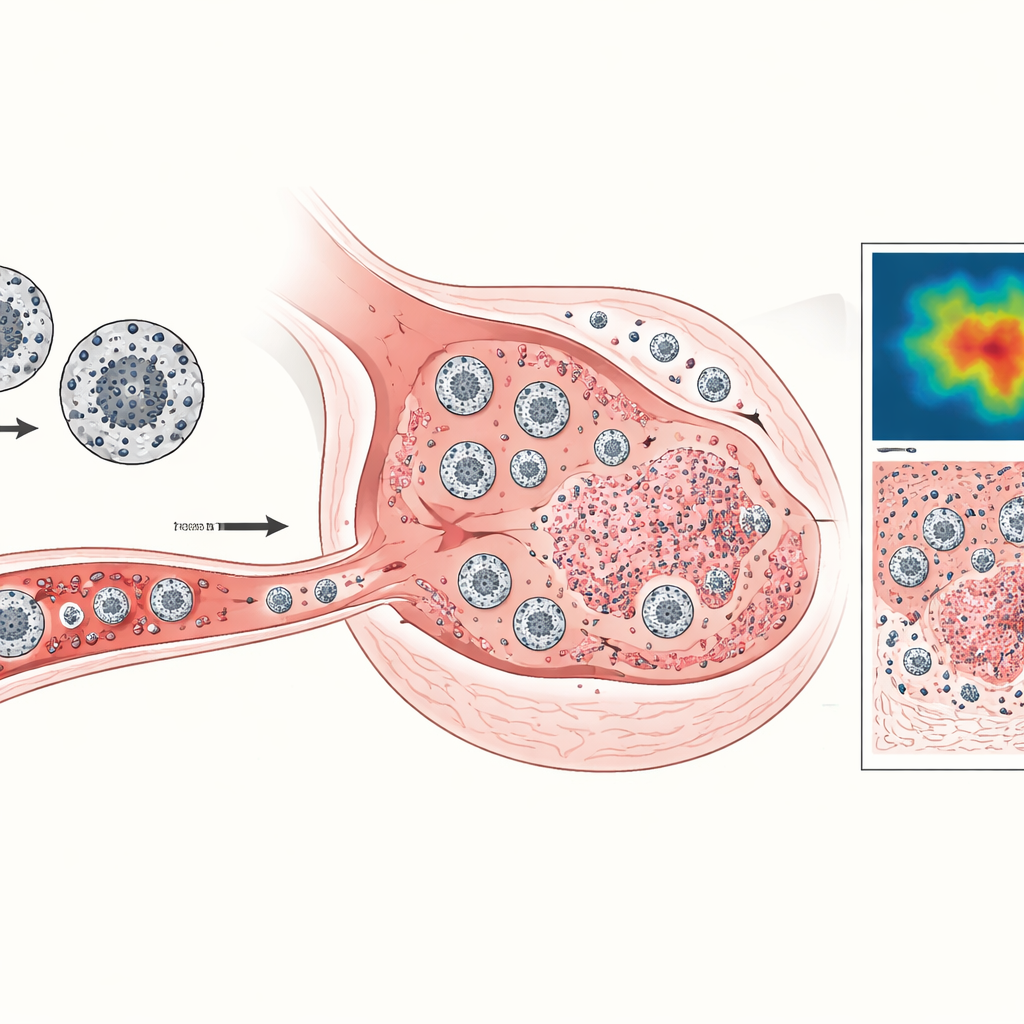
Śledzenie komórek odpornościowych za pomocą maleńkich magnesów
Ponad samym pomiarem rozmiaru guza, naukowcy chcieli sprawdzić, czy pomocne komórki odpornościowe rzeczywiście docierają do nowotworu. Pobierali dwa typy komórek odpornościowych od dawców: cytotoksyczne limfocyty T, które mogą bezpośrednio zabijać komórki nowotworowe, oraz szerszą grupę komórek mieloidalnych, które mogą wspierać lub hamować ataki immunologiczne. Te komórki naładowano nadparamagnetycznymi nanopartikami tlenku żelaza — w praktyce maleńkimi magnesami — i wprowadzono do myszy z guzami. Specjalizowana metoda MRI zwana TurboSPI następnie uwidoczniła miejsca, w których zgromadziły się komórki bogate w żelazo. Porównując sygnał MRI ze starannie skalibrowanymi wzorcami, zespół oszacował, ile znakowanych komórek zajmowało każdy milimetr sześcienny tkanki guza lub węzła chłonnego w różnych momentach.
Ruch komórek odpornościowych w guzach i węzłach chłonnych
Obrazowanie wykazało, że leczone myszy rekrutowały znacznie więcej żelazoznakowanych zabójczych limfocytów T do swoich guzów niż myszy nieleczone, szczególnie w późniejszych punktach czasowych, gdy guzy w grupie kontrolnej szybko rosły i często zawierały prawie żadnych wykrywalnych limfocytów T. Komórki mieloidalne również pojawiały się częściej w guzach zwierząt leczonych, choć ich dokładna rola — korzystna czy szkodliwa — pozostaje do wyjaśnienia. Zespół dokładnie przyjrzał się pachwinowym węzłom chłonnym, małym centrom odpornościowym odprowadzającym chłonkę albo z guza, albo z miejsca wstrzyknięcia szczepionki. U leczonych myszy węzeł odprowadzający DPX-Survivac konsekwentnie puchł bardziej niż węzeł odprowadzający guz, a to powiększenie wiązało się z mniejszymi rozmiarami guzów, co sugeruje silną aktywację odpornościową w odpowiedzi na szczepionkę. Badania cytometrii przepływowej na tkankach guza i płynie w jamie brzusznej potwierdziły, że leczenie zmieniało proporcje komórek odpornościowych, zmniejszając niektóre populacje supresyjne lub towarzyszące i zwiększając ogólny udział komórek odpornościowych w płynie, w którym unoszą się wolne komórki nowotworowe mogące się rozprzestrzeniać.
Co to może znaczyć dla przyszłej opieki
Podsumowując, badanie pokazuje, że ta trójskładnikowa immunoterapia może spowalniać wzrost guzów jajnika u myszy i wydaje się robić to poprzez przyciąganie większej liczby niszczących guzy limfocytów T do nowotworu oraz stymulację aktywności odpornościowej w pobliskich węzłach chłonnych. Równie ważne, demonstruje, że MRI można wykorzystać nie tylko do pomiaru rozmiaru guzów, ale także do śledzenia wędrówki terapeutycznych komórek odpornościowych w całym organizmie. Jeśli podobne techniki dałoby się zaadaptować u ludzi, lekarze mogliby kiedyś używać nieinwazyjnych skanów, aby wcześnie stwierdzić, czy złożona immunoterapia przyciąga właściwe komórki we właściwe miejsce, co pozwoliłoby precyzyjniej dostosowywać leczenie pacjentek z rakiem jajnika.
Cytowanie: Gosse, J.T., Skelton, C.S., Tremblay, ML. et al. MRI of combination immunotherapy in an epithelial ovarian cancer preclinical model. npj Imaging 4, 25 (2026). https://doi.org/10.1038/s44303-026-00157-8
Słowa kluczowe: rak jajnika, immunoterapia, śledzenie komórek za pomocą MRI, szczepionka przeciwnowotworowa, inhibitor punktu kontrolnego