Clear Sky Science · pl
Skorelowane obrazowanie multimodalne do mikroskalowego mapowania przestrzennego interakcji aktywności genów kolagenu w ludzkich tkankach
Dlaczego warto zajrzeć do wnętrza mięśni
Choroby, które stopniowo bliznują nasze organy, jak dystrofia mięśniowa Duchenne’a (DMD), rozwijają się na skalach zbyt małych, by dostrzec je gołym okiem. Aktywność genów zachodzi w pojedynczych komórkach, a otaczająca je tkanka podporowa składa się z cienkich włókien białkowych. Do tej pory naukowcom rzadko udawało się oglądać te dwa światy jednocześnie na tej samej cienkiej warstwie ludzkiej tkanki. W tym badaniu przedstawiono metodę, która pozwala to zrobić, ukazując, jak sygnały genów i strukturalne rusztowanie organizmu wchodzą w interakcje na poziomie mikroskopowym.
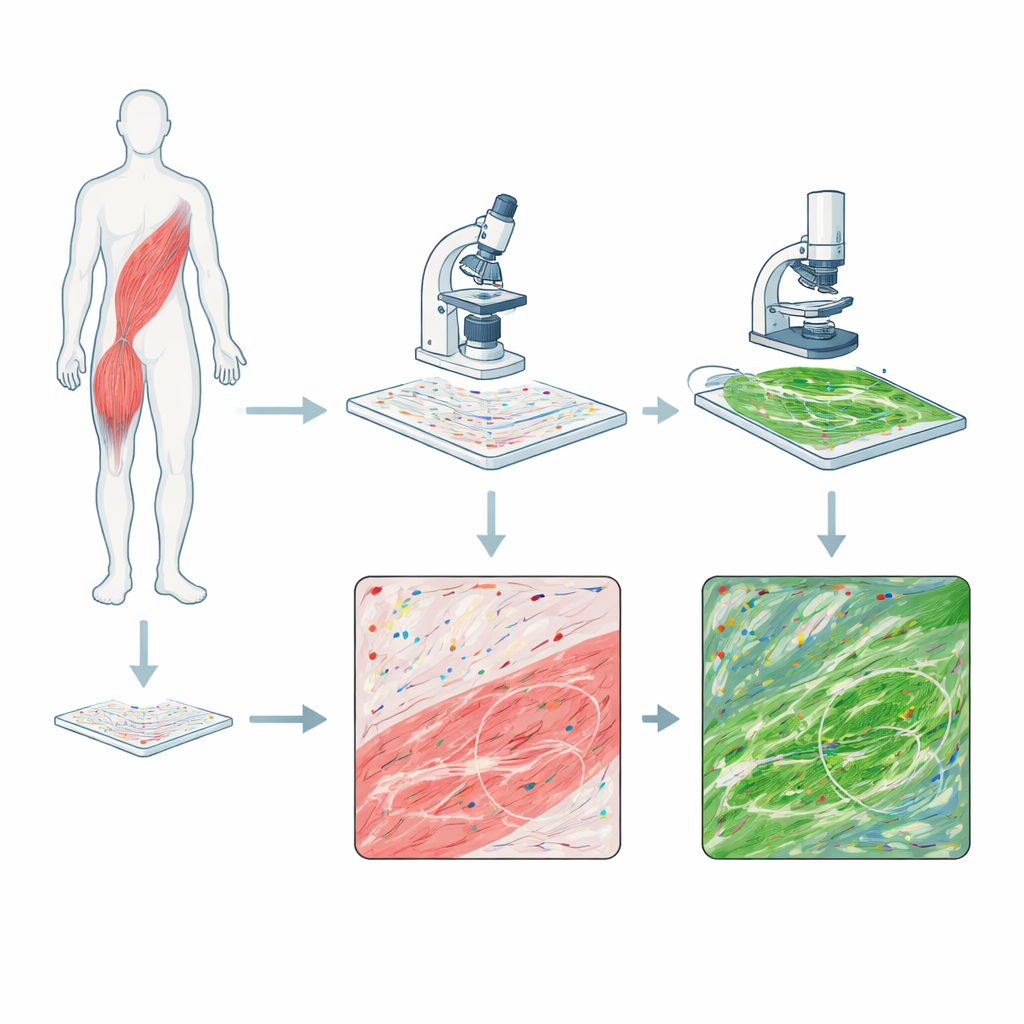
Dwie „kamery” na tym samym kawałku tkanki
Naukowcy połączyli dwie zaawansowane metody obrazowania na pojedynczych przekrojach biopsji mięśni szkieletowych od osób z DMD oraz od zdrowego ochotnika. Jedna metoda, RNAscope, barwi pojedyncze cząsteczki RNA — robocze kopie genów — jako kolorowe kropki, pokazując miejsca lokalizacji określonych komunikatów genetycznych. Druga metoda, mikroskopia multiphotonowa, wykorzystuje światło lasera, by sprawić, że włókna kolagenu w tkance świecą bez dodatku barwnika, rejestrując architekturę tkanki łącznej, która gęstnieje podczas bliznowacenia i włóknienia. Najpierw obrazując sygnały RNA, a następnie sygnały kolagenu na tej samej szkiełku, mogli wyrównać oba obrazy tak, by każdą kropkę aktywności genowej porównać z otaczającą siecią włókien, piksel po pikselu.
Co mówią osobne obrazy
Oglądanie każdej z metod osobno już uwydatniło wyraźne różnice między mięśniem chorobowym a zdrowym. RNAscope wykazało, że mięśnie od pacjentów z DMD zawierały mniej transkryptów dystrofiny — cząstek RNA potrzebnych do wytworzenia brakującego białka dystrofiny — niż próbka zdrowa. Pozostałe sygnały różniły się też wielkością w zależności od tego, która część genu była celowana, co sugeruje różnice w przetwarzaniu długiego komunikatu dystrofinowego. Tymczasem obrazy multiphotonowe pokazały, że mięśnie DMD były wypełnione długimi, gęstymi włóknami kolagenu — wizualny znak bliznowacenia włóknistego — podczas gdy mięsień zdrowy miał mniej włókien, bardziej równomiernie rozłożonych. Te obserwacje zgadzają się z doświadczeniem klinicznym: w DMD tkanka mięśniowa stopniowo zastępowana jest tłuszczem i bliznami.
Oddalając widok: szerokie wzorce w tkance
Po cyfrowym zarejestrowaniu obu rodzajów obrazów zespół podzielił każdy przekrój tkanki na siatkę, traktując każde pole jako małą dzielnicę. W każdym kwadracie mierzyli zarówno cechy kolagenu — długość włókien, orientację i to, czy włókna są skręcone czy proste — jak i lokalną gęstość kropek RNA dystrofiny. Ten widok w postaci „mapy cieplnej” ujawnił łaciate, regionalne zróżnicowanie zarówno aktywności genów, jak i struktury kolagenowej w mięśniach DMD. Jednak gdy te miary porównano testami statystycznymi, obfitość transkryptów i właściwości kolagenu nie wykazały niemal żadnej spójnej korelacji na tej grubej skali. Innymi słowy, przy uśrednianiu na dość dużych obszarach, rejony bogate w RNA dystrofiny nie były konsekwentnie bardziej ani mniej włókniste niż rejony z mniejszą liczbą sygnałów RNA.
Przybliżając: relacje w skali komórkowej
Najciekawsze wyniki pojawiły się, gdy naukowcy skupili się na „sąsiedztwach” mierzących zaledwie kilka dziesiątek mikrometrów — mniej więcej rozmiaru pojedynczych włókien mięśniowych i ich bezpośredniego otoczenia. Dla każdej kropki RNA narysowali serię rosnących okręgów i pytali, ile włókien kolagenu znajduje się w ich obrębie oraz jak długie są te włókna. Zarówno w tkankach DMD, jak i zdrowych, włókna kolagenu były najdłuższe tuż obok sygnałów RNA dystrofiny i stopniowo skracały się wraz ze wzrostem odległości. W najbardziej silnie zbliznowaciałych próbkach kropki transkryptów niemal zawsze miały kolagen w pobliżu, nawet na bardzo małych odległościach, podczas gdy w próbce zdrowej wiele kropek RNA znajdowało się w obszarach z niewielką lub żadną ilością pobliskiego kolagenu. Analizy kontrolne z użyciem losowo rozmieszczonych punktów i nieco zmodyfikowanych ustawień przetwarzania obrazu wykazały, że ten wzorzec nie mógł być wyjaśniony jedynie przypadkiem ani anomaliami oprogramowania.
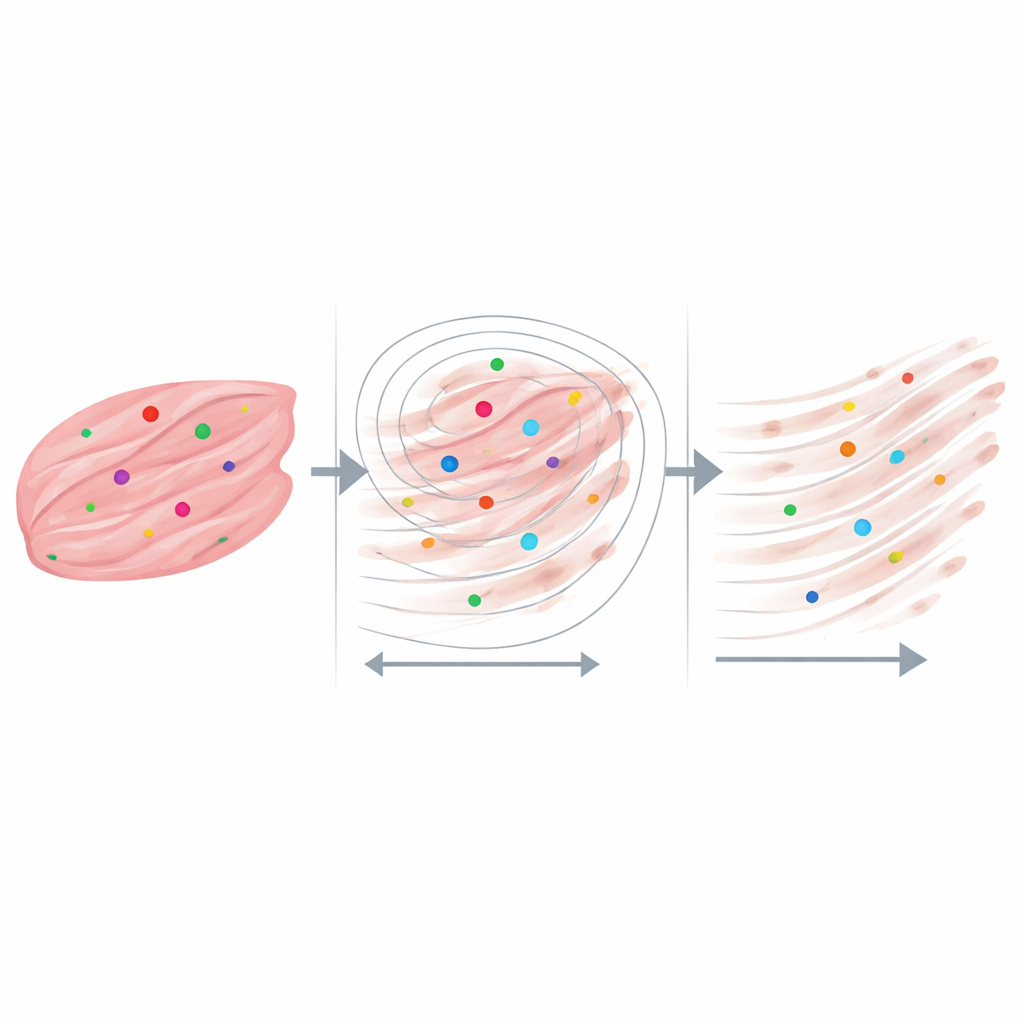
Co to może oznaczać dla chorób mięśni i nie tylko
Wyniki te sugerują, że istotne powiązania między komunikatami genowymi a strukturą tkanki mogą być ukryte przy patrzeniu jedynie na duże uśrednienia, lecz stają się widoczne przy badaniu na poziomie komórkowym. W tym badaniu dowodowym regiony bogate w określone transkrypty dystrofiny miały tendencję do lokalizowania się w pobliżu dłuższych, gęstszych włókien kolagenu, co sugeruje, że lokalna aktywność genowa i włóknista przebudowa mogą wzajemnie się wpływać w małych mikrośrodowiskach mięśniowych. Autorzy podkreślają, że grupa pacjentów jest niewielka i praca nie stanowi jeszcze testu klinicznego. Zamiast tego przedstawiają elastyczną platformę, którą można rozszerzyć na inne geny, typy tkanek i metody obrazowania. Łącząc informacje o tym, gdzie geny są aktywne, z informacją o tym, jak zbudowane jest tkankowe rusztowanie, podejście to otwiera drogę do odkrywania nowych przestrzennych biomarkerów włóknienia, regeneracji i odpowiedzi na pojawiające się terapie oparte na RNA.
Cytowanie: Scodellaro, R., Mietto, M., Ferlini, A. et al. Correlative multimodal imaging for microscale spatial mapping of collagen-gene activity interactions in human tissues. npj Imaging 4, 17 (2026). https://doi.org/10.1038/s44303-026-00149-8
Słowa kluczowe: obrazowanie multimodalne, miopatia Duchenne’a (DMD), zwłóknienie kolagenowe, przestrzenna ekspresja genów, biopsja mięśnia szkieletowego