Clear Sky Science · pl
Jednokrokowa strategia znakowania radiacyjnego dla PET, SPECT i terapeutycznych radioizotopów z użyciem nanopartikelów jako uniwersalnego chelatora
Dlaczego małe cząstki radioaktywne mają znaczenie
Współczesna opieka onkologiczna coraz częściej polega na lokalizowaniu i leczeniu guzów za pomocą radioaktywnych leków, które uwidaczniają je w skanach i w niektórych przypadkach niszczą je od środka. Tworzenie każdego nowego radioaktywnego leku jest jednak powolne i kłopotliwe, ponieważ większość konstrukcji musi być zaprojektowana pod konkretny metal radioaktywny. W tej pracy badacze proponują zupełnie inne podejście: użycie jednego rodzaju nanopartikelów na bazie żelaza jako „uniwersalnego gniazda”, które może przyjmować różne izotopy medyczne do obrazowania i terapii, co potencjalnie przyspiesza opracowywanie i dopracowywanie takich leków.
Od wielu kluczy do jednego zamka
Obecne radioaktywne leki zwykle opierają się na chemicznych „szponach” zwanych chelatorami, które chwytają atomy metali i łączą je z przeciwciałami lub innymi cząstkami celującymi. Każdy metal radioaktywny wymaga zazwyczaj własnego chelatora i własnej receptury — warunki takie jak temperatura, kwasowość i czas reakcji ulegają zmianie. Dla niektórych ważnych medycznie metali, zwłaszcza tych stosowanych w silnych terapiach alfa, wciąż brak idealnego chelatora. Autorzy twierdzą, że podejście „metal po metalu” stało się wąskim gardłem: lista użytecznych izotopów rośnie, ale chemia pozwalająca nimi bezpiecznie operować nie nadąża.
Nanocząstki jako uniwersalne gniazdo
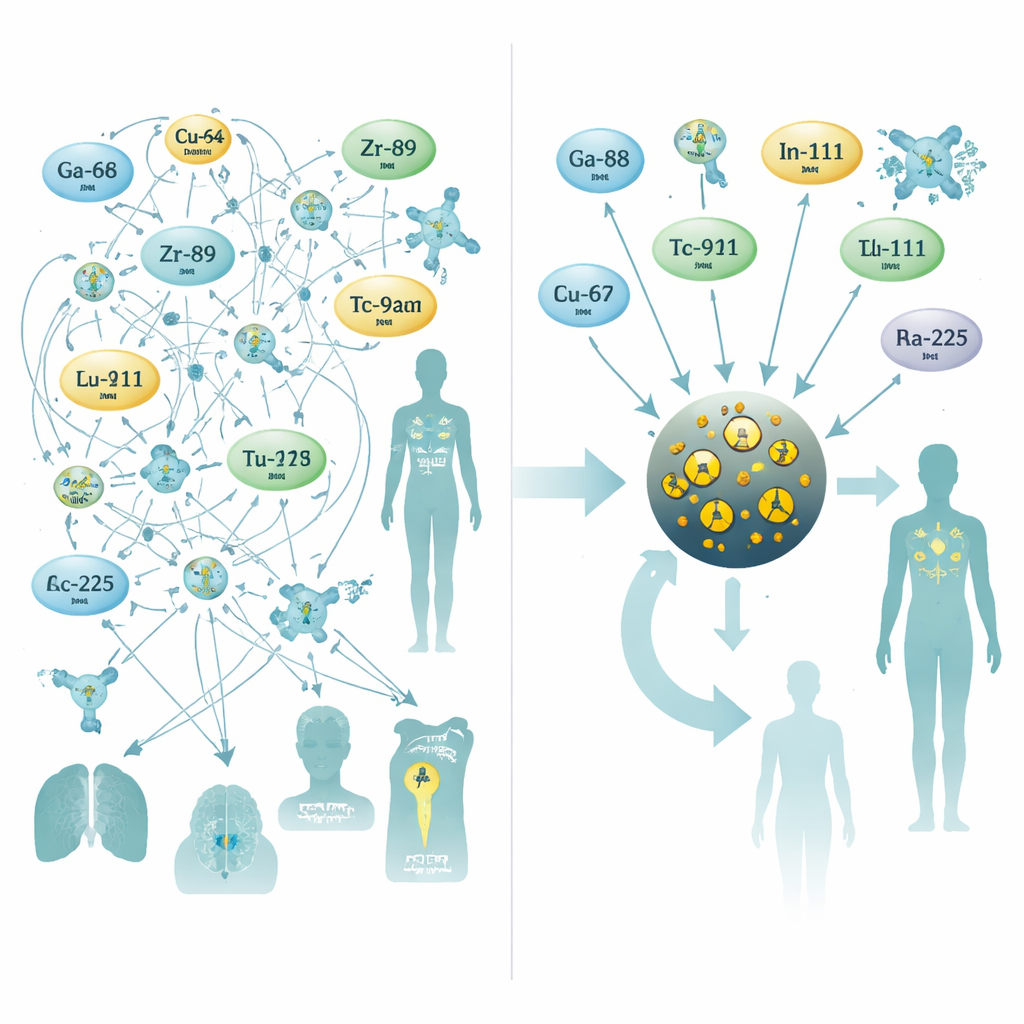
Aby to rozwiązać, badacze zwrócili się ku bardzo małym nanocząstkom tlenku żelaza, materiałowi już badanym jako kontrast do MRI. Zaprojektowali cząstki z rdzeniem z tlenku żelaza o średnicy około trzech nanometrów, otoczonym powłoką z cytrynianu, która zapewnia im stabilność we krwi. W trakcie jednego, 10‑minutowego etapu syntezy wspomaganej mikrofalami, domieszkowali rdzeń jednym z dziesięciu różnych radioaktywnych metali powszechnie używanych w PET, SPECT lub terapii wewnętrznej. Ten proces „w jednym naczyniu” dał cząstki o stałym rozmiarze i wysokich wydajnościach oraz, co kluczowe, doskonałej stabilności w surowicy ludzkiej — nawet dla trudnych izotopów terapeutycznych, takich jak rad-223 i aktyn-225, których produkty rozpadu często wydostają się z tradycyjnych chelatorów.
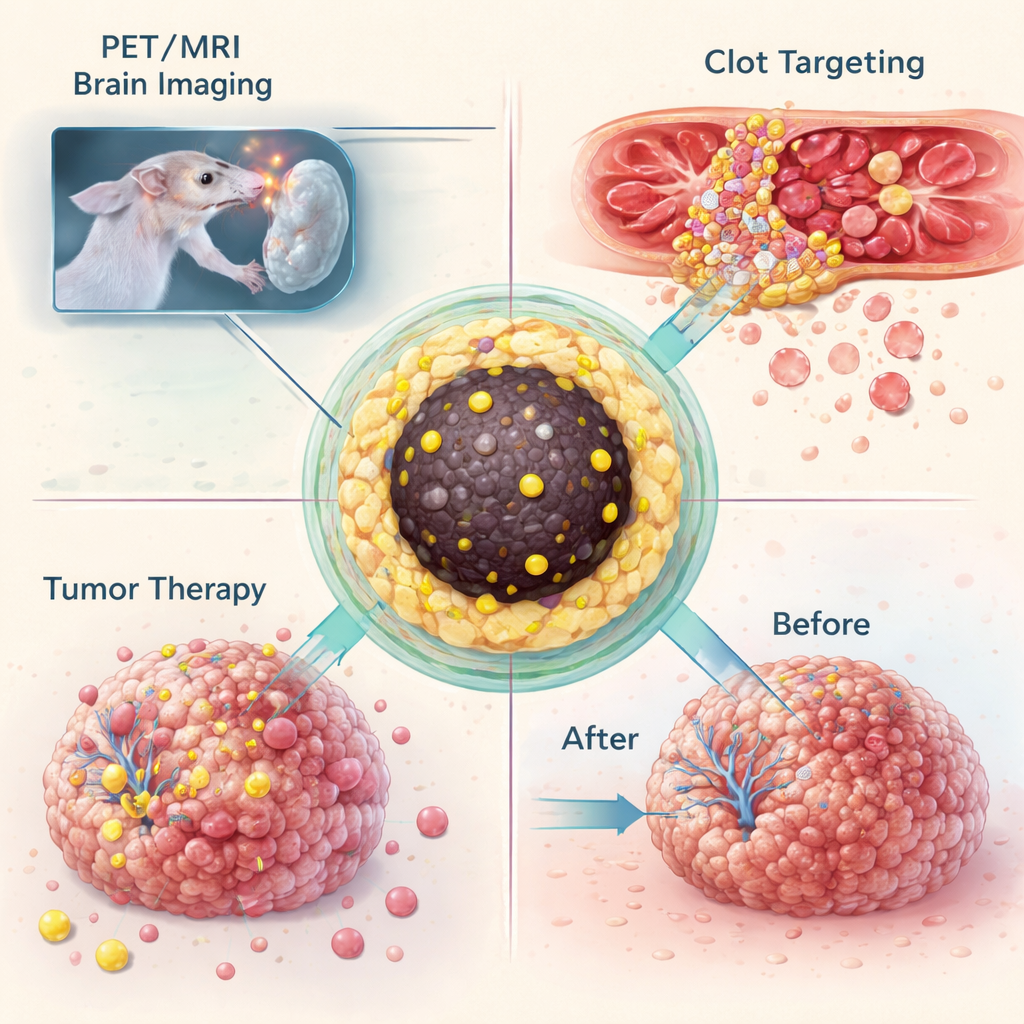
Obrazowanie skrzepów i guzów mózgu
Pokazawszy, że mogą zamykać wiele różnych izotopów w tej samej konstrukcji nanocząstki, zespół przetestował, co te „nanotracery” potrafią u żywych zwierząt. W modelu myszy z glejakiem, śmiertelnym guzem mózgu, cząstki znakowane galem‑68 wstrzyknięto do krwiobiegu i obrazowano za pomocą połączonego PET i MRI. Cząstki kumulowały się w guzach na tyle dużych, by naruszyć barierę krew–mózg, co pozwoliło tej samej formulacji zapewnić jednocześnie wyraźny kontrast w MRI i czuły sygnał PET. W innym eksperymencie cząstki zmodyfikowano chemicznie, by mogły się połączyć, za pomocą wysoce selektywnej reakcji „click”, z przeciwciałem celującym w aktywowane płytki krwi wewnątrz skrzepów. U myszy z uszkodzoną tętnicą szyjną ta dwuetapowa strategia „pretargetingu” dała wyraźne sygnały PET w miejscu skrzepu, podczas gdy zwierzęta kontrolne nie wykazały takiego ogniska.
Od diagnozy po leczenie i bezpieczniejsze wydalanie
Ta sama platforma posłużyła również do dostarczania terapii. Gdy nanocząstki z lutetem‑177 wstrzyknięto bezpośrednio do guzów glejaka u myszy, cząstki pozostawały w dużej mierze skoncentrowane w masie guza przez co najmniej dwa tygodnie. W tym czasie nieleczone guzy urastały do kilku razy swojej pierwotnej wielkości, podczas gdy guzy leczone przestały rosnąć, co sugeruje, że zlokalizowana dawka promieniowania była wystarczająca do zatrzymania progresji. Zdając sobie sprawę, że powtarzane zabiegi mogłyby przeciążyć wątrobę i śledzionę żelazem, zespół zmodyfikował warunki syntezy, tworząc jeszcze mniejsze cząstki — około czterech do pięciu nanometrów — które są wystarczająco małe, by mogły być filtrowane przez nerki. Te skurczone cząstki wciąż pewnie trzymały ładunek radioaktywny, ale były szybko wydalane do pęcherza, zmniejszając długoterminowe kumulowanie w głównych narządach.
Co to może znaczyć dla przyszłej opieki onkologicznej
Dla osób niebędących specjalistami kluczowa wiadomość jest taka, że badacze stworzyli jedną, elastyczną platformę nanocząsteczkową, którą można łączyć z wieloma różnymi metalami radioaktywnymi bez konieczności za każdym razem wymyślania chemii od nowa. W modelach zwierzęcych ta sama podstawowa cząstka może pomagać wykrywać guzy mózgu, uwidaczniać skrzepy, dostarczać promieniowanie bezpośrednio do guzów, a nawet być dostrojona tak, by opuszczać organizm przez nerki. Choć przed wprowadzeniem tej metody do pacjentów potrzeba jeszcze badań, oferuje ona obiecującą ścieżkę do projektowania rodzin środków diagnostycznych i terapeutycznych o wspólnym zachowaniu w organizmie, różniących się jedynie rodzajem przenoszonego promieniowania. Taka spójność może uprościć rozwój, poprawić testy bezpieczeństwa i ostatecznie uczynić zaawansowane narzędzia medycyny nuklearnej szerzej dostępnymi.
Cytowanie: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
Słowa kluczowe: radiotheranostyka, nanocząstki, obrazowanie PET, glejak, celowana radioterapia