Clear Sky Science · pl
Przyspieszona i zlokalizowana synukleinopatia w hybrydowym modelu myszy: implikacje dla badań z użyciem pozytonowej tomografii emisyjnej
Dlaczego te badania są ważne
Choroba Parkinsona jest najbardziej znana z drżeń i problemów z poruszaniem się, ale głęboko w mózgu zaczyna się od drobnych zmian, które trudno dostrzec. Lekarze pilnie potrzebują metod wykrywania tych zmian wcześnie oraz narzędzi do szybkiego testowania nowych leków. To badanie opisuje udoskonalony model myszy, który odtwarza kluczowe cechy uszkodzeń mózgu podobnych do Parkinsona w ciągu zaledwie kilku tygodni i w bardzo określonym obszarze mózgu, dostosowanym do zastosowania z zaawansowanymi badaniami obrazowymi zwanymi PET. 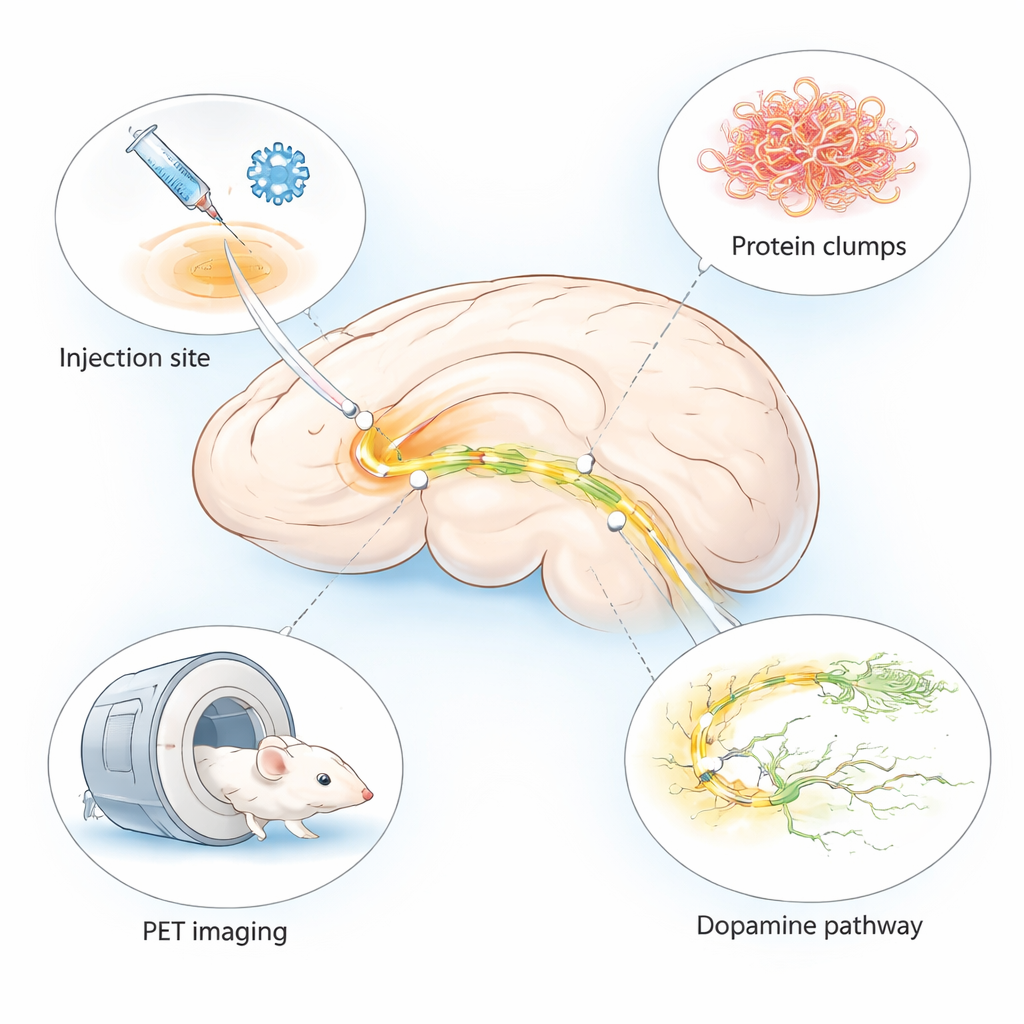
Budowanie szybszego, bardziej skoncentrowanego modelu choroby
Wiele istniejących modeli zwierzęcych choroby Parkinsona potrzebuje miesięcy, by rozwinąć objawy, albo nie odtwarza pełnego zakresu zmian mózgowych obserwowanych u pacjentów. Autorzy połączyli dwa sprawdzone podejścia w jeden „hybrydowy” model. Wstrzyknęli niegroźnego wirusa powodującego, że komórki mózgu produkują ludzką alfa‑synukleinę — białko, które tworzy grudki w Parkinsonie — razem z uprzednio uformowanymi fibrylami, które działają jak zarodniki prowokujące dalsze agregowanie. Oba preparaty podano do małego, związanego z ruchem obszaru zwanego istotą czarną po jednej stronie mózgu myszy. Ten układ wywołuje miejscowe, ale intensywne zmiany przypominające chorobę po stronie wstrzykniętej, podczas gdy przeciwna strona pozostaje stosunkowo zdrowa do porównania.
Śledzenie grudek białkowych i obumierających komórek nerwowych
Już po zaledwie dwóch tygodniach od wstrzyknięcia myszy wykazywały wysokie poziomy ludzkiej alfa‑synukleiny i jej nieprawidłowej, fosforylowanej formy w docelowym obszarze mózgu. Pod mikroskopem badacze zaobserwowali struktury przypominające ciała Lewy’ego i neuryty Lewy’ego, które są znakami rozpoznawczymi choroby Parkinsona. W ciągu kolejnych kilku tygodni te nieprawidłowe depozyty nasilały się. Równocześnie komórki nerwowe produkujące dopaminę — kluczową dla płynności ruchu — zaczęły zanikać. Markery tych komórek spadły do około 60 procent poziomu widocznego po stronie nienaruszonej do piątego tygodnia, potwierdzając wyraźną, postępującą utratę systemu dopaminergicznego.
Zapalenie, zanik synaps i osłabione „elektrownie”
Komórki odpornościowe mózgu, zwane mikroglejem, również przeszły w silnie aktywny, zapalny stan wokół uszkodzonego obszaru. Barwienia kilku białek związanych z zapaleniem były znacznie silniejsze w pobliżu złogów alfa‑synukleiny niż po przeciwnej stronie mózgu. Później zespół wykrył utratę synaps — tych drobnych punktów kontaktu, gdzie komórki nerwowe się komunikują — oraz oznaki, że mitochondria, „elektrownie” komórek, nie działają poprawnie. Razem te ustalenia pokazują, że model nie tylko generuje grudki białkowe; odzwierciedla też reakcję łańcuchową zapalenia, nieudanego połączenia i problemów z energią, które przyczyniają się do śmierci komórek nerwowych w chorobie Parkinsona. 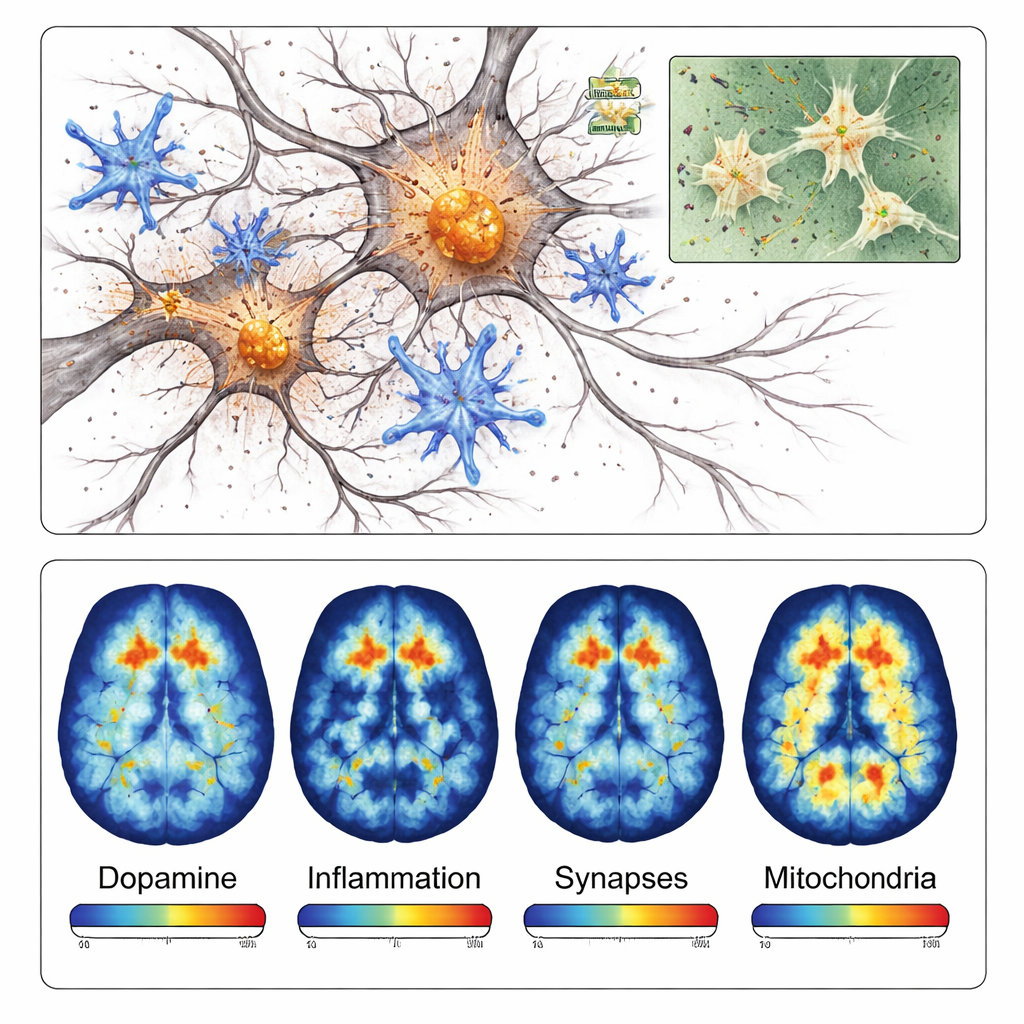
Wykorzystanie skanerów PET
Ponieważ ten model jest zlokalizowany i rozwija się szybko, jest szczególnie dobrze dopasowany do pozytonowej tomografii emisyjnej (PET), techniki obrazowania mierzącej określone cząsteczki w żywych mózgach. Badacze przetestowali cztery różne znaczniki PET, które wiążą się z zakończeniami nerwów dopaminergicznych, zapalnym mikroglejem, białkami synaptycznymi i enzymami mitochondrialnymi. W każdym przypadku skany PET wykazały niższe lub wyższe sygnały po stronie wstrzykniętej w sposób zgodny z obserwacjami mikroskopowymi. Na przykład znacznik ukierunkowany na szlaki dopaminowe wykazał około 40 procent mniej sygnału po stronie uszkodzonej, podczas gdy znacznik zapalny pokazał ponad 40 procent wyższy sygnał w dotkniętym obszarze.
Co to oznacza dla pacjentów i przyszłych terapii
Ten nowy model myszy łączy w krótkim czasie wiele kluczowych zmian, które u ludzi z chorobą Parkinsona rozwijają się przez lata. Ponieważ uszkodzenie jest ograniczone do małego, dobrze zdefiniowanego obszaru i można je śledzić za pomocą skanów PET, badacze mogą skuteczniej testować nowe znaczniki obrazowania i potencjalne terapie. Choć żadna mysz nie odwzoruje w pełni ludzkiego schorzenia, to podejście oferuje potężne, praktyczne narzędzie do zmniejszania dystansu między pracami podstawowymi a badaniami u ludzi, ostatecznie pomagając udoskonalić diagnostykę i przyspieszyć poszukiwanie lepszych terapii.
Cytowanie: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
Słowa kluczowe: choroba Parkinsona, alfa-synukleina, synukleinopatia, obrazowanie PET, model myszy