Clear Sky Science · pl
Modele równań różniczkowych zwyczajnych opisujące dynamikę replikacji SARS-CoV-2 i skuteczność leków przeciwwirusowych
Dlaczego liczby mają znaczenie przy nowym wirusie
Gdy pojawił się COVID-19, lekarze widzieli, jakie skutki wirus wywołuje u pacjentów, ale trudno było przewidzieć, kto poważnie zachoruje lub kiedy lek należy podać, by przyniósł największą korzyść. Artykuł przeglądowy opisuje, jak badacze przekształcili pomiary wirusa pochodzące od pacjentów, zwierząt i hodowli komórkowych w matematyczne „filmy” infekcji wewnątrz organizmu. Modele te wykorzystują równania do śledzenia wzrostu wirusa, reakcji komórek i układu odpornościowego oraz tego, jak leki przeciwwirusowe i szczepionki mogą przechylić szalę na naszą korzyść.
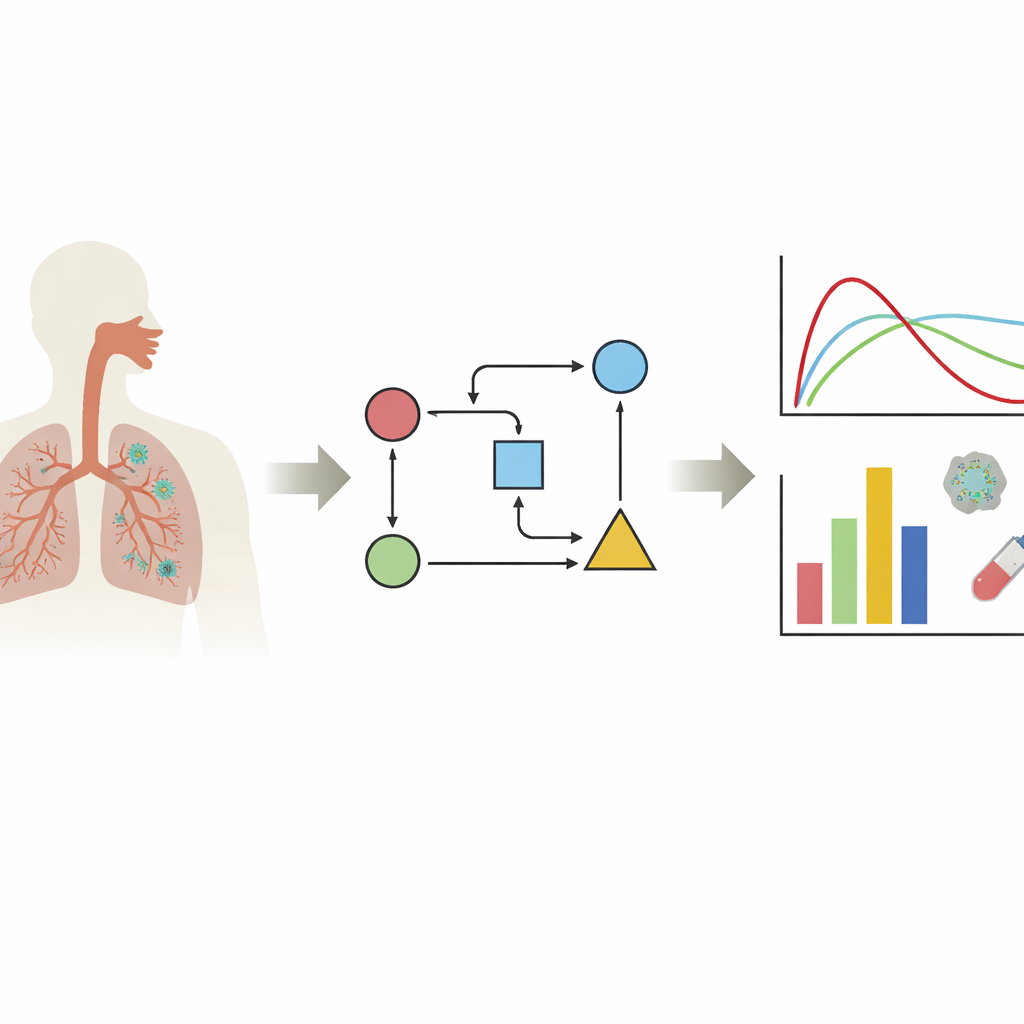
Śledzenie wirusa wewnątrz organizmu
Autorzy koncentrują się na rodzinie modeli zwanych modelami ograniczonymi przez komórki docelowe. Mówiąc prościej, modele te śledzą trzy główne elementy: zdrowe komórki podatne na zakażenie, komórki już zakażone oraz wolne cząstki wirusa. Wprowadzając do tych równań rzeczywiste dane o poziomach wirusa, badacze mogą oszacować ukryte cechy infekcji: jak szybko wirus zakaża komórki, jak długo zakażona komórka produkuje wirusa oraz jak szybko wirus jest eliminowany. Przegląd pokazuje, że większość badań skupia się na tkankach najistotniejszych dla COVID-19 — nosie oraz górnych i dolnych drogach oddechowych — podczas gdy tylko niewiele modeli bada inne organy. Jednym z kluczowych wniosków jest to, że zachowanie wirusa może wyglądać bardzo różnie w zależności od tkanki, wariantu wirusa i linii komórkowej użytej w laboratorium, dlatego nie istnieje jeden „typowy” przebieg infekcji.
Co uczymy się o układzie odpornościowym
Wiele modeli dodaje warstwy reprezentujące wczesne mechanizmy obronne układu odpornościowego oraz jego wolniejszą, bardziej ukierunkowaną odpowiedź. Badania skupione na pierwszej linii obrony sugerują, że szybka, odpowiednio skoordynowana aktywność komórek odporności wrodzonej i cząsteczek sygnałowych może stłumić infekcję, ale rzadko samodzielnie ją całkowicie usuwa. Inne prace podkreślają kluczową rolę komórek T i przeciwciał w ostatecznym opanowaniu wirusa. Modele te oddają także mroczniejszy aspekt: jeśli ukierunkowana odpowiedź immunologiczna pojawi się zbyt późno lub będzie niewłaściwie skierowana, te same mechanizmy, które powinny nas chronić, mogą napędzać szkodliwe „burze cytokinowe”, w których nadmiar sygnałów zapalnych uszkadza zdrowe tkanki. W symulacjach delikatna równowaga między działaniem pomocnym a szkodliwym często decyduje, czy choroba pozostanie łagodna, czy stanie się zagrażająca życiu.
Kiedy leki i szczepionki działają najlepiej
Ponieważ równania można uruchamiać wielokrotnie przy różnych założeniach, są potężnym narzędziem do testowania strategii leczenia na komputerze zanim spróbuje się ich u ludzi. W wielu badaniach modele zgadzają się co do jednej kluczowej kwestii: leki przeciwwirusowe działają najlepiej, gdy podane są bardzo wcześnie, zanim wirus osiągnie szczyt i zanim zakaże większości dostępnych komórek. Szczególnie obiecujące są terapie blokujące kopiowanie materiału genetycznego wirusa, zwłaszcza w połączeniu z innymi lekami działającymi przez różne mechanizmy. Leczenie podjęte późno zazwyczaj ma niewielki wpływ w symulacjach, chyba że użyje się kilku silnych leków jednocześnie. Szczepienia konsekwentnie przewyższają same leki, głównie dlatego, że przygotowują układ odpornościowy do szybkiego rozpoznania wirusa i skracają czas trwania wysokiego poziomu wiremii.
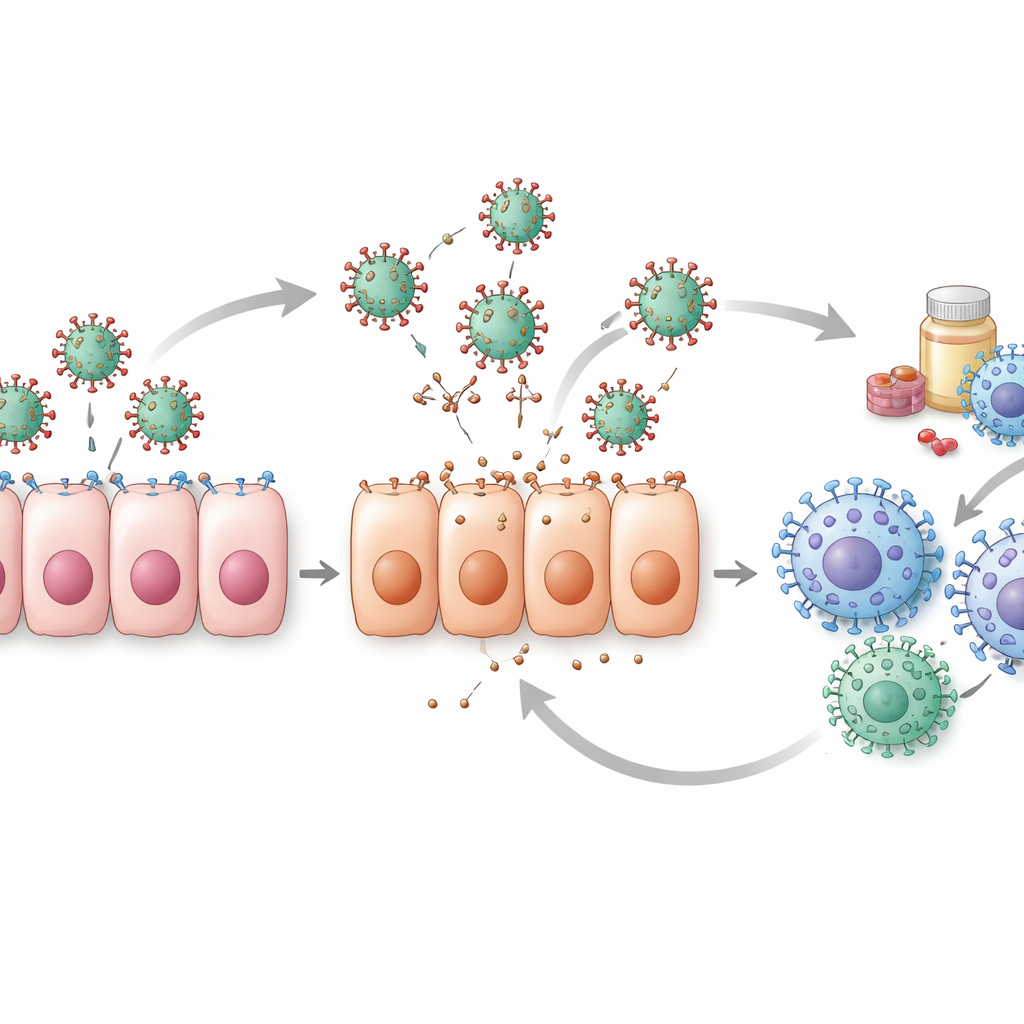
Ukryte wyzwania w danych
Przegląd ujawnia także słabości kryjące się za liczbami. Większość klinicznych zbiorów danych zaczyna się dopiero wtedy, gdy ludzie zaczynają odczuwać objawy, co oznacza, że modele często pomijają kluczowe pierwsze dni infekcji, gdy poziomy wirusa rosną najszybciej. Bez tych wczesnych pomiarów różne kombinacje parametrów modelu mogą wyjaśniać te same dane, co utrudnia pewne określenie właściwej interpretacji. Tylko mniejszość badań przeprowadza rygorystyczne testy sprawdzające, czy oszacowania parametrów są naprawdę jednoznaczne i wiarygodne. Badania na zwierzętach i eksperymenty w hodowlach komórkowych pomagają wypełnić niektóre luki, szczególnie dla wczesnych punktów czasowych, ale różnice między gatunkami i systemami laboratoryjnymi ograniczają bezpośrednią możliwość przenoszenia tych wyników na ludzi.
Co to oznacza na przyszłość
Dla niespecjalisty najważniejszy wniosek jest taki, że starannie skonstruowane modele matematyczne znacząco poprawiły nasze zrozumienie zachowania SARS-CoV-2 wewnątrz organizmu oraz tego, jak czas, kombinacje leków i wcześniejsze szczepienia wpływają na przebieg choroby. Modele generalnie zgadzają się, że wczesna, silna interwencja — szczególnie poprzez szczepienia i terminowe zastosowanie leków przeciwwirusowych — daje układowi odpornościowemu najlepszą szansę na zwycięstwo, podczas gdy opóźnione reakcje, zarówno ze strony organizmu, jak i leczenia, wiążą się z cięższym przebiegiem choroby. Jednocześnie autorzy podkreślają, że narzędzia te są tylko tak dobre, jak dane, które się do nich wprowadza. Aby przygotować się na przyszłe warianty lub nowe wirusy, wzywają do bogatszego, wcześniejszego pobierania próbek klinicznych i szerszych pomiarów odpowiedzi immunologicznej, tak aby „liczby stojące za infekcją” mogły szybciej i dokładniej wspierać decyzje w rzeczywistych ogniskach choroby.
Cytowanie: Kapischke, T., Herrmann, S.T., Bertzbach, L.D. et al. Ordinary differential equation models of SARS-CoV-2 replication dynamics and antiviral drug efficacies. npj Viruses 4, 17 (2026). https://doi.org/10.1038/s44298-026-00183-8
Słowa kluczowe: Dynamika wirusa SARS-CoV-2, modelowanie w obrębie gospodarza, termin podania terapii przeciwwirusowej, odpowiedź immunologiczna, Szczepienia przeciw COVID-19