Clear Sky Science · pl
Różne role chaperonów Hsp70 w wydzielaniu białek ortoflawirusa i formowaniu wirionów
Dlaczego mali pomocnicy od szoku cieplnego mają znaczenie dla wirusów atakujących mózg
Wirusy przenoszone przez kleszcze i komary, takie jak wirus kleszczowego zapalenia mózgu i wirus Zachodniego Nilu, mogą wnikać do mózgu i wywoływać poważne choroby, a mimo to brak jest specyficznych leków, które by je powstrzymywały. W tym badaniu przyjrzano się, jak te wirusy przejmują zestaw naszych własnych „pomocników” białkowych, zwanych chaperonami Hsp70, aby zbudować i uwolnić nowe cząstki wirusa. Ponieważ białka Hsp70 są już badane jako cele w terapii przeciwnowotworowej, zrozumienie tej relacji może otworzyć nowe drogi leczenia groźnych zakażeń wirusowych bez bezpośredniego atakowania wirusów.
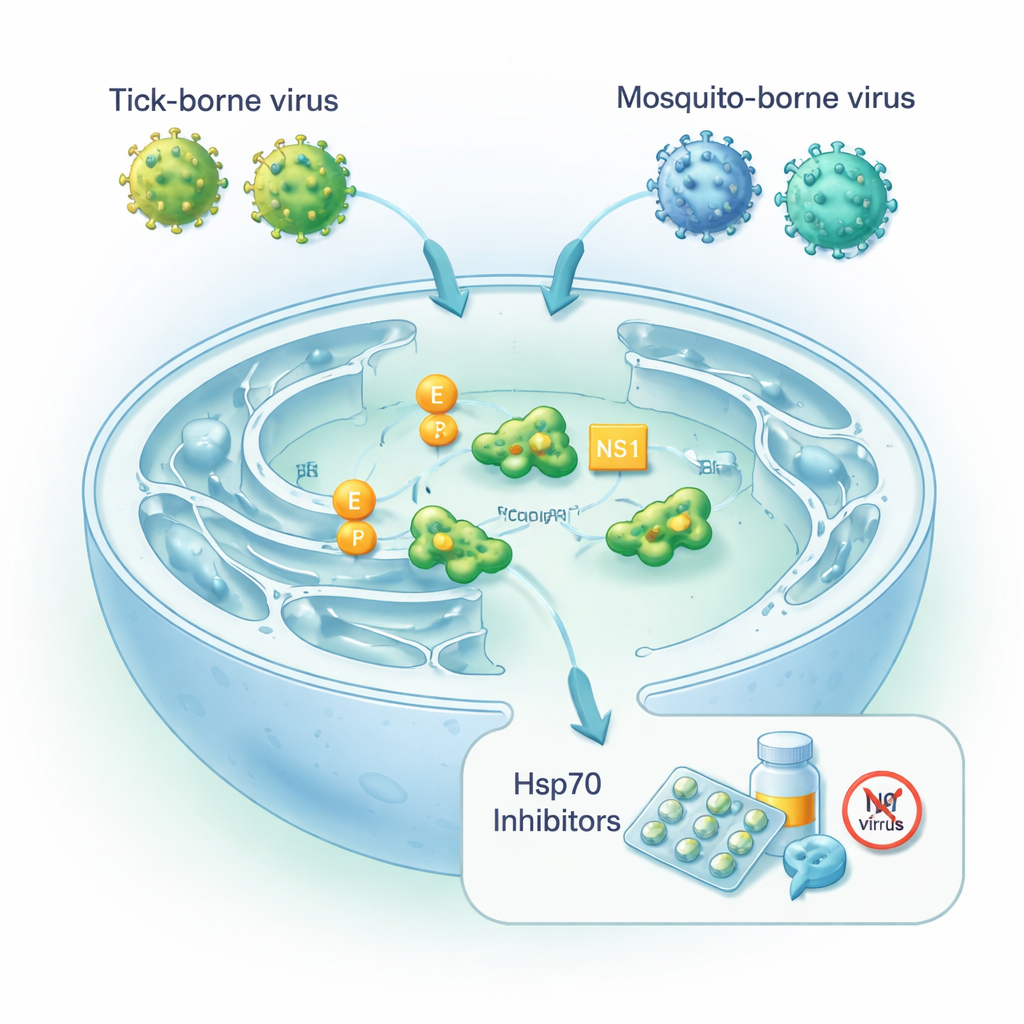
Wirusy polegające na komórkowej maszynerii składania białek
Ortoflawirusy to małe wirusy RNA, których materiał genetyczny koduje długi poliproteinę, którą trzeba pociąć i złożyć na kilka funkcjonalnych fragmentów. Dwa kluczowe składniki wirusa to białko otoczki E, które pokrywa cząstkę wirusa i pozwala jej wejść do nowych komórek, oraz białko nienowotworowe NS1, które pomaga wirusowi kopiować genom i może być wydzielane, by modulować układ odpornościowy. Wszystko to zachodzi w siateczce śródplazmatycznej, części komórki, gdzie wiele białek jest składanych i przygotowywanych do eksportu. Tam komórka polega na chaperonach Hsp70, w tym na formie rezydentnej zwanej BiP, aby zapobiegać niewłaściwemu fałdowaniu nowo powstających białek w warunkach stresu. Autorzy zapytali, jak silnie neurotropowe ortoflawirusy przenoszone przez kleszcze i komary zależą od tych chaperonów przy składaniu zakaźnych cząstek.
Bezpośrednie „uściski dłoni” między białkami wirusowymi a Hsp70
Używając komórek zmodyfikowanych tak, by nadprodukowały konkretne białka wirusowe, a także komórek zakażonych autentycznymi wirusami, badacze wyizolowali BiP lub Hsp70 i sprawdzili, którzy partnerzy wirusowi byli razem z nimi. Stwierdzili, że BiP i Hsp70 konsekwentnie tworzyły kompleksy z białkiem otoczki E z kilku ortoflawirusów, zarówno przenoszonych przez kleszcze, jak i przez komary. Sugeruje to, że fałdowanie E w siateczce śródplazmatycznej jest kierowane przez te chaperony. Obraz był bardziej selektywny dla NS1: BiP i Hsp70 wiązały się silnie z NS1 wirusów przenoszonych przez kleszcze — wirusem kleszczowego zapalenia mózgu i wirusem Langat — ale nie z NS1 wirusów przenoszonych przez komary, takich jak wirus Zachodniego Nilu i Usutu. Różnice te prawdopodobnie odzwierciedlają zmienności w tym, jak NS1 jest ozdabiane łańcuchami cukrowymi i jak się fałduje, co sugeruje, że nie wszystkie spokrewnione wirusy korzystają z tych samych ścieżek gospodarza.
Blokowanie chaperonów gwałtownie zmniejsza produkcję wirusa
Ponieważ białka Hsp70 są podatne na działanie leków, zespół przetestował dwie małe cząsteczki, które zaburzają różne elementy maszyny chaperonowej. YM‑1 celuje w domenę wiążącą nukleotydy, immobilizując białka Hsp70 w stanie nieaktywnym, podczas gdy PES‑Cl blokuje kieszeń wiążącą substraty, która normalnie chwyta białka-klienty. W dawkach pozostawiających większość komórek przy życiu, YM‑1 drastycznie zmniejszył ilość zakaźnego wirusa uwalnianego dla wszystkich czterech testowanych ortoflawirusów i obniżył poziom białka otoczki wykrywanego w medium hodowlanym, co wskazuje na ogólny blok w tworzeniu lub uwalnianiu cząstek. PES‑Cl, w przeciwieństwie do tego, miał niewielki wpływ na miano zakaźne ani na poziomy białka otoczki, mimo że osłabił fizyczną interakcję między Hsp70/BiP a białkiem otoczki w testach wiązania. To sugeruje, że krótkotrwałe zakłócenie miejsca chwytającego nie wystarcza, by unieruchomić składanie wirusa, podczas gdy wyłączenie cyklu napędzanego energią chaperonu tak.
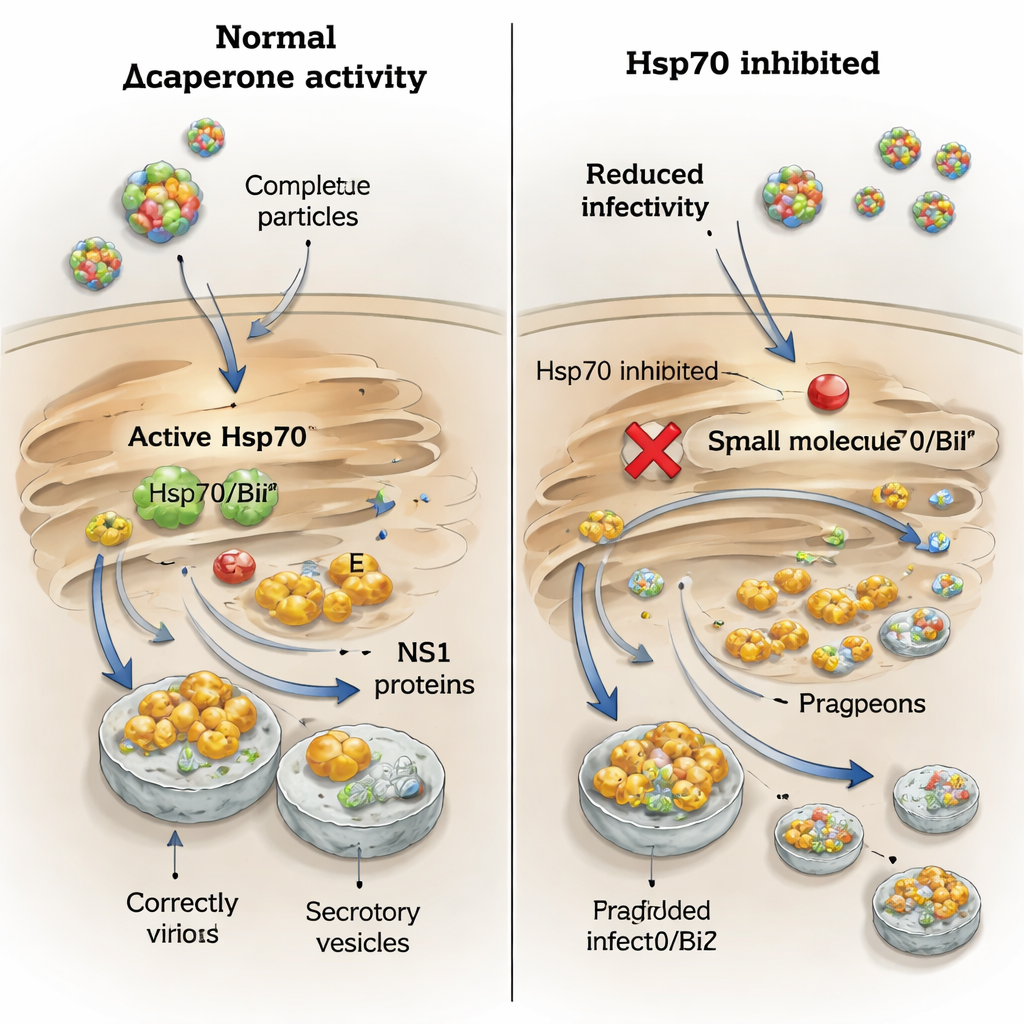
Szczególna zależność wirusów przenoszonych przez kleszcze od BiP w przypadku NS1
Historia dotycząca NS1 była bardziej zniuansowana. Gdy zakażone komórki traktowano PES‑Cl, wydzielanie NS1 z wirusów kleszczowego zapalenia mózgu i Langat spadło gwałtownie, podczas gdy NS1 wirusów Zachodniego Nilu i Usutu nie uległo zmianie. Odzwierciedla to wcześniejsze odkrycie, że tylko NS1 wirusów przenoszonych przez kleszcze silnie wiąże się z BiP i Hsp70. Aby przyjrzeć się roli BiP bliżej, autorzy użyli małych interferujących RNA do obniżenia poziomów BiP specyficznie. To zmniejszyło ilości zarówno białka otoczki, jak i NS1 wewnątrz komórek i w płynie otaczającym komórki dla wirusów kleszczowego zapalenia mózgu i Zachodniego Nilu, lecz miana zakaźne spadły tylko umiarkowanie. Gdy komórki pozbawione BiP traktowano lekami blokującymi degradację białek, poziomy NS1 wewnątrz komórki odbudowały się, ale jego wydzielanie nie — co pokazuje, że BiP jest potrzebny nie tylko do ochrony NS1 przed rozkładem, lecz także do prowadzenia go szlakiem sekrecyjnym.
Co to oznacza dla przyszłych strategii przeciwwirusowych
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie, że te wirusy atakujące mózg silnie polegają na własnych komórkowych pomocnikach fałdowania białek, aby zbudować swoją zewnętrzną powłokę i — w przypadku niektórych gatunków — wysyłać NS1 jako wydzielaną broń. Szeroko działający inhibitor chaperonów, taki jak YM‑1, może zatem mocno ograniczyć produkcję zakaźnych cząstek wielu spokrewnionych wirusów jednocześnie, choć jego silne efekty prawdopodobnie wykraczają poza pojedynczy chaperon i mogą obciążać zdrowe komórki. Bardziej ukierunkowane podejścia, być może skupiające się na tym, jak BiP i Hsp70 obsługują konkretne wirusowe klienty, takie jak NS1, mogą kiedyś pomóc zaprojektować terapie trudniejsze do rozwinięcia przez wirusy oporności, a jednocześnie oszczędzające większość normalnego fałdowania białek w gospodarzu.
Cytowanie: Blank, L., Lorenz, C. & Steffen, I. Divergent roles of Hsp70 chaperones in orthoflavivirus protein secretion and virion formation. npj Viruses 4, 8 (2026). https://doi.org/10.1038/s44298-026-00175-8
Słowa kluczowe: ortoflawirus, chaperon Hsp70, wirus kleszczowego zapalenia mózgu, wirus Zachodniego Nilu, cele leków przeciwwirusowych