Clear Sky Science · pl
Rozpuszczalne białko G wirusa syncytialnego dróg oddechowych sprzyja rozprzestrzenianiu się wirusa poprzez inicjację NLRP3 zależną od TLR2 i pyroptozę
Dlaczego ten wirus płucny ma znaczenie dla wszystkich
Wirus syncytialny dróg oddechowych, w skrócie RSV, jest najbardziej znany jako zimowe zagrożenie dla niemowląt, ale także powoduje hospitalizacje wśród wielu starszych dorosłych i osób z osłabionym układem odpornościowym. Nawet przy nowych szczepionkach i przeciwciałach ochronnych RSV nadal infekuje ludzi wielokrotnie i może powodować ciężkie uszkodzenia płuc. Badanie to analizuje słabo poznane białko wirusowe — rozpuszczalną formę białka G RSV — i ujawnia, jak może ono subtelnie przygotowywać komórki płuc do gwałtownego zapalenia oraz ułatwiać wirusowi skuteczniejsze rozprzestrzenianie się drogami oddechowymi.
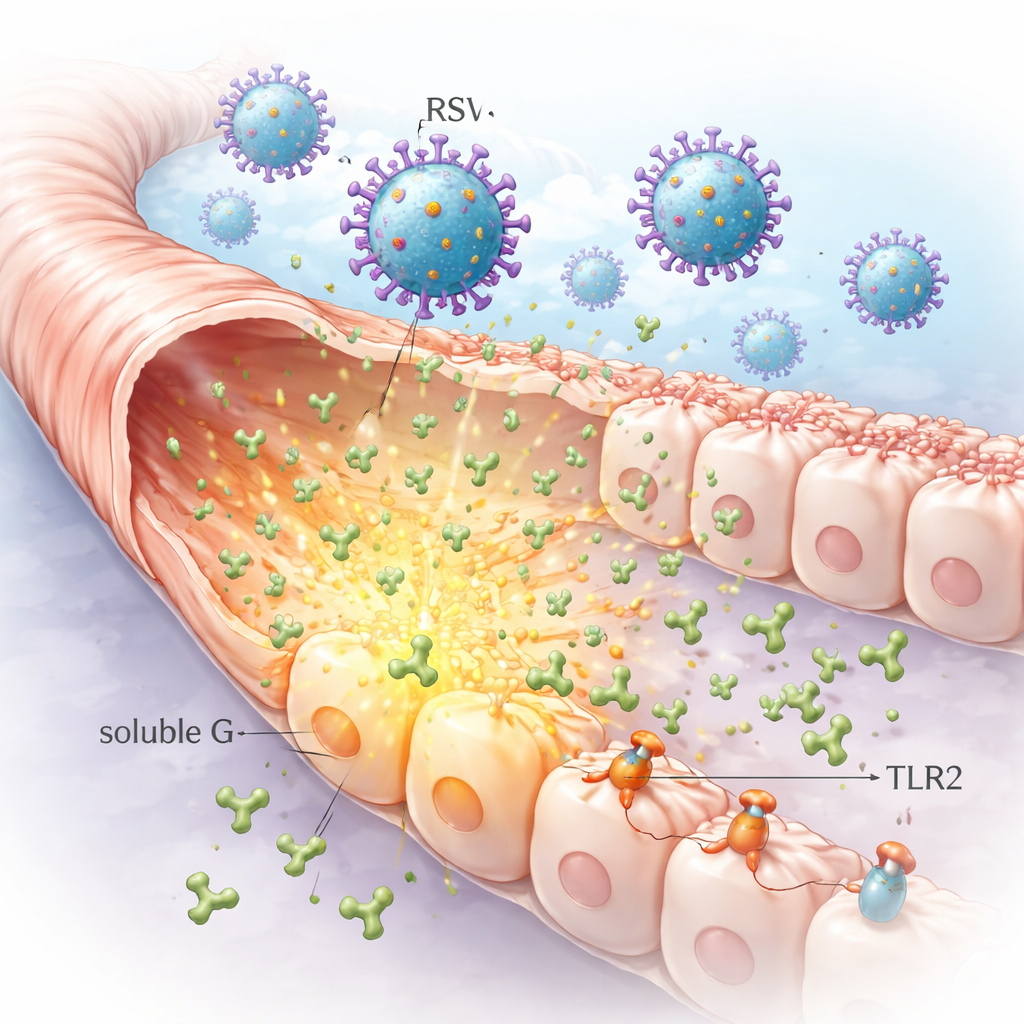
Sekretowane białko wirusowe, które podróżuje przed zakażeniem
RSV ma na powierzchni białko adhezyjne zwane G, które pomaga mu przyczepiać się do komórek dróg oddechowych. Niezwykle, zakażone komórki uwalniają też duże ilości wolnej, unoszącej się wersji tego białka, znanej jako rozpuszczalne G. Badacze wykazali, że hodowane w laboratorium komórki płucne zakażone RSV mogą wyrzucać bardzo wysokie stężenia rozpuszczalnego G do otoczenia. Ponieważ ta forma może dyfundować z miejsca pierwotnego zakażenia, może docierać do sąsiednich komórek jeszcze niezainfekowanych, przygotowując grunt do szerszych zmian w nabłonku płucnym niż sam wirus by spowodował.
Rozpuszczalne G jako dwufunkcyjny klucz do powierzchni komórek
Łącząc mikroskopię, testy typu pull-down i traktowanie enzymatyczne, zespół odtworzył sposób, w jaki rozpuszczalne G przyczepia się do komórek. Stwierdzili, że może wiązać się z łańcuchami cukrowymi zwanymi glikozoaminoglikanami, jak również z poznanym receptorem RSV — CX3CR1. Co kluczowe, rozpuszczalne G także wiąże się z cząsteczką rozpoznającą wzorce na komórkach odpornościowych i dróg oddechowych, zwaną TLR2. Mały motyw w białku G, znany jako CX3C, okazał się istotny dla silnego wiązania z CX3CR1 i dla wydajnego rekrutowania TLR2. Oznacza to, że rozpuszczalne G może najpierw zostać luźno złapane na powierzchni komórki, a następnie zaangażować bardziej specyficzne receptory kontrolujące odpowiedź komórkową na zagrożenia.
Przygotowywanie komórek płuc do zapalnego rodzaju śmierci komórkowej
Aktywacja TLR2 przez rozpuszczalne G okazała się daleka od obojętnej. W komórkach raportujących układu odpornościowego i liniach komórek ludzkich płuc, rozpuszczalne G uruchomiło szlak sygnałowy MyD88–NF-κB w dół od TLR2, prowadząc do uwalniania zapalnych sygnałów, takich jak IL-6 i IL-8. Jednocześnie zwiększyło produkcję składników molekularnego „systemu alarmowego” zwanego inflammasomem NLRP3 oraz enzymów generujących reaktywne cząsteczki, takie jak tlenek azotu i rodniki tlenowe. Same w sobie zmiany te powodowały tylko łagodne uszkodzenia. Jednak gdy wcześniej przygotowane komórki zostały następnie zakażone RSV, drugi cios wywołał pełne złożenie inflammasomu, aktywację enzymu kaspazy‑1, powstawanie porów w błonie komórkowej i zapalny rodzaj śmierci komórkowej znany jako pyroptoza. Proces ten przebijał komórki otworami, wypuszczał zapalne treści i pokrywał się z większymi ilościami zakaźnego wirusa uwalnianego do płynu hodowlanego.
Jak ta kaskada może pogorszyć chorobę płuc
Efekt pro‑śmierci rozpuszczalnego G był najsilniejszy w komórkach nabłonka dróg oddechowych — tych samych, które RSV woli infekować — i zależał od inflammasomu NLRP3, ponieważ specyficzny inhibitor NLRP3 w dużej mierze przywracał przeżywalność komórek. W przeciwieństwie do tego, niektóre komórki odpornościowe bogate w TLR2, ale ubogie w receptor CX3CR1, nie przechodziły w tych samych warunkach silnej śmierci litycznej. Ten wzorzec sugeruje, że RSV wykorzystuje rozpuszczalne G do selektywnego osłabiania i niszczenia ochronnej wyściółki dróg oddechowych, jednocześnie zachowując część komórek odpornościowych, które mogą dalej produkować sygnały. Wynikiem jest środowisko płucne z większym stanem zapalnym, większą ilością szczątków komórkowych i większymi możliwościami dla cząstek wirusa, by uciec i zakażać sąsiednie komórki.
Co to oznacza dla przyszłych terapii
Dla osoby niebędącej specjalistą kluczowy przekaz jest taki, że RSV nie polega wyłącznie na bezpośrednim uszkodzeniu przez inwazję wirusową. Poprzez uwalnianie dużych ilości rozpuszczalnego białka G może ono „zmiękczać” pobliskie komórki poprzez TLR2, zwiększając ich podatność na zapalny rodzaj śmierci i wypływ wirusa. Praca ta identyfikuje kilka etapów tej kaskady — samo rozpuszczalne G, jego motyw CX3C, TLR2 i inflammasom NLRP3 — jako potencjalne cele terapeutyczne. W teorii terapie blokujące interakcję między rozpuszczalnym G a TLR2 lub tłumiące aktywność NLRP3 mogłyby zmniejszyć zarówno uszkodzenie płuc, jak i rozprzestrzenianie się wirusa. Takie podejścia mogłyby w przyszłości uzupełniać istniejące szczepionki i przeciwciała przeciw RSV, oferując lepszą ochronę dla najmłodszych i najbardziej podatnych pacjentów.
Cytowanie: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
Słowa kluczowe: wirus syncytialny dróg oddechowych, rozpuszczalne białko G, inflammasom TLR2, pyroptoza, zapalenie płuc