Clear Sky Science · pl
Probabilistyczne podejście uczenia głębokiego do segmentacji splotu naczyniówkowego w zaburzeniach ze spektrum autyzmu
Dlaczego ta praca ma znaczenie dla zdrowia mózgu i autyzmu
Splot naczyniówkowy to niewielka struktura głęboko w mózgu, która pomaga w wytwarzaniu i filtrowaniu płynu otaczającego mózg i rdzeń kręgowy, a także odgrywa kluczową rolę w aktywności układu odpornościowego w mózgu. Coraz więcej dowodów sugeruje, że u niektórych osób z zaburzeniami ze spektrum autyzmu (ASD) ta struktura może wyglądać lub funkcjonować inaczej, co może odzwierciedlać zmiany związane z zapaleniem w mózgu. Aby naprawdę zrozumieć te związki, naukowcy muszą przeanalizować tysiące skanów mózgu — a to wymaga szybkich, niezawodnych narzędzi komputerowych, które automatycznie wykryją i obrysują splot naczyniówkowy. W tym badaniu przedstawiono i przetestowano takie narzędzie, pokazując nie tylko jego skuteczność, lecz także stopień pewności, z jaką formułuje swoje odpowiedzi.
Mała, lecz potężna brama mózgu
Splot naczyniówkowy znajduje się w wypełnionych płynem przestrzeniach mózgu i tworzy barierę między krwią a przezroczystym płynem zwanym płynem mózgowo-rdzeniowym. Pomaga kontrolować, co wchodzi i wychodzi ze środowiska mózgu, oraz uczestniczy w sygnalizacji immunologicznej, w tym w reakcjach związanych z zapaleniem. Wcześniejsze badania wykazały, że splot naczyniówkowy może być powiększony lub zmieniony w różnych chorobach mózgu, od stwardnienia rozsianego po depresję, a wstępne prace sugerują, że różnice mogą występować także u niektórych osób z autyzmem. Jednak ręczne odrysowywanie tej struktury na skanach MRI jest powolne, trudne i częściowo subiektywne, co sprawia, że badania na dużą skalę są praktycznie niemożliwe bez automatyzacji.
Nauka komputera rozpoznawania splotu naczyniówkowego
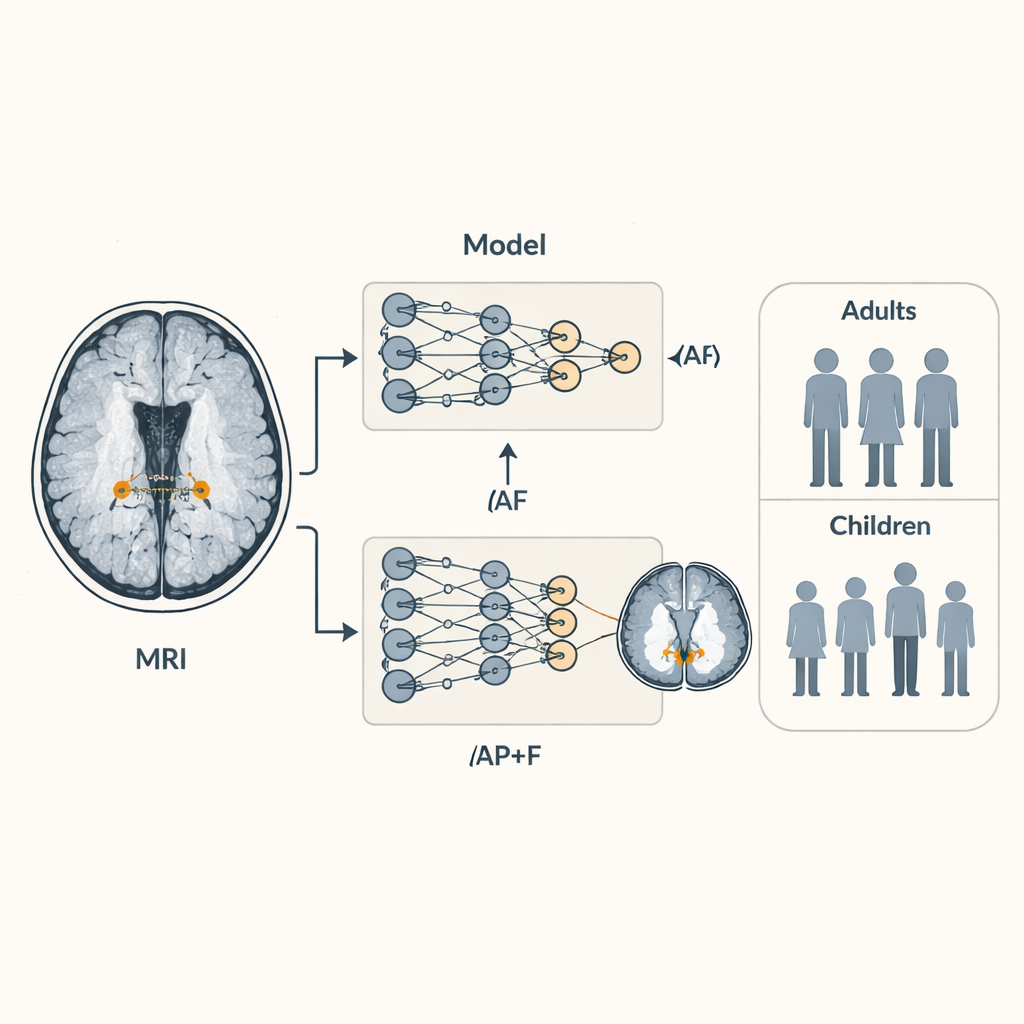
Autorzy skupili się na ASCHOPLEX, niedawno opracowanym systemie uczenia głębokiego, który automatycznie segmentuje, czyli obrysowuje, splot naczyniówkowy na skanach MRI. Początkowo trenowany na dorosłych z i bez stwardnienia rozsianego, ASCHOPLEX już wykazał dokładność zbliżoną do ludzkiej w innych grupach. W tym badaniu zespół dostosował narzędzie do ASD, „dostrajając” je za pomocą niewielkiego, lecz starannie oznakowanego zbioru 12 dorosłych (z autyzmem i bez) pochodzących z lokalnego projektu badawczego. Następnie przetestowali jego działanie na dodatkowych 53 dorosłych, których splot naczyniówkowy został ręcznie odrysowany przez ekspertów, co pozwoliło na bezpośrednie porównanie człowiek–maszyna. Porównali też ASCHOPLEX z szeroko stosowanym narzędziem do analizy MRI mózgu, FreeSurfer, które nie było zaprojektowane specjalnie dla tej struktury.
Dodanie poczucia pewności do predykcji
Powyżej pytania o to, czy narzędzie ma rację, badacze chcieli wiedzieć, jak bardzo jest pewne każdej decyzji. Aby to osiągnąć, zmienili ASCHOPLEX w model „probabilistyczny”, włączając technikę zwaną dropout zarówno podczas trenowania, jak i testowania. W praktyce oznacza to, że model jest uruchamiany wielokrotnie na tym samym skanie, za każdym razem z nieco innymi ustawieniami wewnętrznymi, co daje zbiór nieco różnych predykcji. Analizując, jak bardzo te predykcje zgadzają się lub rozchodzą w poszczególnych punktach mózgu, zespół mógł oszacować niepewność — miejsca, w których model jest pewny, i miejsca, w których nie jest. Podejście to zastosowano nie tylko do lokalnego zbioru dorosłych, lecz także do ponad 1 800 uczestników, dzieci i dorosłych, z dużego projektu Autism Brain Imaging Data Exchange (ABIDE).
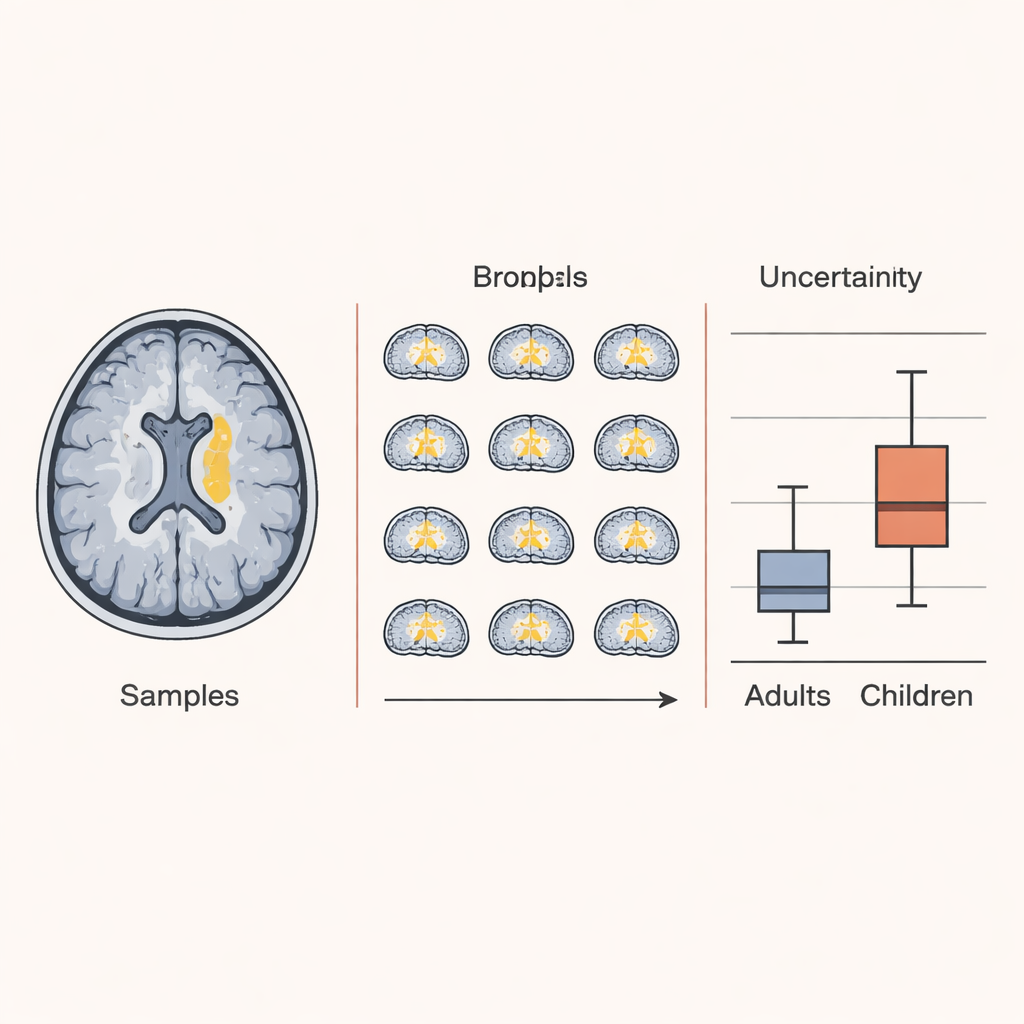
Jak dobrze narzędzie działało w różnych grupach wiekowych
Po dostrojeniu ASCHOPLEX ściśle pokrywał się z ręcznymi obrysami splotu naczyniówkowego u dorosłych z autyzmem i bez niego, osiągając poziomy dokładności porównywalne lub lepsze niż zgodność między ekspertami. Wyraźnie przewyższał FreeSurfer, który nigdy nie był optymalizowany pod kątem tej struktury. Co ważne, po dostrojeniu ASCHOPLEX nie wykazywał już różnic w wydajności między dorosłymi z autyzmem i bez autyzmu ani między mężczyznami a kobietami, co zmniejsza obawy o systematyczne uprzedzenia. Gdy wersja probabilistyczna została zastosowana do dużego zbioru ABIDE, model był najbardziej pewny w przypadku dorosłych, szczególnie tych podobnych do grupy treningowej, ale jego niepewność rosła zarówno dla dorosłych, jak i dzieci pochodzących z zewnętrznych ośrodków — i była najwyższa u dzieci. Szczegółowa analiza wykazała, że ta dodatкова niepewność odzwierciedlała głównie brak znajomości skanów mózgów dzieci przez model, a nie słabą jakość skanów.
Co to oznacza dla przyszłych badań nad autyzmem
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że badacze mają teraz praktyczne narzędzie oparte na sztucznej inteligencji, które może z dużą dokładnością znaleźć bardzo małą, istotną strukturę mózgową u osób z autyzmem i bez niego oraz ocenić pewność każdego wyniku. ASCHOPLEX, zwłaszcza w swojej probabilistycznej formie, można stosować do dużych zbiorów obrazów w celu przesiewowego wykrywania zmian splotu naczyniówkowego, które mogą wskazywać na zmienioną aktywność immunologiczną w mózgu. Jednocześnie rosnąca niepewność w przypadku dzieci podkreśla, że takie narzędzia nadal wymagają dodatkowego treningu na młodszych populacjach, zanim będzie można im w pełni zaufać we wszystkich grupach wiekowych. Ogólnie rzecz biorąc, badanie pokazuje, jak połączenie uczenia głębokiego z jawnie mierzonym poziomem pewności może uczynić analizy obrazowania mózgu bardziej efektywnymi i przejrzystymi, torując drogę do lepszego zrozumienia zmian neuroimmunologicznych w autyzmie.
Cytowanie: Bargagna, F., Morin, T.M., Chen, YC. et al. A probabilistic deep learning approach for choroid plexus segmentation in autism spectrum disorder. NPP—Digit Psychiatry Neurosci 4, 2 (2026). https://doi.org/10.1038/s44277-026-00056-1
Słowa kluczowe: zaburzenia ze spektrum autyzmu, splot naczyniówkowy, rezonans magnetyczny mózgu, uczenie głębokie, nezapalenie nerwowe