Clear Sky Science · pl
Kompleksowe ramy genomowe do identyfikacji genów predysponujących do raka piersi lub jajnika z niedoborem naprawy przez rekombinację homologiczna
Dlaczego niektóre rodziny mają wyższe ryzyko zachorowania
Wiele kobiet z rakiem piersi lub jajnika ma silne rodzinne występowanie choroby, lecz badania genetyczne często nie dostarczają jasnego wyjaśnienia. Ta luka, nazywana czasem „brakującą dziedzicznością”, pozostawia rodziny bez odpowiedzi i może ograniczać dostęp do spersonalizowanego nadzoru czy terapii, np. leków ukierunkowanych. W tym badaniu celem było opracowanie nowego, bardziej skutecznego sposobu poszukiwania ukrytych genów zwiększających ryzyko raka poprzez połączenie kilku rodzajów danych genomicznych i klinicznych, zamiast analizowania ich osobno. 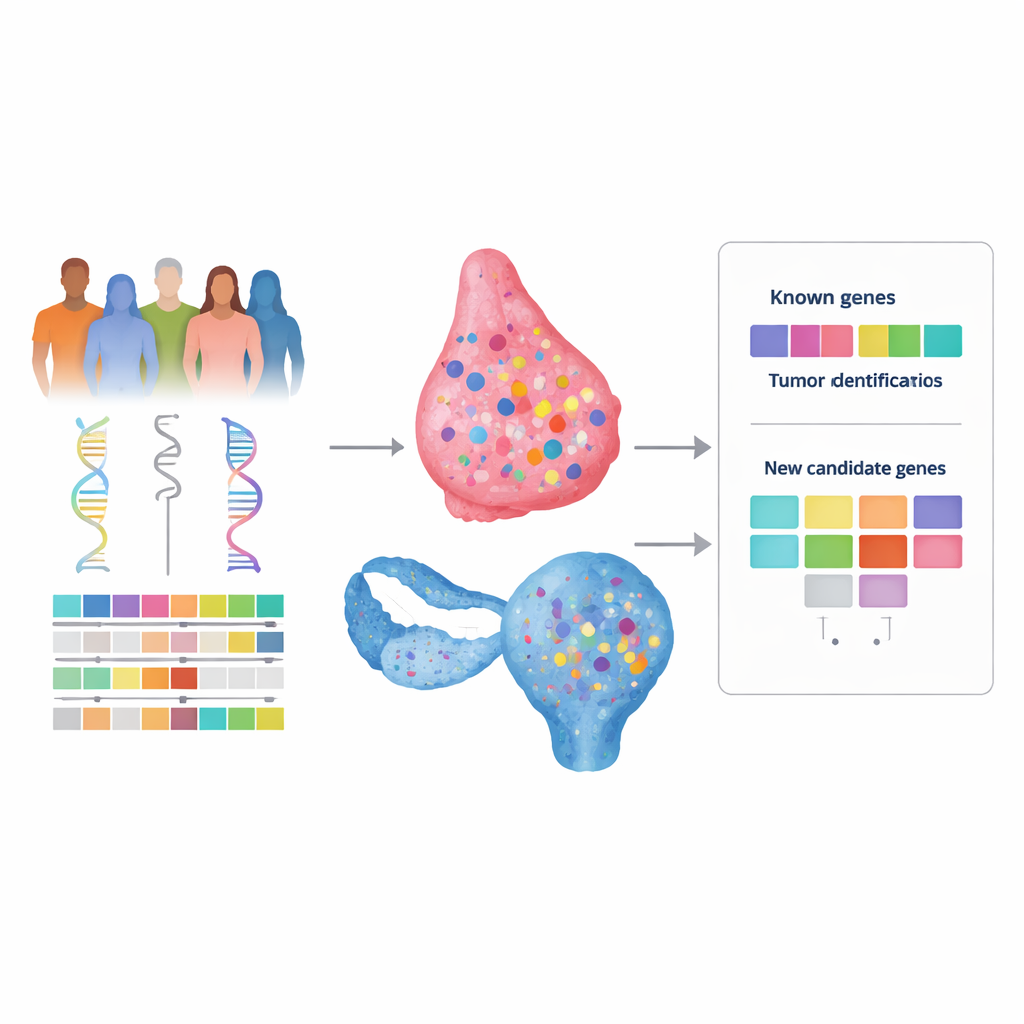
Poszukiwanie odcisku palca wadliwej naprawy DNA
Naukowcy skupili się na specyficznym typie naprawy uszkodzeń DNA, znanej jako naprawa przez rekombinację homologiczna, która normalnie usuwa niebezpieczne pęknięcia materiału genetycznego. Gdy ten system zawodzi, komórki akumulują charakterystyczny „sygnaturowy” wzór mutacji – wzorzec zmian w DNA guza, który działa jak molekularny odcisk palca. Ten wzorzec występuje szczególnie często w pewnych trudnych do leczenia nowotworach piersi i jajnika. Zespół założył, że jeśli guz wykazuje taki odcisk, prawdopodobnie utracił obie działające kopie jakiegoś genu naprawy DNA, znanego lub nieznanego, i że można to powiązać z dziedzicznymi zmianami w tym genie.
Budowanie połączonych ram genetycznych i klinicznych
Aby przetestować tę ideę, autorzy przeanalizowali DNA setek pacjentek z rakiem piersi i jajnika z The Cancer Genome Atlas, który udostępnia zarówno materiał z krwi (dziedziczny), jak i z guza (nabyty), wraz z danymi klinicznymi. Przeszukali cały egzom – białkododające części genomu – w poszukiwaniu rzadkich, dziedzicznych wariantów wyglądających na szkodliwe oraz takich, które miały w guzie „drugie trafienie”, na przykład utratę pozostałej zdrowej kopii. Dla każdego genu sprawdzili, czy takie zdarzenia dwóch trafień występują częściej w guzach z sygnaturą niedoboru naprawy niż w guzach jej pozbawionych. Co istotne, nie ograniczali się do uprzednio ustalonego panelu genów, co pozwoliło na wyłonienie nieoczekiwanych kandydatów.
Sprawdzenie działania metody i wykrycie nowych podejrzanych
Jako punkt odniesienia, ramy prawidłowo wyeksponowały dobrze znane geny raka piersi i jajnika BRCA1 i BRCA2 jako silnie powiązane z sygnaturą defektu naprawy w obu typach nowotworów, potwierdzając, że podejście działa zgodnie z oczekiwaniami. W raku piersi wskazano także dodatkowy gen, THBS4, oraz zasugerowano możliwe role genów KIF13B i TESPA1. Jednak szczegółowy przegląd przypadków wykazał, że zmiany w THBS4 często występowały równolegle z innymi, lepiej ugruntowanymi zdarzeniami związanymi z naprawą DNA, co czyniło go mniej przekonującym kandydatem na głównego czynnika. 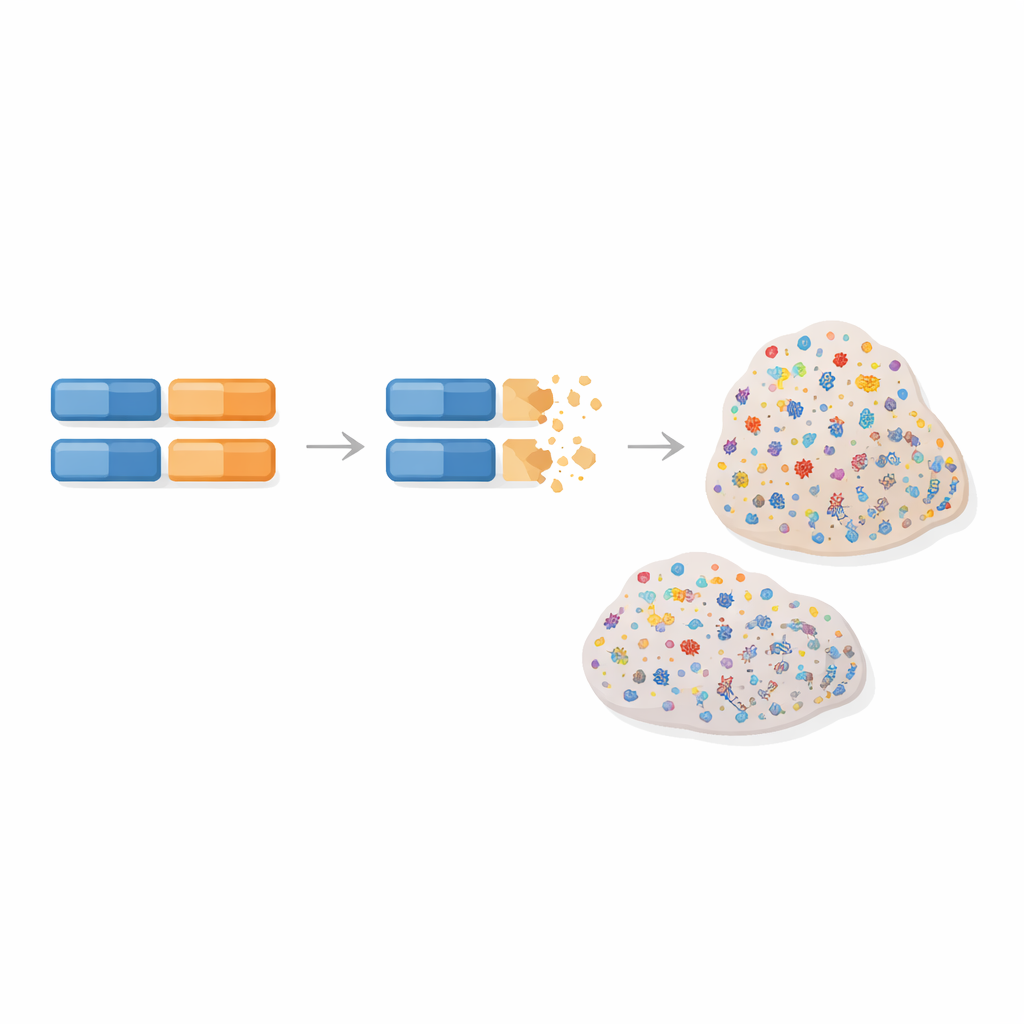
Skupienie na nie wyjaśnionych guzach o wysokim ryzyku
Aby pójść dalej niż same statystyki, badacze włączyli szczegóły kliniczne, takie jak podtyp guza, wiek w chwili rozpoznania i pochodzenie etniczne. Skoncentrowali się na pacjentach, których guzy wyraźnie wykazywały sygnaturę defektu naprawy i należały do grup klinicznych już powiązanych z tą biologią – nowotworów piersi o fenotypie basal‑like oraz wysokozróżnicowanych surowiczych raków jajnika – lecz brakowało w nich znanych zdarzeń typu BRCA. U tych pacjentek ponownie szukali dziedzicznych wariantów z „drugim trafieniem”, tym razem w ramach szerokiej, przeglądowej listy genów związanych z rakiem i naprawą DNA. Ten „kliniczno‑genomiczny” przegląd wyłonił kilka genów zaangażowanych w naprawę pęknięć dwuniciowych DNA oraz blisko powiązany szlak zespołu Fanconiego, w tym RAD51B, RAD54B, RAD54L, FANCD2 i inne, jako prawdopodobne nowe składniki dziedzicznego ryzyka.
Co to oznacza dla pacjentów i przyszłych badań
Badanie nie twierdzi, że jednoznacznie dowiodło istnienia nowych genów ryzyka raka; liczba pacjentek z danym kandydackim genem jest wciąż niewielka i potrzebne będą większe, bardziej zróżnicowane kohorty, aby potwierdzić ich role. Zamiast tego autorzy przedstawiają powtarzalny plan działania: sposób łączenia danych dziedzicznych i guzowych, charakterystycznych sygnatur mutacyjnych oraz cech klinicznych, aby systematycznie priorytetyzować geny mogące leżeć u podstaw niewyjaśnionych przypadków rodzinnych. W miarę stosowania tych ram do większych zbiorów danych i innych typów nowotworów, można zmniejszyć lukę w „brakującej dziedziczności”, dopracować panele badań genetycznych i pomóc większej liczbie pacjentów zrozumieć ich indywidualne ryzyko oraz opcje profilaktyki i terapii ukierunkowanej.
Cytowanie: Camacho-Valenzuela, J., Matis, T., Roca, C. et al. A comprehensive genomic framework for identifying genes predisposing to homologous recombination repair-deficient breast or ovarian cancer. BJC Rep 4, 15 (2026). https://doi.org/10.1038/s44276-026-00218-w
Słowa kluczowe: niedobór naprawy przez rekombinację homologiczna, genetyka raka piersi, rak jajnika, geny naprawy DNA, predyspozycje do raka