Clear Sky Science · pl
Ocena STAR (stroma-tumor AI risk): związek proporcji nowotworu do zrębu wyznaczonej przez AI z przeżyciem pacjentów daje dodatkową wartość prognostyczną ponad KELIM w raku nabłonkowym jajnika
Dlaczego „sąsiedztwo” wokół guza ma znaczenie
Kiedy myślimy o raku, zwykle wyobrażamy sobie skupisko zbuntowanych komórek. Tymczasem guzy żyją w ruchliwym otoczeniu tkanki podtrzymującej, naczyń krwionośnych i komórek układu odpornościowego, zwanym zrębem (stroma). W tym badaniu postawiono proste, ale istotne pytanie: czy możemy wykorzystać równowagę między komórkami nowotworowymi a otaczającą je tkanką, mierzoną przez sztuczną inteligencję na rutynowych preparatach mikroskopowych, aby przewidzieć, które pacjentki z rakiem jajnika będą miały lepsze lub gorsze wyniki — jeszcze przed rozpoczęciem leczenia?
Nowy sposób odczytywania standardowych skrawków
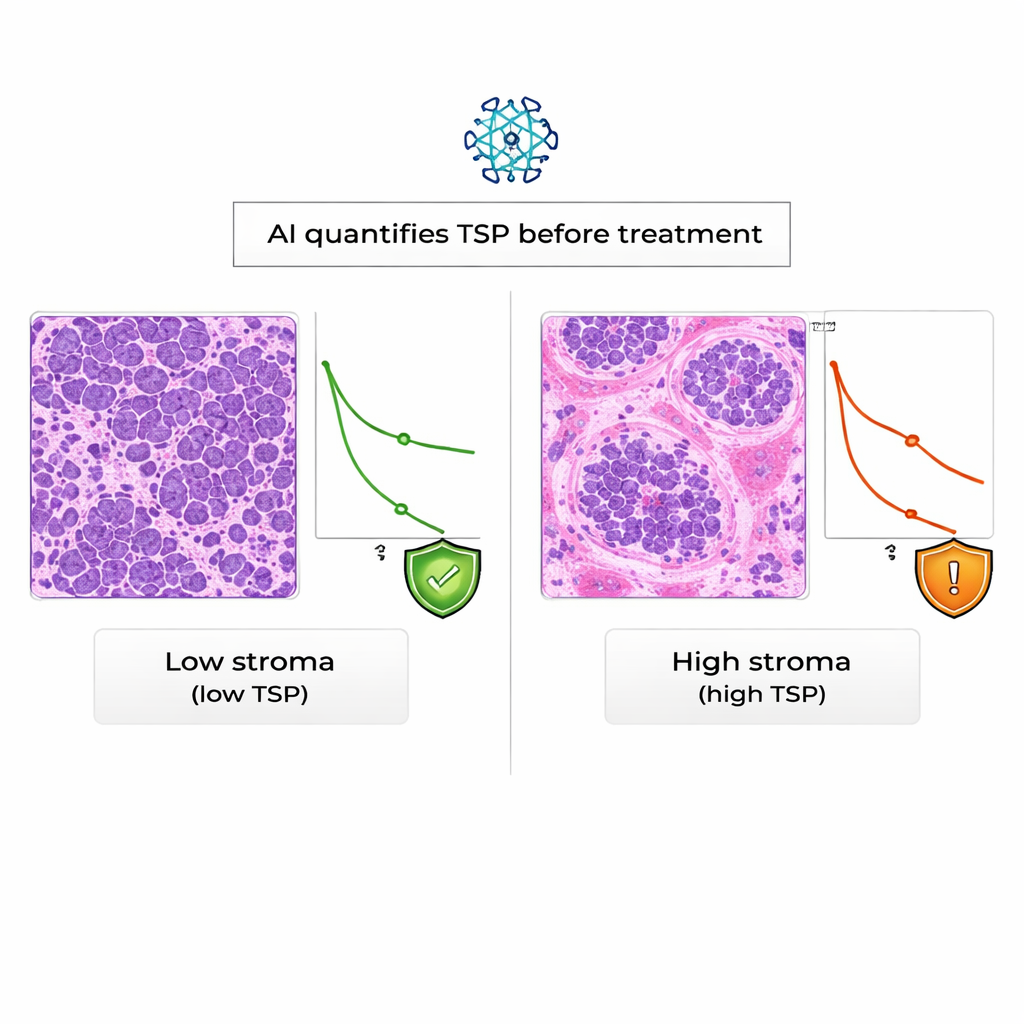
Kobietom z rakiem nabłonkowym jajnika zwykle pobiera się tkankę podczas operacji lub biopsji. Próbki te są barwione i badane pod mikroskopem w każdym szpitalu. Badacze skupili się na cechy zwanej proporcją guz–zrąb (TSP): ile obrazu zajmuje tkanka podtrzymująca w porównaniu z komórkami nowotworowymi. W wcześniejszych pracach patolodzy oceniali tę proporcję wzrokowo i zauważali, że guzy bogate w zrąb często zachowywały się bardziej agresywnie i były oporne na standardową chemioterapię opartą na platynie. W obecnym badaniu zespół zastosował system głębokiego uczenia, aby automatycznie zmierzyć TSP na zdigitalizowanych skrawkach, zamieniając ręczne, częściowo subiektywne zadanie w szybki i powtarzalny wskaźnik dostępny już przy rozpoznaniu.
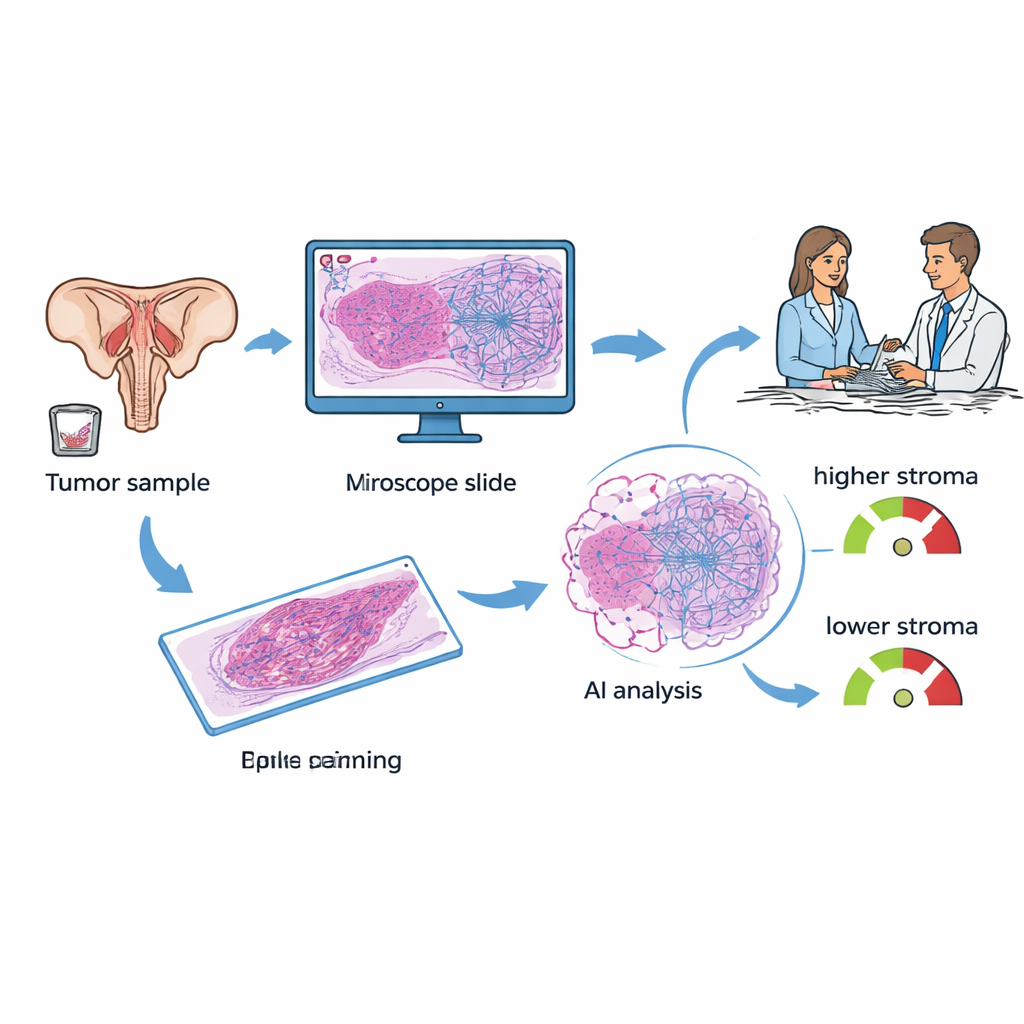
Porównanie analizy tkanek przez AI z wynikiem opartym na krwi
Obecnie jednym z szerzej dyskutowanych narzędzi w raku jajnika jest KELIM, wynik oparty na szybkości spadku markera krwi CA-125 w pierwszych 100 dniach chemioterapii. KELIM jest tani i użyteczny, ale można go obliczyć dopiero po kilku tygodniach leczenia, a nie wszystkie pacjentki mają wystarczającą liczbę wczesnych badań krwi, by generować wynik. Badacze zebrali dane od 89 kobiet leczonych w jednym ośrodku onkologicznym, które miały zarówno skrawki tkankowe, jak i co najmniej trzy pomiary CA‑125. Obliczyli KELIM dla każdej pacjentki, patolog oznaczył obszary guza na skrawkach, a następnie model AI oszacował TSP, klasyfikując każdy przypadek jako „niski zrąb” (mniej niż 50% zrębu) lub „wysoki zrąb” (50% lub więcej).
AI dorównuje ekspertom i wskazuje guzy o wyższym ryzyku
Ocena AI była zbliżona do oceny doświadczonych patologów: w 94% przypadków automatyczna klasyfikacja TSP zgadzała się z oceną ręczną, co uznano za doskonały poziom zgodności. Kiedy zespół przeanalizował wyniki pacjentek, stwierdzono, że kobiety, których guzy zostały zaklasyfikowane przez AI jako o wysokim udziale zrębu, miały istotnie gorsze przeżycie ogólne niż te z guzami o niskim udziale zrębu. Statystycznie rzecz biorąc, wysoki TSP niemal podwajał ryzyko zgonu w czasie obserwacji, a efekt ten utrzymywał się nawet po uwzględnieniu wyniku KELIM. Dla porównania, w tej realnej grupie pacjentek KELIM wiązał się z opornością na leki platynowe, ale nie był jednoznacznie powiązany z długością przeżycia pacjentek.
Co to może oznaczać dla decyzji terapeutycznych
Ponieważ TSP można zmierzyć na rutynowych skrawkach pobranych przy rozpoznaniu, TSP oparty na AI oferuje sposób oceny ryzyka przed rozpoczęciem chemioterapii, potencjalnie o wiele miesięcy wcześniej niż KELIM. Wynik wskazujący wysoki udział zrębu może ostrzec klinicystów, że guz prawdopodobnie będzie bardziej agresywny i trudniejszy do leczenia, co może skłonić do intensywniejszego nadzoru, wcześniejszego rozważenia dodatkowych terapii lub innej strategii chirurgicznej. Metoda jest też stosunkowo niskokosztowa: opiera się na istniejących obrazach patologicznych i modelu oprogramowania, zamiast na nowych badaniach laboratoryjnych. Autorzy argumentują, że zautomatyzowany TSP mógłby współistnieć z innymi markerami, takimi jak badania genetyczne i trendy CA‑125, w celu doprecyzowania rokowania bez znacznego obciążenia dla pacjentek czy zespołów patologicznych.
Patrząc w przyszłość: mądrzejsze, wcześniejsze wskazówki dla pacjentek
Dla osoby niebędącej specjalistą główny przekaz jest taki, że nie wszystkie raki jajnika są takie same, a tkanka podtrzymująca wokół guza niesie ważne wskazówki dotyczące zachowania choroby. Badanie pokazuje, że AI potrafi wiarygodnie odczytywać te wskazówki na standardowych skrawkach biopsyjnych i że guz o dużej zawartości zrębu zwykle wiąże się z gorszym przeżyciem, niezależnie od istniejących wyników opartych na krwi. Choć przed włączeniem tej metody do rutynowej opieki potrzebne są większe i bardziej zróżnicowane badania, TSP wyznaczony przez AI ma potencjał jako wczesny sygnał ostrzegawczy, który może pomóc lekarzom dostosować plany leczenia i dać pacjentkom wyraźniejsze oczekiwania już od samego początku.
Cytowanie: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
Słowa kluczowe: rak jajnika, sztuczna inteligencja, mikrośrodowisko guza, marker prognostyczny, patologia cyfrowa