Clear Sky Science · pl
Badanie genomowe ujawnia pojawienie się wielooporniej dominującej linii w populacjach Proteus mirabilis
Dlaczego ten szpitalny zarazek ma dla ciebie znaczenie
Dla wielu osób zakażenia dróg moczowych to sporadyczne, bolesne utrapienie. Jednak w szpitalach i domach opieki niektóre infekcje wywołują wytrzymałe bakterie, które przyczepiają się do cewników, opierają się wielu antybiotykom i cicho rozprzestrzeniają się między ludźmi i zwierzętami. To badanie śledzi właśnie takiego sprawcę, Proteus mirabilis, na całym świecie, używając jego DNA jak pamiętnika podróży, aby ujawnić, jak jedna trudna do leczenia rodzina powoli zdobyła dominację w ciągu ostatniego stulecia.
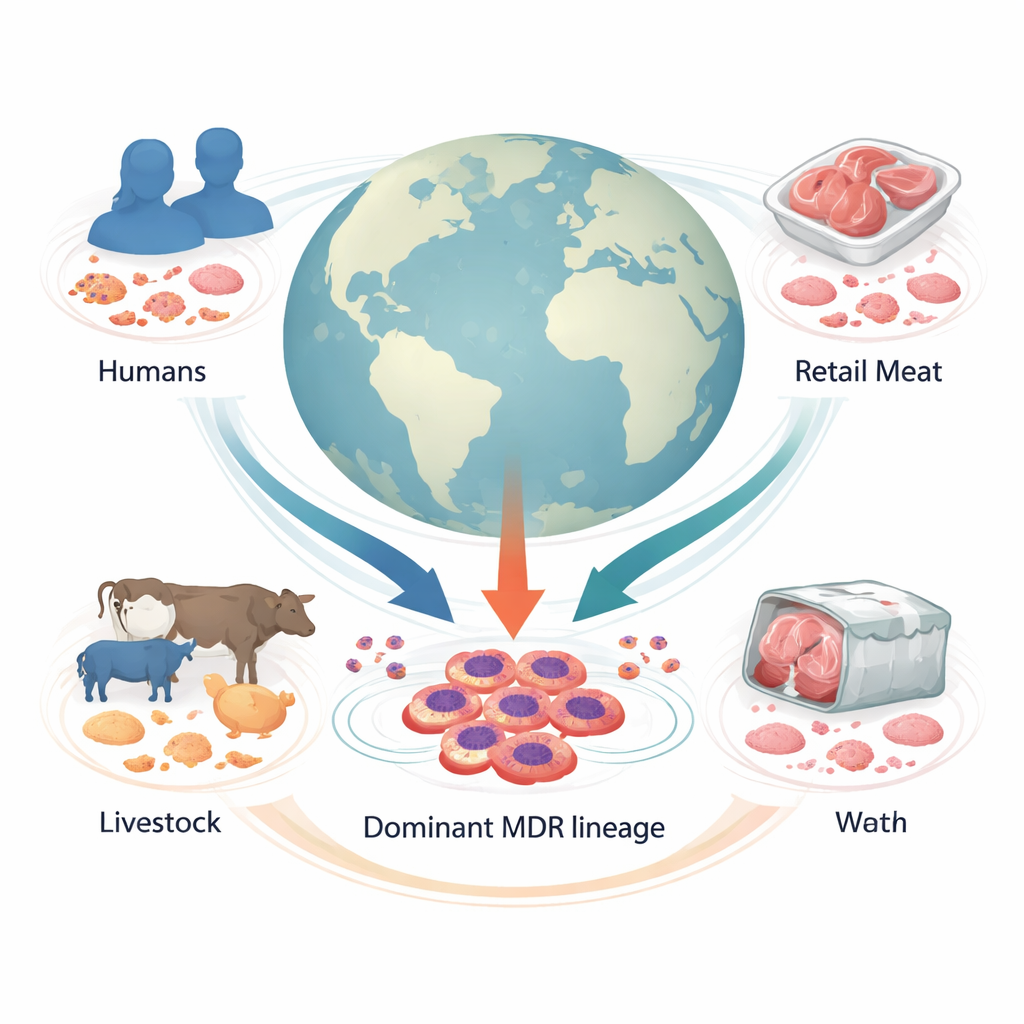
Globalne spojrzenie na ukryte zagrożenie
Naukowcy zebrali genomy z 1 142 próbek Proteus mirabilis pobranych w 34 krajach od ludzi, zwierząt hodowlanych, mięsa sprzedawanego w handlu detalicznym oraz z innych środowisk. Porównując pełne genomy, pogrupowali bakterie w 178 rodzin genetycznych. Jedna wyróżniała się szczególnie: „Klustera-1”, główna linia, która stanowiła jedną piątą wszystkich próbek i obejmowała szczepy z oddziałów szpitalnych na kilku kontynentach. Większość tych szczepów pochodziła od ludzi, ale znaczący udział stanowiły też izolaty ze zwierząt gospodarskich i mięsa, co wskazuje, że ta linia przemieszcza się między gatunkami i wzdłuż łańcucha żywnościowego.
Linia uzbrojona w liczne tarcze przeciwko lekom
Gdy zespół przeskanował genomy w poszukiwaniu genów oporności na antybiotyki, Klastra-1 miała zauważalnie cięższy ładunek. Średnio poszczególne jej członki nosiły prawie 18 genów oporności każdy, znacznie więcej niż inne linie. Wśród nich znajdowały się geny unieszkodliwiające niektóre z naszych najsilniejszych antybiotyków, jak karbapenemy, często zarezerwowane jako leki ostatniej szansy. Wiele z tych genów oporności znajduje się wewnątrz dużej „wyspy” DNA zwanej PmGRI1, która może przenosić się między bakteriami. Niektóre wersje tej wyspy niosą jednocześnie ponad 20 genów oporności, skutecznie zmieniając Proteus w chodzącą aptekę obrony i pozostawiając lekarzy z niewieloma opcjami leczenia.
Lepkie cechy, które pomagają bakteriom przetrwać
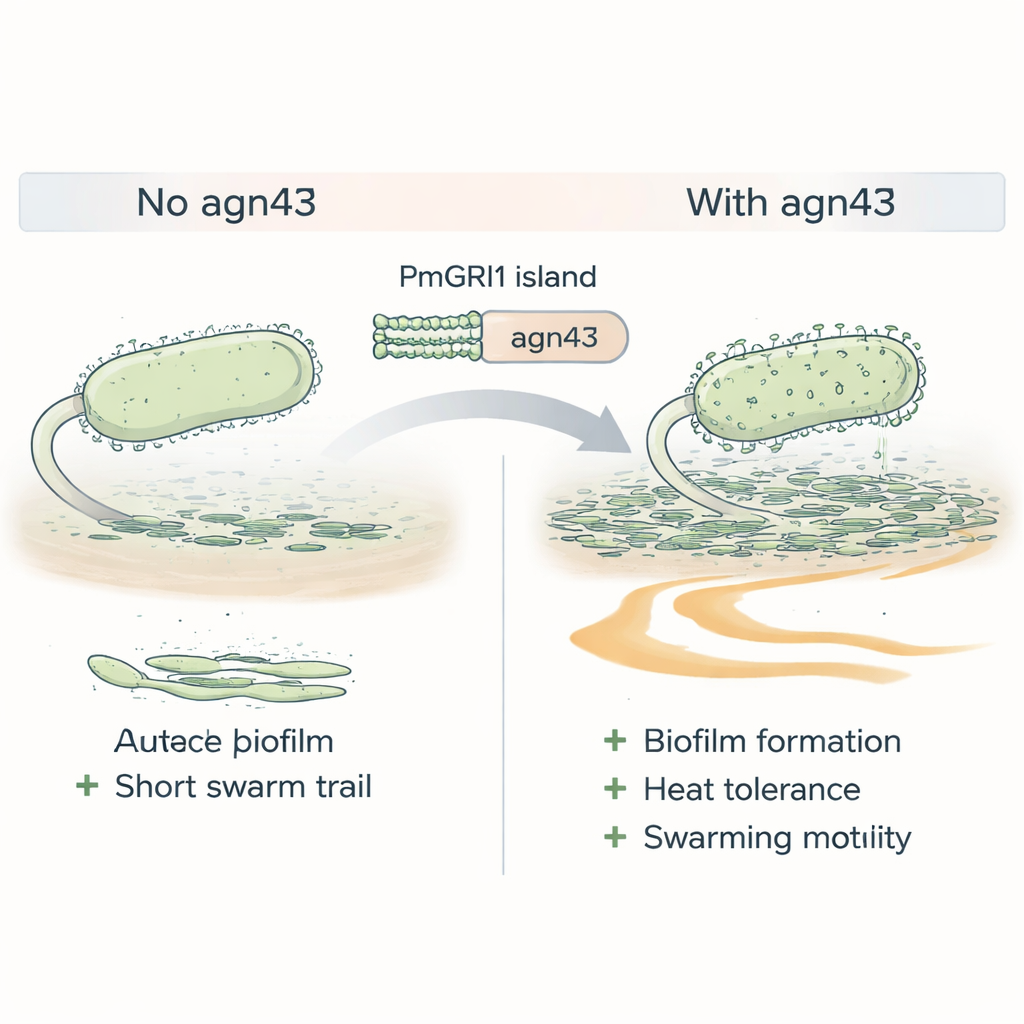
Sama oporność nie gwarantuje sukcesu; bakterie muszą też dobrze przetrwać w organizmie i środowisku szpitalnym. Szczepy Klastra-1 były wzbogacone w geny związane z przyczepianiem się do komórek i tworzeniem biofilmów — śliskich społeczności, które chronią bakterie przed lekami i układem odpornościowym. Jednym wyróżniającym się genem na wyspie PmGRI1, nazwanym agn43, jest gen kodujący białko powierzchniowe działające jak molekularne rzepy, pomagające komórkom zlepiać się razem. Gdy naukowcy usunęli agn43 w szczepie z Klastra-1, mutant tworzył słabsze biofilmy, gorzej znosił stres cieplny i mniej efektywnie rozprzestrzeniał się powierzchniowo, czyli cechy, które normalnie pomagają Proteus kolonizować cewniki moczowe i rozprzestrzeniać się w drogach moczowych.
Jak i gdzie ta super-linia się rozprzestrzeniła
Łącząc różnice genetyczne z datami izolacji, badacze zrekonstruowali linię czasu dla Klastra-1. Oszacowali, że jego najbliższy wspólny przodek pojawił się około 1910 roku, dekady przed powszechnym użyciem nowoczesnych antybiotyków. Linia później rozdzieliła się na dwie medycznie istotne gałęzie: jedną głównie obserwowaną w Chinach, niosącą gen rozkładający karbapenemy zwany blaKPC-2, oraz drugą głównie w Stanach Zjednoczonych z pokrewnym genem blaIMP-27. Od końca lat 80. XX wieku Klastra-1 gwałtownie się rozrastała i wielokrotnie wykrywano jej przemieszczanie między krajami oraz między ludźmi, zwierzętami hodowlanymi i mięsem, co podkreśla jej potencjał epidemiczny.
Co to oznacza dla pacjentów i zdrowia publicznego
Dla osoby niebędącej specjalistą komunikat jest taki: określona rodzina Proteus mirabilis przekształciła się w wysoce skutecznego zarazka szpitalnego, łącząc dwie korzyści — grubą zbroję genów oporności na antybiotyki oraz dodatkową „lepkość”, która pomaga tworzyć ochronne warstwy i utrzymywać się na cewnikach i tkankach. Takie połączenie sprawia, że infekcje są trudniejsze do leczenia i łatwiejsze do rozprzestrzeniania. Praca ta podkreśla potrzebę ścisłego genetycznego nadzoru tej linii zarówno w szpitalach, jak i w rolnictwie, zaostrzenia kontroli zakażeń związanych z cewnikami oraz ostrożnego stosowania antybiotyków, aby spowolnić wzrost i globalny rozprzód tych wieloopornych szczepów.
Cytowanie: Zhang, T., Wei, H., Ju, Z. et al. Genomic survey uncovers the emergence of a multidrug-resistant dominant lineage in Proteus mirabilis populations. npj Antimicrob Resist 4, 17 (2026). https://doi.org/10.1038/s44259-026-00189-5
Słowa kluczowe: oporność na antybiotyki, zakażenie dróg moczowych, zakażenia szpitalne, genomika bakteryjna, biofilm