Clear Sky Science · pl
Synergia fag–meropenem przeciwko klinicznym izolatom Klebsiella pneumoniae produkującym OXA-48
Dlaczego małe wirusy mogą uratować nieskuteczne antybiotyki
Szpitale na całym świecie zmagają się z zakażeniami, które przestały reagować na nasze najsilniejsze antybiotyki. Jednym z najgroźniejszych sprawców jest bakteria Klebsiella pneumoniae, mogąca wywoływać zapalenie płuc, zakażenia krwi i układu moczowego. W badaniu sprawdzono, czy starannie dobrane wirusy atakujące bakterie — tzw. fagi — mogą współdziałać z silnym antybiotykiem meropenemem, by wyeliminować wysoce oporne szczepy zagrażające dziś pacjentom.
Podstępny szpitalny zarazek w natarciu
Klebsiella pneumoniae stała się poważnym szpitalnym „superbakterią”, ponieważ wiele szczepów nauczyło się oporności na karbapenemy — rodzinę antybiotyków stosowanych jako ostateczna linia obrony. Bakterie te często noszą geny odporności na małych krążkach DNA zwanych plazmidami, które mogą wymieniać między sobą jak karty kolekcjonerskie. Jeden z takich plazmidów, znany jako pOXA-48, koduje enzym rozkładający karbapenemy, przez co leki takie jak meropenem stają się w dużej mierze nieskuteczne. W miarę jak te plazmidy rozprzestrzeniają się w wysokiego ryzyka klonach bakteryjnych w Europie i dalej, standardowe terapie stają się mniej pewne, a nawet rutynowe zabiegi medyczne — bardziej ryzykowne.
Rekrutacja fagów jako precyzyjnych najeźdźców
Ponieważ nowe antybiotyki pojawiają się powoli, naukowcy zwracają się ku terapii fagowej — wykorzystaniu wirusów, które specyficznie zakażają i zabijają bakterie. W tym badaniu zespół skupił się na litycznym fagu nazwanym vB_Kpn_2-P4, który potrafi zainfekować szeroki zestaw klinicznych izolatów Klebsiella zebranych ze szpitali hiszpańskich. W testach laboratoryjnych fag ten atakował bakterie niosące różne mechanizmy oporności na karbapenemy. Jednak, jak często bywa i w przypadku antybiotyków, i fagów, niektóre komórki bakteryjne ostatecznie przetrwały i odrosły, co podkreśla potrzebę strategii łączonych zamiast polegania na jednym środku.
Kiedy lek i wirus działają lepiej razem
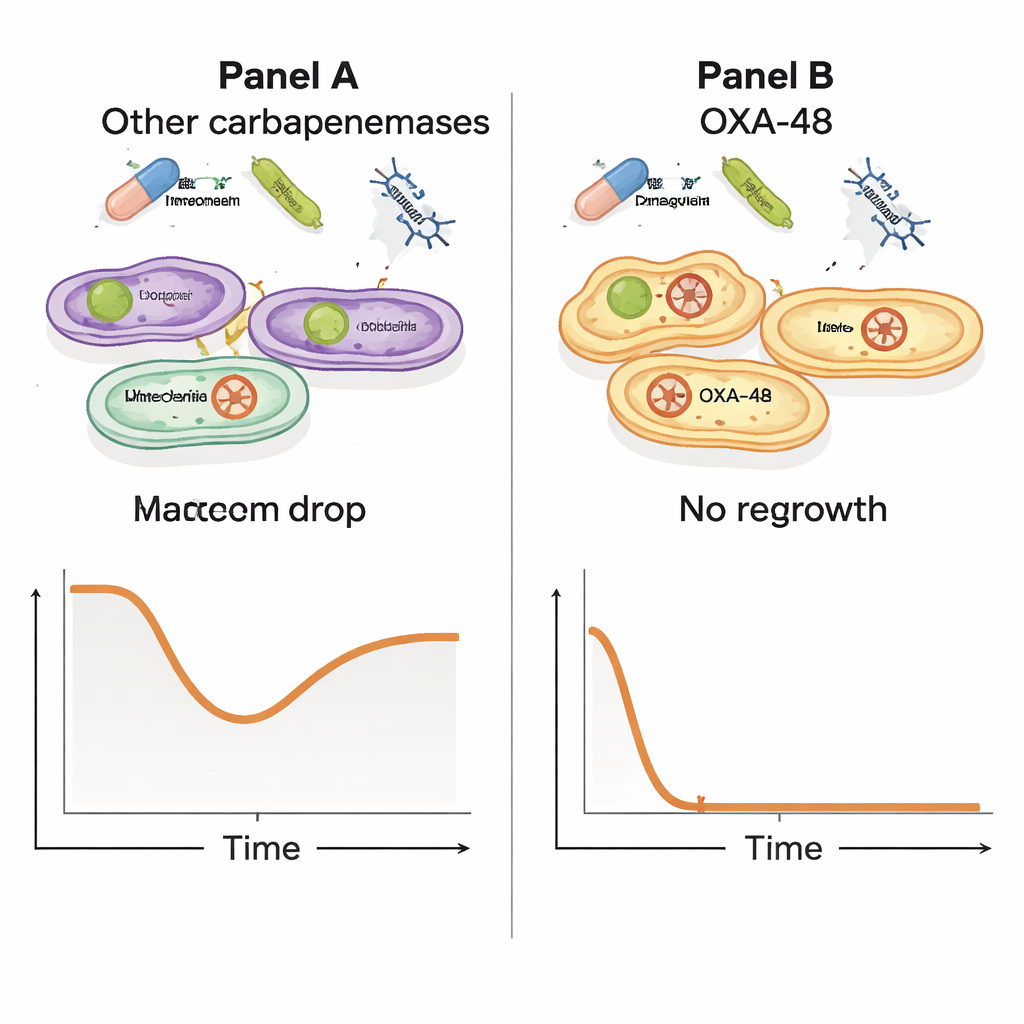
Naukowcy przetestowali następnie, jak meropenem i fag zachowują się stosowane łącznie. Hodowali dwanaście opornych izolatów i wystawili je na działanie meropenemu samego, fagu samego oraz obu jednocześnie, śledząc wzrost przez wiele godzin. Choć wszystkie izolaty tolerowały meropenem w warunkach testu, pojawił się uderzający wzorzec: w szczepach niosących plazmid OXA‑48 kombinacja fagu i wysokiej dawki meropenemu spowodowała dramatyczny spadek liczby bakterii, po którym nie odnotowano wykrywalnego odrostu. Przy niższych stężeniach meropenemu te szczepy OXA‑48 nadal wykazywały silny spadek obciążenia bakteryjnego. Natomiast szczepy z innymi enzymami odpornościowymi nie pokazały takiego potężnego efektu wspólnego, co sugeruje, że jakaś szczególna cecha plazmidu OXA‑48 sprawia, iż bakterie są wyjątkowo wrażliwe, gdy stają naraz wobec obu zagrożeń.
Śledzenie ukrytego genetycznego pomocnika
Aby zrozumieć, dlaczego jedynie producenci OXA‑48 wykazywali tę synergię, zespół porównał genom różnych izolatów bakteryjnych. Zidentyfikowali dziesiątki genów powiązanych z odpowiedzią synergiczną, niemal wszystkie skupione na plazmidzie pOXA‑48. Co ważne, gdy wyizolowali bakterie, które ewoluowały odporność na faga, te przetrwałe nadal nosiły nienaruszony gen OXA‑48; nie pozbyły się plazmidu, żeby uciec. To wskazuje na subtelniejszy obraz, w którym plazmid dający odporność na leki nakłada jednocześnie ukryte koszty na biologię bakterii — koszty, które stają się śmiertelne, gdy fag i antybiotyk uderzają jednocześnie, przechylając szalę przeciw patogenowi.
Co to może znaczyć dla przyszłych terapii
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że genetyczne sztuczki bakterii służące do unikania naszych leków mogą czasem zostać obrócone przeciw nim. W tym przypadku specyficzny plazmid oporności wydaje się czynić niektóre szczepy Klebsiella nadzwyczaj wrażliwymi na skoordynowany atak dopasowanego fagu i meropenemu. Choć prace przeprowadzono w warunkach laboratoryjnych i potrzebne są dalsze badania na modelach zwierzęcych i u pacjentów, wyniki sugerują, że dobranie odpowiedniego faga do właściwego profilu oporności mogłoby przywrócić działanie antybiotyków, które wydawały się utracić moc. Zamiast zastępować antybiotyki, fagi mogą stać się sprytnymi sojusznikami, pomagającymi przechytrzyć superbakterie, które kiedyś wydawały się nie do pokonania.
Cytowanie: Cantallops, I., Ferriol-González, C., Barcos-Rodríguez, T. et al. Phage-meropenem synergy against OXA-48-producing Klebsiella pneumoniae clinical isolates. npj Antimicrob Resist 4, 12 (2026). https://doi.org/10.1038/s44259-026-00186-8
Słowa kluczowe: terapia fagowa, oporność na antybiotyki, Klebsiella pneumoniae, plazmid OXA-48, synergia z meropenemem