Clear Sky Science · pl
Genomowy pejzaż oporności na leki przeciwbakteryjne w Indiach: wyniki badania nadzorczego obejmującego wiele gatunków
Dlaczego problem superbakteryjny w Indiach ma znaczenie dla nas wszystkich
Antybiotykooporne „superbakterie” to rosnące globalne zagrożenie, ale wciąż wiemy zaskakująco niewiele o tym, jak te drobnoustroje ewoluują i rozprzestrzeniają się w wielu rejonach świata. To badanie przygląda się dokładnie niebezpiecznym bakteriom z indyjskich szpitali i odczytuje ich pełne DNA, aby zrozumieć, jak potrafią omijać nasze najsilniejsze leki. Wyniki nie tylko ujawniają, co sprawia, że te mikroby są tak trudne do eliminacji, lecz także sprawdzają, czy szybkie metody oparte na DNA mogą wiarygodnie zastąpić wolniejsze testy laboratoryjne — kwestia mająca wpływ na leczenie zakażeń na całym świecie.
Dokładniejsze spojrzenie na infekcje szpitalne
Naukowcy zebrali 266 izolowanych próbek bakterii od ciężko chorych pacjentów w dużych szpitalach północnych i zachodnich Indii w latach 2022–2024. Większość próbek pochodziła z krwi, ale także z moczu i zakażeń płuc, a przeważająca część pochodziła z oddziałów intensywnej opieki, gdzie pacjenci są najbardziej narażeni. Zespół skupił się na znanych problematycznych patogenach — takich jak Escherichia coli, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa, metycylinooporny Staphylococcus aureus (MRSA) oraz wankomycynooporne Enterococcus (VRE). Dla każdej próbki lekarze przeprowadzili standardowe badania wrażliwości na antybiotyki, które polegają na wystawieniu bakterii na działanie leków w laboratorium, by sprawdzić, które środki nadal działają. Naukowcy następnie zsekwencjonowali genomy bakterii, aby zmapować pełen zestaw genów oporności i porównali to, co DNA „przewidywało”, z wynikami testów laboratoryjnych.
Gdy geny i probówki się nie zgadzają
Porównując predykcje genetyczne z wynikami laboratoryjnymi dla 56 różnych antybiotyków, badanie wykonało ponad 5000 porównań. W większości przypadków metoda oparta na DNA i tradycyjne testy zgadzały się, ale niemal 600 rozbieżności było wyróżniających się. Najczęstszym typem błędu było to, że narzędzie genomowe przewidywało oporność, podczas gdy test laboratoryjny wskazywał, że bakteria nadal jest wrażliwa. Działo się tak często dla leków takich jak minocyklina, kolistyna i gentamycyna, szczególnie w E. coli. Odwrotny typ błędu — gdy test wykazywał oporność, a geny tego wprost nie tłumaczyły — był rzadszy, lecz bardziej niepokojący, ponieważ grozi przeoczeniem oporności. Te „bardzo poważne” rozbieżności występowały szczególnie u jelitowych bakterii zwanych enterokokami, zwłaszcza względem powszechnie stosowanych leków podobnych do penicylin oraz kombinacji trimetoprim‑sulfametoksazol.
Ukryte arsenały w DNA bakterii
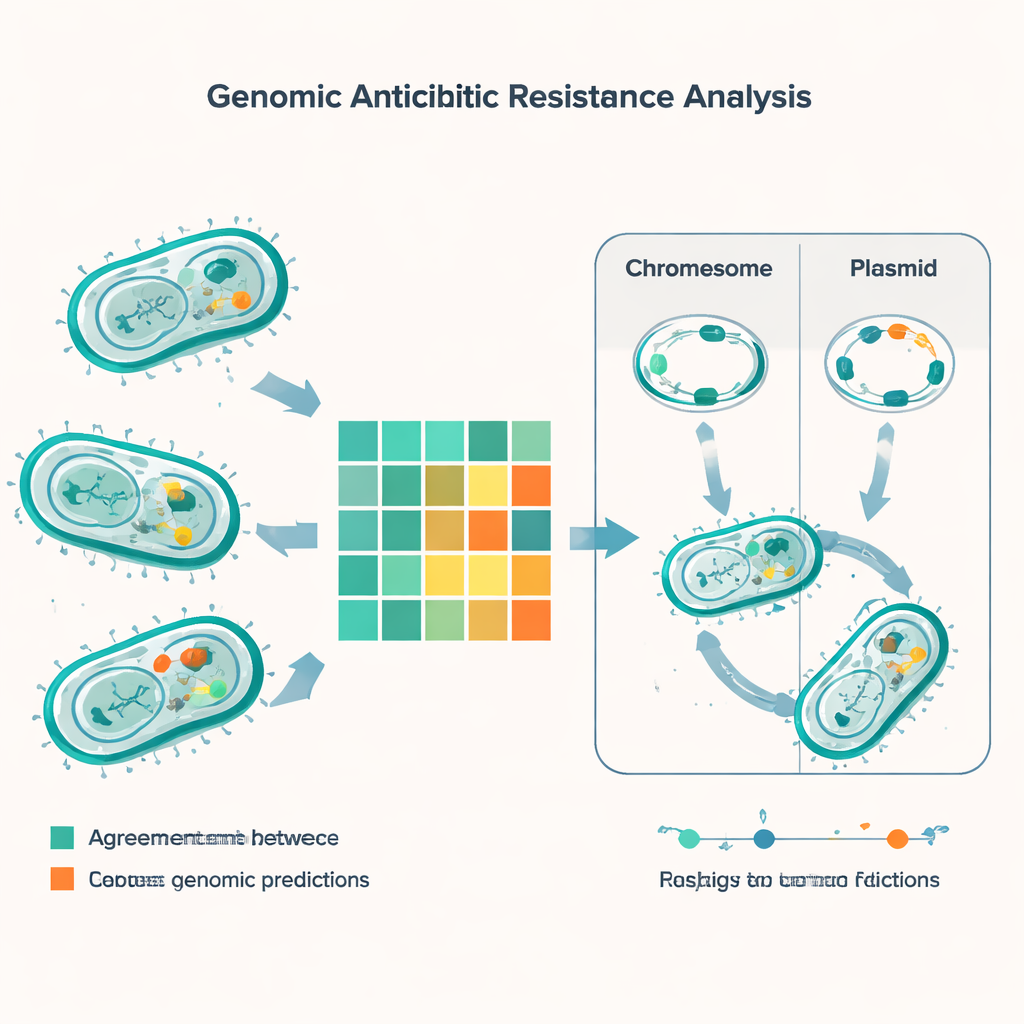
Przegląd genomowy ujawnił gęsty zestaw genów oporności w głównych gatunkach. Każdy z powszechnych patogenów Gram‑ujemnych nosił co najmniej jeden gen beta‑laktamazy, który może rozkładać penicyliny i pokrewne leki, a wiele szczepów miało jednocześnie kilka takich genów. Notoryczne czynniki, takie jak karbapenemazy typu NDM — neutralizujące antybiotyki ostatniej linii — były powszechne w E. coli, Klebsiella, Acinetobacter i Pseudomonas. Badanie wykryło także geny pomagające bakteriom przetrwać wobec silnych antybiotyków peptydowych, takich jak kolistyna, a także klasyczny gen mecA nadający MRSA oporność na metycylinę i klastry odpowiedzialne za oporność na wankomycynę u enterokoków. Porównując genetyczne odciski palców zwane typami sekwencyjnymi, zespół powiązał niektóre z tych genów oporności z znanymi, wysokiego ryzyka liniami bakteryjnymi, które już rozprzestrzeniają się w Indiach i na świecie.
Wymiana genów za pomocą mobilnego DNA
Kluczowa część historii leży nie tylko w tym, które geny bakterie niosą, lecz także gdzie te geny się znajdują. Wiele genów oporności znajduje się na małych krążkach DNA zwanych plazmidami, które bakterie mogą wymieniać jak karty kolekcjonerskie. Przy użyciu specjalistycznego oprogramowania badacze przewidzieli około 1400 plazmidów w badanych próbkach, z wyjątkowo wysoką różnorodnością w E. coli i Klebsiella. W tych gatunkach duża część genów oporności — w tym kilka kluczowych beta‑laktamaz — była przenoszona przez plazmidy, co ułatwia ich przekazywanie między szczepami, a nawet między gatunkami. Inne cechy oporności były zintegrowane w chromosomach bakterii, co oznacza, że mogą utrzymywać się nawet po utracie plazmidów. Zespół skatalogował także elementy genetyczne mobilne — krótkie segmenty DNA, które mogą przeskakiwać i zabierać ze sobą geny oporności — podkreślając kolejny mechanizm szybkiego rozprzestrzeniania się.
Co to oznacza dla przyszłego leczenia
Dla osób niebędących specjalistami główne przesłanie jest takie, że odczytywanie DNA bakterii może znacznie wspomóc walkę z superbakteriami, ale technologia nie jest jeszcze perfekcyjna. Narzędzia genomowe miały tendencję do „przewidywania” oporności z nadmiarem, co jest bezpieczniejsze niż przeoczenie niebezpiecznego szczepu, lecz może skłaniać lekarzy do użycia silniejszych leków niż konieczne. Jednocześnie mniejsza liczba przypadków pokazała, że testy laboratoryjne wykrywały oporność, której obecne katalogi genów nie były w stanie w pełni wyjaśnić, co uwypukla istotne luki w naszej wiedzy. Tworząc szczegółową mapę genów oporności, plazmidów i elementów mobilnych w indyjskich szpitalach, to badanie daje podstawy do lepszych, szybszych diagnostyk opartych na DNA i bardziej świadomego stosowania antybiotyków — nie tylko w Indiach, lecz w każdym miejscu, gdzie superbakterie zagrażają współczesnej medycynie.
Cytowanie: Gheewalla, N., Karthikeyan, V., Jadhav, Y. et al. Genomic landscape of antimicrobial resistance in India: findings from a multi-species surveillance study. npj Antimicrob Resist 4, 13 (2026). https://doi.org/10.1038/s44259-026-00185-9
Słowa kluczowe: oporność na antybiotyki, sekwencjonowanie genomu, infekcje szpitalne, oporne na leki bakterie, oporność przenoszona przez plazmidy