Clear Sky Science · pl
Globalna odpowiedź na ekspozycję na antybiotyk ujawnia kluczową rolę metabolizmu nukleotydów w wysokopoziomowej tolerancji na β-laktamy
Dlaczego niektóre bakterie lekceważą nasze najlepsze antybiotyki
Antybiotyki mają eliminować szkodliwe bakterie, a mimo to wiele infekcji uporczywie się utrzymuje lub powraca po leczeniu. Artykuł bada jedną mniej docenianą przyczynę: niektóre bakterie potrafią się wycofać i tymczasowo przetrwać nawet bardzo wysokie dawki silnych leków, takich jak penicylina. Odkrywając, jak te mikroby przeorganizowują swoją wewnętrzną chemię, by przetrwać atak, badacze wskazują nowe sposoby, które mogą przywrócić skuteczność istniejących antybiotyków.
Skryty trik przetrwania wewnątrz zakażeń
Po wystawieniu na działanie antybiotyków beta-laktamowych, takich jak penicylina, wiele niebezpiecznych bakterii Gram-ujemnych nie ginie natychmiast. Zamiast tego mogą zrzucić sztywną ścianę komórkową i przekształcić się w kruche, okrągłe formy zwane sferoplastami. W tej postaci przestają się dzielić, ale pozostają żywe i metabolicznie aktywne. Gdy lek znika, odbudowują ścianę, wracają do normalnego, pręcikowatego kształtu i mogą ponownie wywołać infekcję. Ponieważ ta „tolerancja” jest krokiem w kierunku pełnej oporności na antybiotyki i niepowodzeń terapii, zrozumienie, jak sferoplasty przetrwają, jest kluczowe dla medycyny przyszłości.
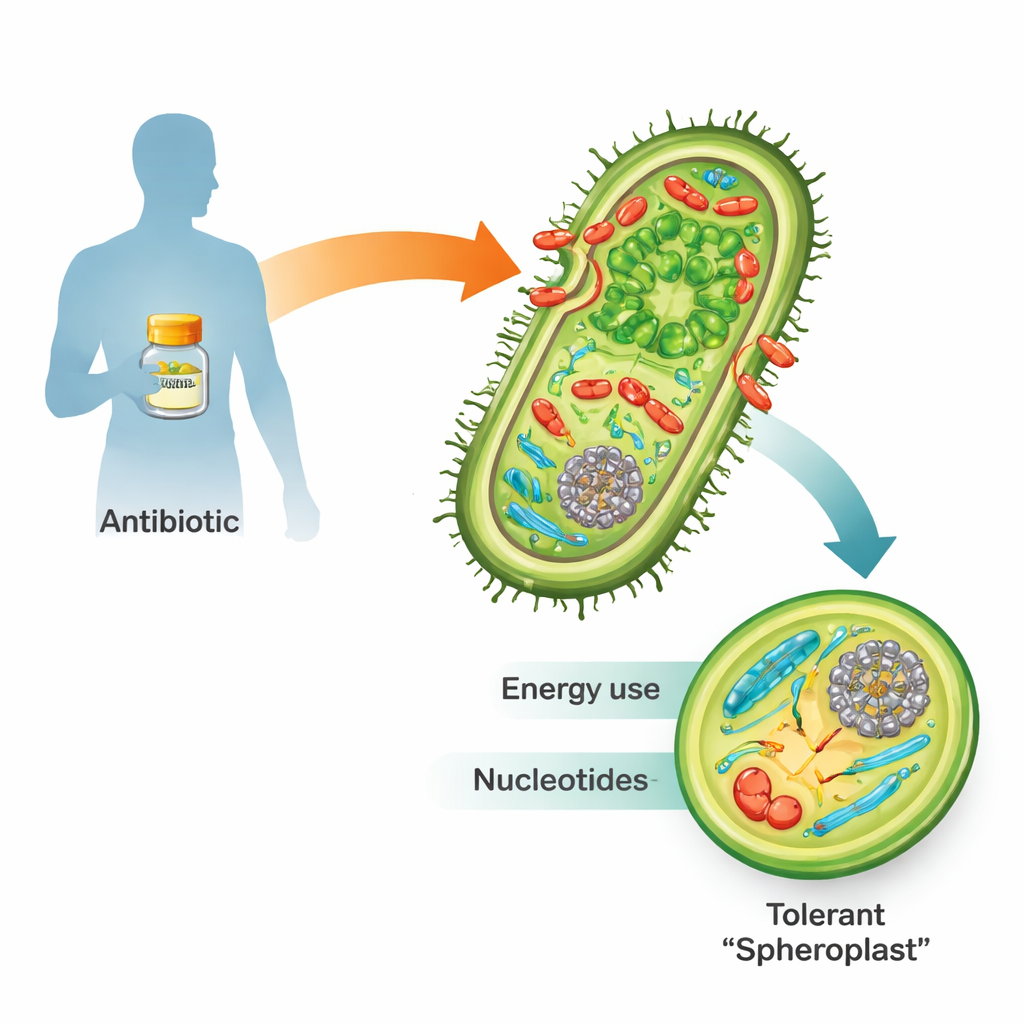
Podsłuchiwanie komórkowego alarmu
Zespół użył Vibrio cholerae, bakterii wywołującej cholerę, jako modelu, ponieważ jest ona wyjątkowo tolerancyjna na beta-laktamy i łatwa do manipulacji genetycznej. Narażono bakterie na dziesięciokrotność minimalnej dawki zabójczej penicyliny i śledzono odpowiedź w czasie za pomocą dwóch potężnych narzędzi. Transkryptomika wykrywała, które geny były włączane lub wyłączane, a metabolomika mierzyła setki małych cząsteczek, które napędzają i budują komórkę. Razem techniki „multi-omiczne” stworzyły mapę w czasie pokazującą, jak tolerancyjna komórka przebudowuje swoje wewnętrzne procesy podczas ataku leku.
Przekierowanie metabolizmu i ukryty słaby punkt
Dane ujawniły rozległe zmiany w kluczowych szlakach. Geny odpowiedzialne za budowę ściany komórkowej zostały silnie włączone, co zgadza się z próbą naprawy uszkodzeń i przygotowania do odbudowy. Systemy reakcji na gorączkę i stres również się załączyły, prawdopodobnie radząc sobie z niepoprawnie sfałdowanymi lub zoksydowanymi białkami powstałymi wskutek stresu wywołanego antybiotykiem. Jednocześnie centralny metabolizm węglowodanów przesunął się: niektóre etapy cyklu TCA (głównego generatora energii komórki) zostały wzmocnione, podczas gdy kluczowe pośrednie produkty glikolizy, takie jak glukozo-6-fosforan i fruktozo-6-fosforan, zostały dramatycznie wyczerpane. Te pośrednie związki zwykle zasilają zarówno produkcję energii, jak i syntezę ściany komórkowej, co sugeruje, że ciągłe, marnotrawne „bezowocne cykle” materiału ściany drenują zasoby.
Nukleotydy pod presją
Najbardziej uderzającą zmianą były zmiany w nukleotydach — cegiełkach DNA, RNA i wielu przenośników energii. Poziomy wielu nukleotydów i ich prekursorów gwałtownie spadły w komórkach traktowanych penicyliną, mimo że geny do ich de novo syntezy były silnie aktywowane. Jednocześnie geny związane z „recyklingiem” nukleotydów zostały przyciszone, jakby komórka próbowała zachować to, co jeszcze pozostało. Wzorce te sugerowały, że sferoplasty znajdują się pod silnym stresem nukleotydowym. Gdy badacze celowo zakłócili szlaki dostarczające prekursorów nukleotydów — na przykład szlak pentozowy — lub zablokowali produkcję nukleotydów innym lekiem, trimetoprimem, połączenie z beta-laktamami zabiło znacznie więcej bakterii niż którykolwiek z leków osobno. Silna synergia została zaobserwowana nie tylko w Vibrio cholerae, lecz także w wysoko tolerancyjnych klinicznych szczepach Klebsiella pneumoniae i Escherichia coli.
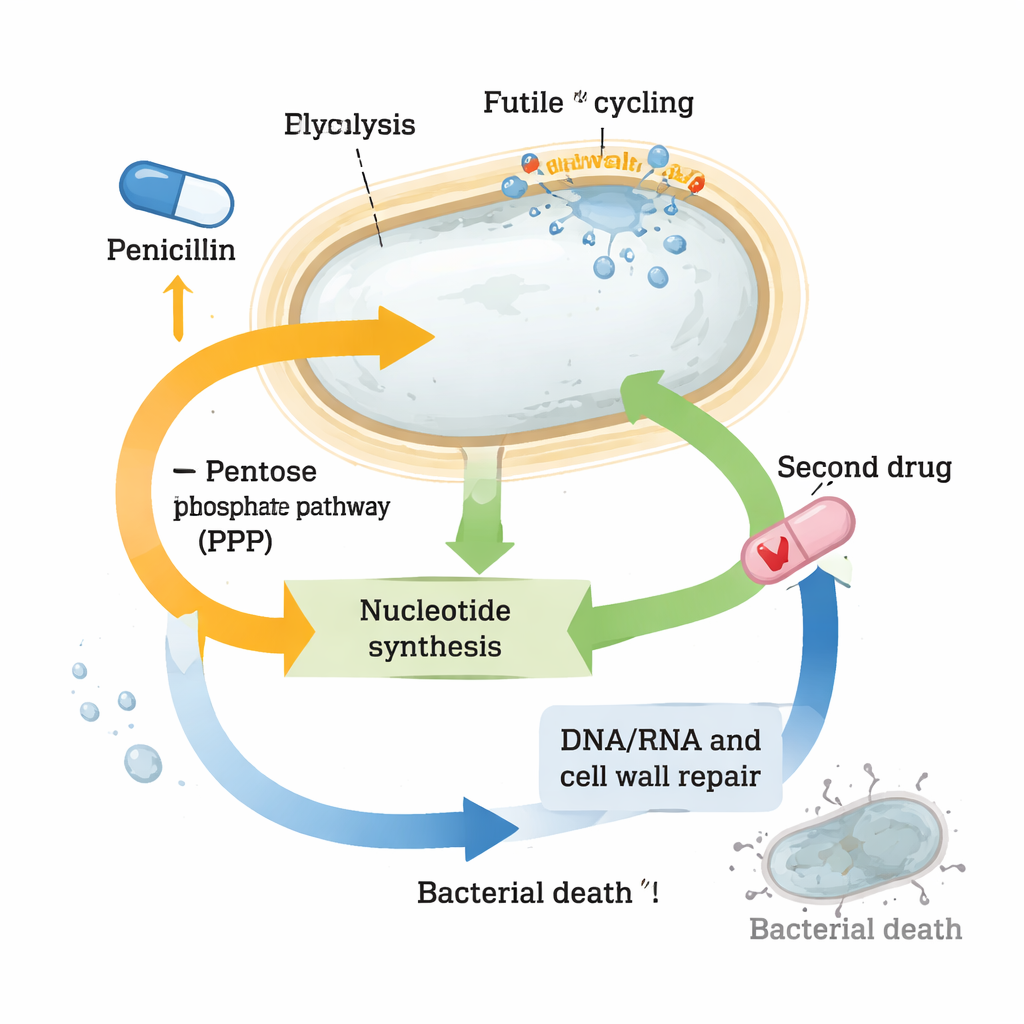
Przekształcanie chemii przetrwania w przewagę terapeutyczną
Pomimo znacznej przebudowy metabolizmu, tolerancyjne sferoplasty utrzymują względnie stabilny poziom nośnika energii ATP i unikają katastrofalnych uszkodzeń, co pomaga im przetrwać długie ekspozycje na antybiotyki. Jednak praca pokazuje, że robiąc to, doprowadzają swoje pule nukleotydów niemal do granicy. Ta chwiejna równowaga tworzy podatność: delikatne przesunięcie metabolizmu nukleotydów drugim lekiem powoduje załamanie ich obrony i przywraca silne działanie bakteriobójcze. Dla czytelników niebędących specjalistami wniosek jest taki, że niektóre bakterie przetrwają antybiotyki nie dlatego, że leki nie trafiają w cele, lecz dlatego, że komórki szybko przeorganizowują swoją chemię, by przetrwać cios. Znajdując i wykorzystując słabe ogniwa tej sieci przetrwania — tutaj metabolizm nukleotydów — badacze mogą powstrzymać stare antybiotyki przedają się w potężne terapie skojarzone, które przechytrzą nawet wysoce tolerancyjne patogeny.
Cytowanie: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
Słowa kluczowe: tolerancja na antybiotyki, antybiotyki beta-laktamowe, metabolizm nukleotydów, przetrwanie bakterii, kombinacje leków