Clear Sky Science · pl
Uczenie maszynowe ułatwiające akustyczne pułapkowanie w czasie rzeczywistym w zmiennych, wielowarstwowych środowiskach z myślą o manipulacji mikropęcherzykami prowadzonych za pomocą obrazowania rezonansem magnetycznym
Prowadzenie mikroskopijnych nośników leków za pomocą dźwięku i skanów
Nowoczesne terapie przeciwnowotworowe coraz częściej opierają się na inteligentnych nośnikach leków, które mogą dostarczać substancję leczniczą bezpośrednio do guzów, oszczędzając zdrową tkankę. W tym badaniu badacze eksplorują futurystyczny sposób kierowania takimi nośnikami wewnątrz ciała przy użyciu ultradźwiękowych „pułapek” prowadzonych obrazowaniem rezonansem magnetycznym (MRI). Poprzez połączenie fal dźwiękowych, obrazowania medycznego i uczenia maszynowego, autorzy dążą do utrzymania mikroskopijnych pęcherzyków nośników leków w pobliżu poruszających się guzów, nawet gdy ciało przesuwa się przy każdym oddechu.
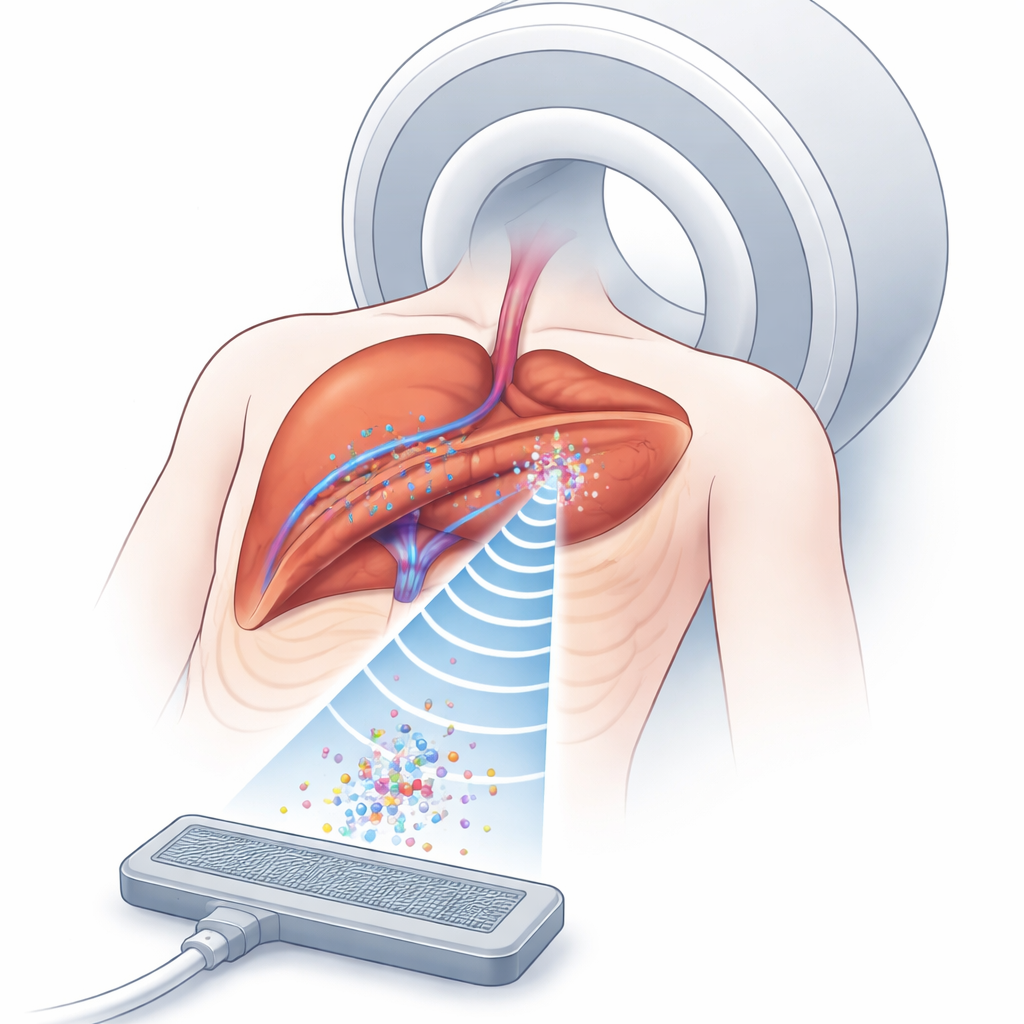
Dlaczego zatrzymywanie mikroskopijnych pęcherzyków ma znaczenie
Mikropęcherzyki przenoszące leki przemieszczają się w naczyniach krwionośnych i mogą uwalniać ładunek po wywołaniu ultradźwiękami. Wyzwanie polega na utrzymaniu wystarczającej liczby tych pęcherzyków w odpowiednim miejscu, wystarczająco długo, głęboko wewnątrz ciała. Ultradźwięki potrafią tworzyć niewidoczne kieszenie siły — akustyczne pułapki — które utrzymują małe obiekty w płynie bez bezpośredniego kontaktu. MRI z kolei widzi zarówno tkankę, jak i wzorzec efektów ultradźwięków, nawet wewnątrz narządów. Połączenie tych dwóch narzędzi pozwala koncentrować nośniki leków wokół guzów precyzyjniej niż sama farmakoterapia. Jednak w rzeczywistych pacjentach tkanki o różnych właściwościach — tłuszcz, mięśnie, narządy i poruszające się płuca — załamują i zniekształcają fale dźwiękowe, co utrudnia utworzenie i utrzymanie stabilnej pułapki dokładnie na lokalizacji guza.
Problem poruszającego się, warstwowego ciała
W prostych środowiskach, takich jak powietrze czy woda, inżynierowie już potrafią używać fazowanych układów emiterów ultradźwięków do pchania, przyciągania i obracania małych obiektów. Wewnątrz ciała jednak dźwięk musi przejść przez wiele warstw o różnej gęstości i prędkości, a granice między nimi powodują załamanie i zniekształcenia. Tradycyjne metody obliczeniowe mogą teoretycznie skorygować te efekty, obliczając, ile czasu dźwięk potrzebuje, aby dotrzeć od każdego emitera do punktu docelowego. Takie podejścia dzielą jednak ciało na miliony drobnych elementów i symulują propagację fal przez każdy z nich — to bardzo czasochłonny proces, który działa jedynie wtedy, gdy tkanki pozostają niemal nieruchome. Sam oddech może przesunąć tkanki w jamie brzusznej o kilka milimetrów, szybko dezaktualizując wcześniej obliczone rozwiązanie.
Nauczanie modelu przewidywania ścieżek dźwięku
Autorzy rozwiązują to ograniczenie za pomocą modelu opartego na uczeniu, który działa jako szybki skrót: zamiast za każdym razem symulować fale dźwiękowe, trenują sieć neuronową do przewidywania, ile czasu potrzebuje każdy impuls ultradźwiękowy, by dotrzeć do punktu docelowego. Najpierw budują szczegółowe środowisko wirtualne używając komory wypełnionej gazem oddzielonej od powietrza cienką plastikową folią, naśladując przejście dźwięku przez różne warstwy tkankowe. Przy użyciu symulatora opartego na fizyce generują zbiór treningowy czasów przelotu dźwięku między wieloma punktami docelowymi a siatką ultradźwiękową 14 na 14. Pozwalają też komorze przesuwać się w dwóch kierunkach, aby imitować ruch, i opisują jej pozycję śledząc trzy wizualne markery, podobnie jak przyszłe markery widoczne w MRI mogłyby monitorować oddech pacjenta. Wyszkolona sieć uczy się mapować żądaną pozycję pułapki oraz położenie komory bezpośrednio na wymagany wzorzec czasowy dla wszystkich 196 emiterów, osiągając dokładność na poziomie mikrosekund w zaledwie około 26 milisekund.
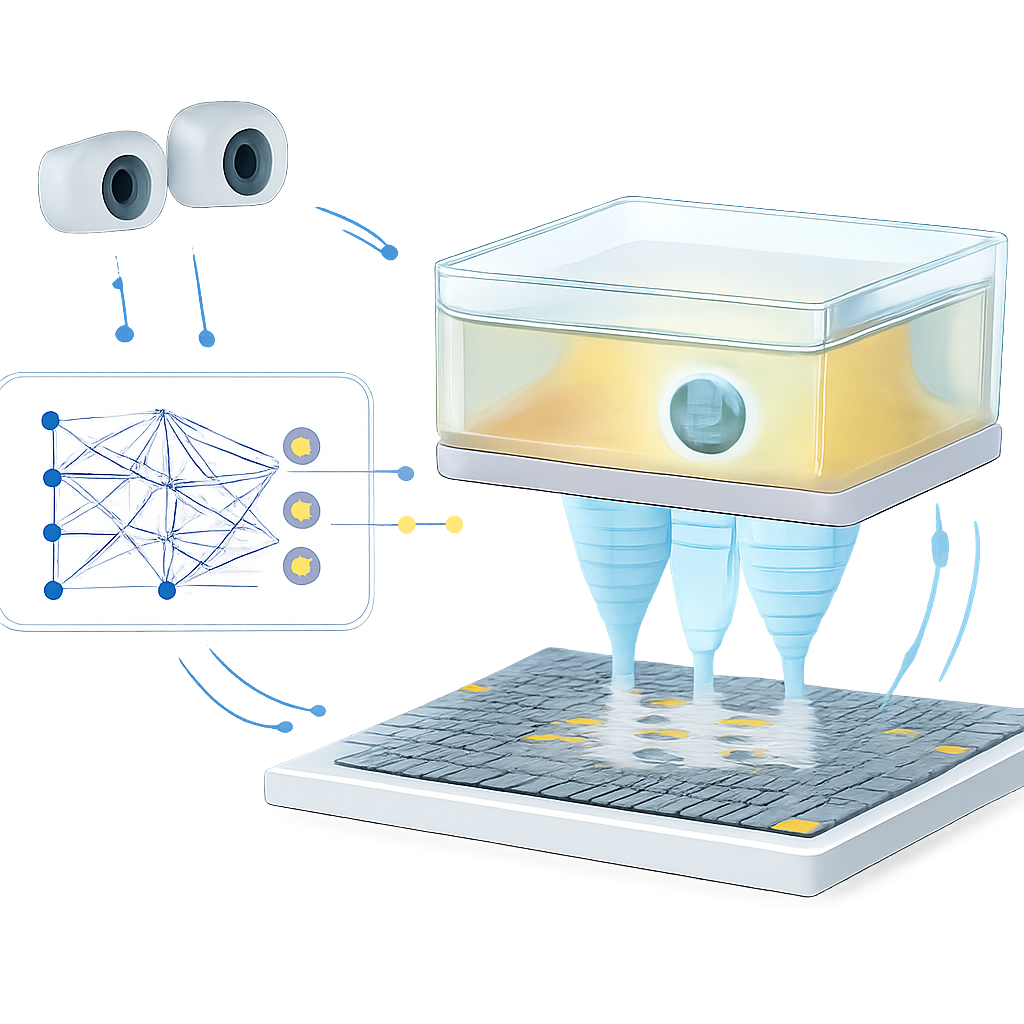
Domykanie pętli za pomocą wizyjnego sprzężenia zwrotnego i szybkich aktualizacji
Samo tempo działania nie wystarcza; pułapka musi też adaptować się, gdy środowisko zmienia się nieoczekiwanie. Aby to pokazać, zespół zbudował system sterowania w pętli zamkniętej. Kamery stereoskopowe obserwują małą kulkę z polistyrenu utrzymaną w powietrzu przez akustyczną pułapkę w poruszającej się komorze. Gdy kulka odpływa od celu poza ustalony próg, system koryguje pozycję docelową, wprowadza zaktualizowane współrzędne i orientację komory do modelu uczącego się i szybko odświeża wzorzec fazowy sterujący siatką. W eksperymentach system może aktualizować wzorzec fazowy do 15 razy na sekundę, kierując kulkę po ścieżkach w kształcie liter H, K i U z średnim błędem około 1 milimetra — porównywalnym z precyzją pozycjonowania niektórych klinicznych systemów ultradźwięków skupionych. Ta sama zasada sprzężenia zwrotnego skraca też czas, przez jaki kulka odbiega od zamierzonego miejsca podczas ruchu komory, pokazując, że pętla sterowania potrafi kompensować ruchy i niezamodelowane efekty pochodzące od folii plastikowej i struktury wsporczej.
Co to oznacza dla przyszłych terapii
Dla osoby niebędącej specjalistą główna wiadomość jest taka, że badacze zbudowali coś w rodzaju zdalnie sterowanego, bezkontaktowego „belamu holowniczego”, który pewnego dnia mógłby zaparkować pęcherzyki z ładunkiem leku w pobliżu guza i utrzymać je tam, mimo że pacjent oddycha. Ich model uczenia maszynowego zastępuje ciężkie symulacje szybkim predyktorem, podczas gdy kamery (a w przyszłości markery MRI) informują system o ruchu ciała, aby pułapka mogła być na bieżąco dostrajana. Chociaż obecna praca wykorzystuje powietrze, gazy i plastik zamiast rzeczywistych tkanek i lewituje plastikową kulkę zamiast prawdziwych mikropęcherzyków, demonstruje sterowanie w czasie rzeczywistym w poruszającym się, warstwowym medium. Przy silniejszym sprzęcie, wyższych częstotliwościach ultradźwięków i śledzeniu ruchu bazującym na MRI, podejście to mogłoby rozwinąć się w narzędzie kliniczne do prowadzonych MRI, wspomaganych robotycznie terapii ultradźwiękowych, które dostarczają leki dokładniej i bezpieczniej głęboko w organizmie.
Cytowanie: Wu, M., Li, X. & Tang, T. Machine learning-facilitated real-time acoustic trapping in time-varying multi-medium environments toward magnetic resonance imaging-guided microbubble manipulation. Commun Eng 5, 52 (2026). https://doi.org/10.1038/s44172-026-00600-z
Słowa kluczowe: akustyczne pułapkowanie, terapia prowadzona za pomocą MRI, dostarczanie leków za pomocą mikropęcherzyków, uczenie maszynowe w ultradźwiękach, nieinwazyjna manipulacja robotyczna