Clear Sky Science · pl
Stłumienie aktywacji nasierdzia i obfitości miofibroblastów poprzez oś Fbln2–Nupr1b pobudza regenerację serca u danio pręgowanego
Dlaczego niektóre serca potrafią się same leczyć
Po zawale u człowieka uszkodzony mięsień zwykle zostaje zasypany sztywną blizną, która nigdy w pełni się nie regeneruje. Danio pręgowane — niewielkie, prążkowane ryby akwariowe — zachowują się inaczej: odrastają tkankę sercową i z czasem usuwają większość blizny. W badaniu postawiono pozornie proste pytanie o dalekosiężnych implikacjach medycznych: skąd serce wie, kiedy budować bliznę, a kiedy ją usuwać, aby mogła odrosnąć nowa tkanka mięśniowa? Odkodowanie tej równowagi u danio może wskazać strategie, które pewnego dnia pomogą uszkodzonym ludzkim sercom naprawić się zamiast pogrążać w niewydolności.
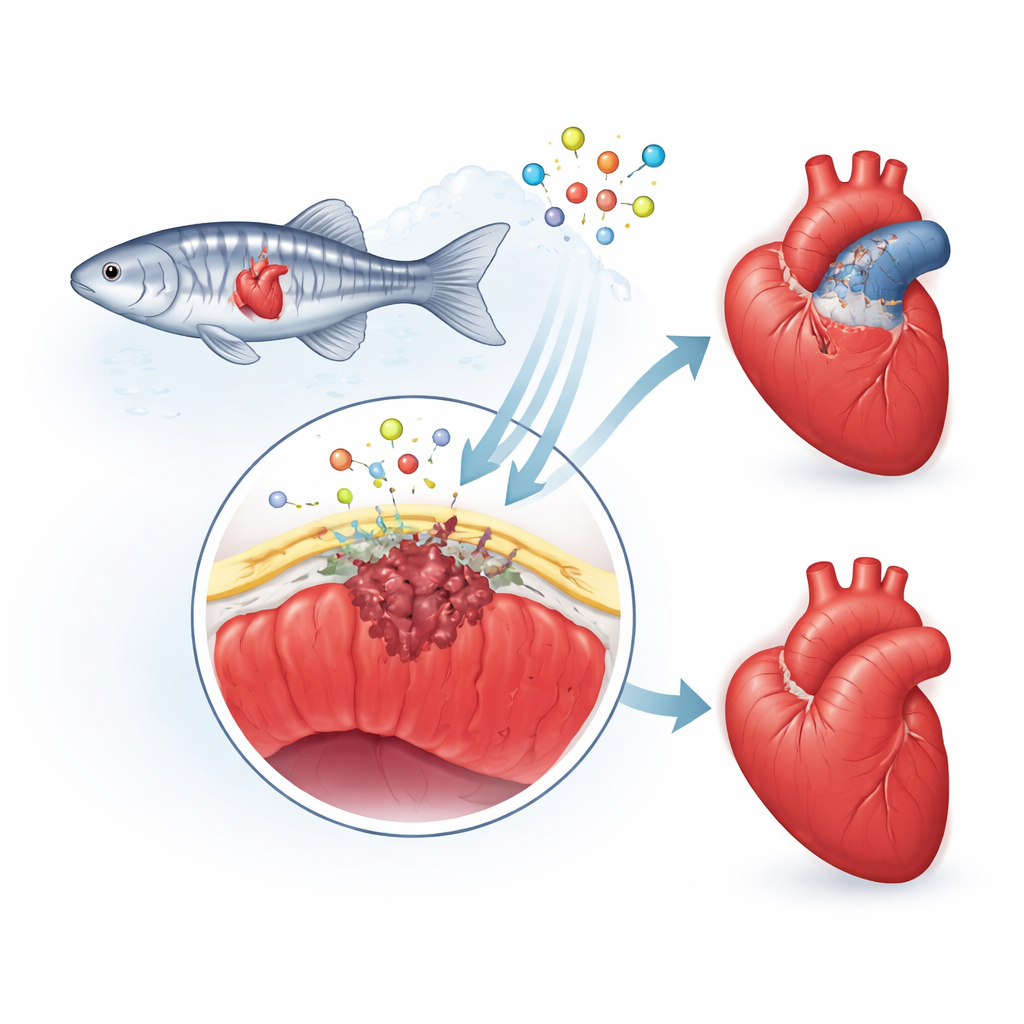
Ochronna zewnętrzna „skóra” serca
Naukowcy skupili się na nasierdziu, cienkiej „skórze” pokrywającej serce. Po urazie ta warstwa uaktywnia się, komórki zmieniają tożsamość i część z nich wnika w obszar uszkodzenia. Tam przekształcają się w komórki podporowe i formujące bliznę oraz wydzielają sygnały chemiczne kierujące tworzeniem naczyń i wzrostem mięśnia sercowego. U ludzi odpowiedź naprawcza ma tendencję do nadreakcji, co pozostawia grubą, trwałą bliznę. U danio jednak blizna jest przejściowa i stopniowo rozkładana, gdy zdrowy mięsień wraca. Zespół podejrzewał, że białko zwane fibuliną-2 (Fbln2), występujące w zrębie otaczającym serce, pomaga ustalać tempo i intensywność tej reakcji nasierdziowej.
Molekularny ściemniacz bliznowacenia
Wykorzystując edycję genów u danio, naukowcy stworzyli dwa rodzaje zwierząt o różnym poziomie Fbln2: szczep z obniżonym Fbln2 i drugi pozbawiony tego białka całkowicie. Uszkodzili serca ryb za pomocą sondy zamrażającej, naśladując zawał, i obserwowali proces gojenia przez tygodnie i miesiące. Gdy poziomy Fbln2 były obniżone, wczesne dzielenie się komórek mięśnia sercowego i komórek wyściółki naczyń spadało, lecz powstała włóknista blizna była mniejsza i łatwiej poddawała się przebudowie. Po trzech miesiącach serca te dobrze się zregenerowały i zachowywały niewiele kolagenu — głównego składnika blizny. Natomiast ryby całkowicie pozbawione Fbln2 wykazywały silniejsze stłumienie kluczowego szlaku wzrostu i bliznowacenia związanego z rodziną sygnałów TGFβ oraz miały znacznie mniej komórek tworzących bliznę tuż pod nasierdziem. Ich wczesne blizny również były mniejsze — lecz później te serca nie potrafiły usunąć kolagenu i kończyły z dużymi, trwałymi bliznami oraz słabą regeneracją.
Zbliżenie na zmiany stanu nasierdzia
Aby zobaczyć zachowanie komórek nasierdzia z rozdzielczością pojedynczych komórek, zespół zastosował sekwencjonowanie RNA pojedynczych komórek krótko po urazie. Zidentyfikowali kilka „stanów” komórek nasierdzia, w tym komórki w spoczynku, nowo uaktywnione, zestresowane adaptujące się do niskiego tlenu oraz komórki aktywnie dzielące się. U ryb z normalnym Fbln2 komórki nasierdzia płynnie przechodziły od stanu spoczynku do aktywacji i dalej do dojrzałych stanów. U ryb z obniżonym lub brakującym Fbln2 ten postęp zahamował się: komórki utknęły we wczesnych fazach, a bardziej dojrzałe grupy aktywowane były niedoreprezentowane, szczególnie w zwierzętach z całkowitym brakiem białka. Wiele genów, które normalnie włączają się podczas aktywacji nasierdzia i w odpowiedzi na sygnalizację TGFβ, zostało stłumionych, co wskazuje, że Fbln2 działa jako regulator tego szlaku decydujący o sile zaangażowania nasierdzia w formowanie i przebudowę tkanki bliznowatej.
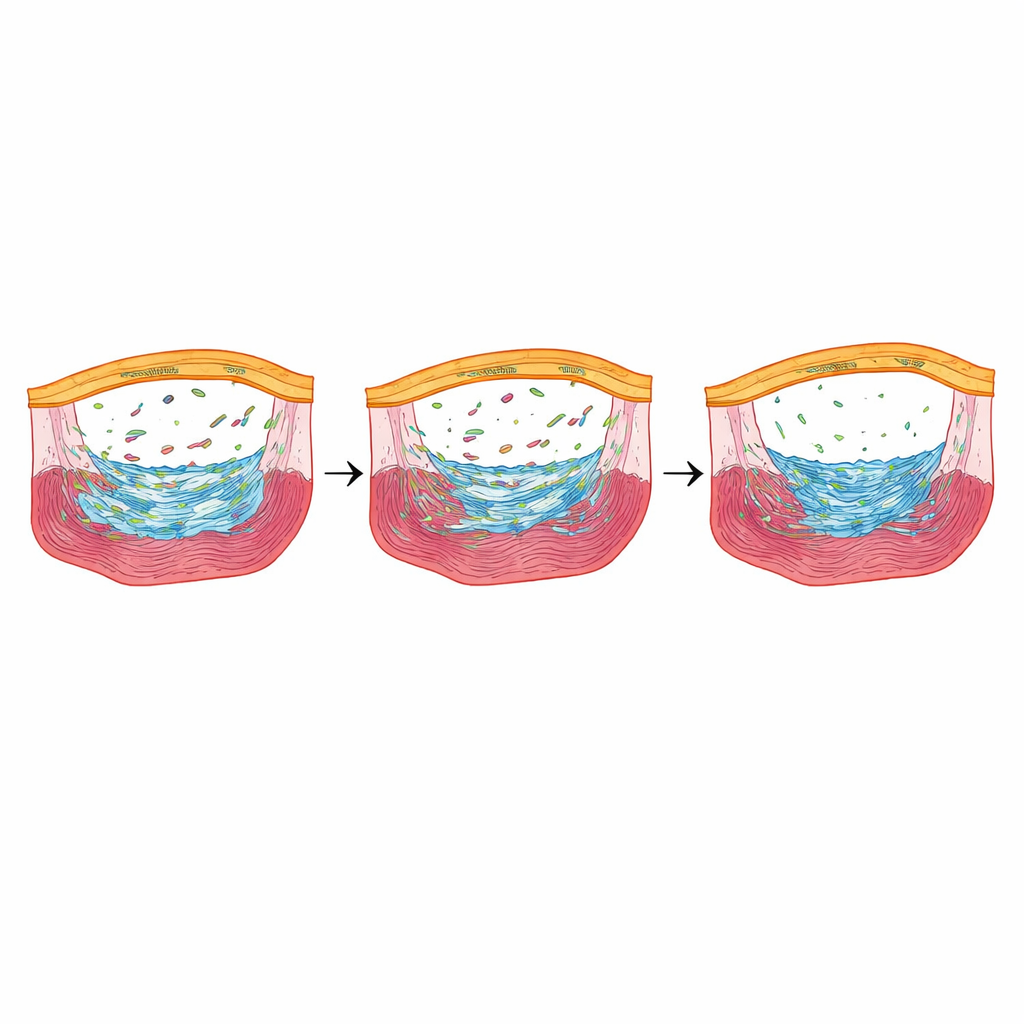
Reagujący na stres regulator, który dopracowuje naprawę
Wśród genów najsilniej zredukowanych przy obniżeniu Fbln2 wyróżniał się jeden: nupr1b, regulator reagujący na stres, aktywny w komórkach nasierdzia podczas wczesnego gojenia. Gdy badacze usunęli nupr1b, danio miały mniej nasierdziowych komórek formujących bliznę i zmniejszone dzielenie się komórek mięśnia sercowego, a miesiące po urazie utrzymywały duże depozyty kolagenu — podobnie jak ryby całkowicie pozbawione Fbln2. Co istotne, gdy krótkotrwale wymusili ekspresję nupr1b wyłącznie w komórkach nasierdzia ryb z obniżonym Fbln2, liczba komórek tworzących bliznę i proliferacja komórek mięśnia sercowego wróciły, a późne bliznowacenie zwiększyło się. Chemiczne zablokowanie receptorów TGFβ obniżało poziomy nupr1b, umieszczając nupr1b poniżej osi sygnalizacyjnej Fbln2–TGFβ.
Co to znaczy dla leczenia serca człowieka
Razem te wyniki ujawniają „epicardialną oś Fbln2–Nupr1b”, która pomaga sercom danio balansować między zbyt małym a zbyt dużym włóknieniem. Delikatne wyciszenie tej osi łagodzi wczesny wyrzut bliznowacenia i sprzyja efektywnemu usuwaniu blizny, podczas gdy całkowite jej wyłączenie psuje regenerację i pozostawia sztywną bliznę. W medycynie ludzkiej nauczka jest taka, że celem nie jest całkowite zablokowanie bliznowacenia, lecz jego regulacja — utrzymanie wystarczającej struktury, by zapobiec pęknięciu, przy jednoczesnym zapewnieniu, że tkanka bliznowata będzie przejściowa i może zostać zastąpiona zdrowym mięśniem. Zrozumienie i w przyszłości wykorzystanie tego systemu kontroli u danio może naprowadzić terapie, które skłonią uszkodzone ludzkie serce ku prawdziwej regeneracji zamiast przewlekłego bliznowacenia.
Cytowanie: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
Słowa kluczowe: regeneracja serca, włóknienie, danio pręgowane, nasierdzie, szlak TGF-beta