Clear Sky Science · pl
Interpretowalny model uczenia maszynowego do przewidywania rokowania w medulloblastomie integrujący cechy genetyczne i kliniczne
Dlaczego to badanie ma znaczenie dla rodzin
Dla rodzin, które stają w obliczu medulloblastomy — szybko rozwijającego się nowotworu mózgu dotyczącego głównie dzieci — jedno z najtrudniejszych pytań brzmi: „Jak będzie wyglądać przyszłość mojego dziecka?” Dzisiejsze plany leczenia opierają się często na szerokich grupach ryzyka, zamiast uwzględniać unikalne połączenie historii choroby, biologii guza i terapii radiacyjnej u każdego pacjenta. To badanie pokazuje, jak interpretowalna metoda uczenia maszynowego może połączyć te szczegóły, dając jaśniejsze, bardziej spersonalizowane prognozy dotyczące przeżycia długoterminowego, co może naprowadzić na bezpieczniejszą i skuteczniejszą opiekę.
Bliższe spojrzenie na częsty nowotwór dziecięcy
Medulloblastoma powstaje w móżdżku i stanowi około jednej piątej nowotworów mózgu u dzieci. Wielu dzieci przeżywa co najmniej pięć lat od rozpoznania, ale wyniki wciąż bardzo się różnią, zwłaszcza u pacjentów uznanych za wysokiego ryzyka. Standardowe leczenie zwykle obejmuje operację, a następnie radioterapię mózgu i rdzenia kręgowego, często z chemioterapią. Chociaż intensywne terapie mogą ratować życie, mogą też pozostawić u osób, które przeżyły, poważne długoterminowe problemy, takie jak trudności w nauce czy zaburzenia neurologiczne. Lekarze muszą więc znaleźć delikatną równowagę: zastosować wystarczającą terapię, by zapobiec nawrotowi guza, ale nie na tyle intensywną, by poważnie pogorszyć jakość życia.
Łączenie wielu informacji
Aby poprawić narzędzia prognostyczne, badacze zebrali jeden z największych dotąd zbiorów danych dla tej choroby. Skonsolidowali szczegółowe zapisy 729 osób leczonych w ośrodkach chińskich w latach 2001–2023 oraz 201 dodatkowych pacjentów z międzynarodowych współprac. Dla każdego pacjenta uwzględniono wiek, płeć, rozprzestrzenienie guza przy rozpoznaniu, mikroskopowy typ guza, wyniki operacji, dawkę radioterapii do mózgu i rdzenia, stosowanie chemioterapii oraz kluczowe cechy genetyczne guza, w tym aktywność genów takich jak MYC, MYCN, OTX2 i GFI1. Ponieważ nie wszystkie szpitale lub pacjenci mogą dostarczyć ten sam zakres danych, zespół zbudował cztery wersje modelu: jedną z danymi klinicznymi, molekularnymi i radioterapeutycznymi; jedną z danymi klinicznymi i molekularnymi; jedną z danymi klinicznymi i radioterapeutycznymi; oraz jedną używającą tylko podstawowych informacji klinicznych.
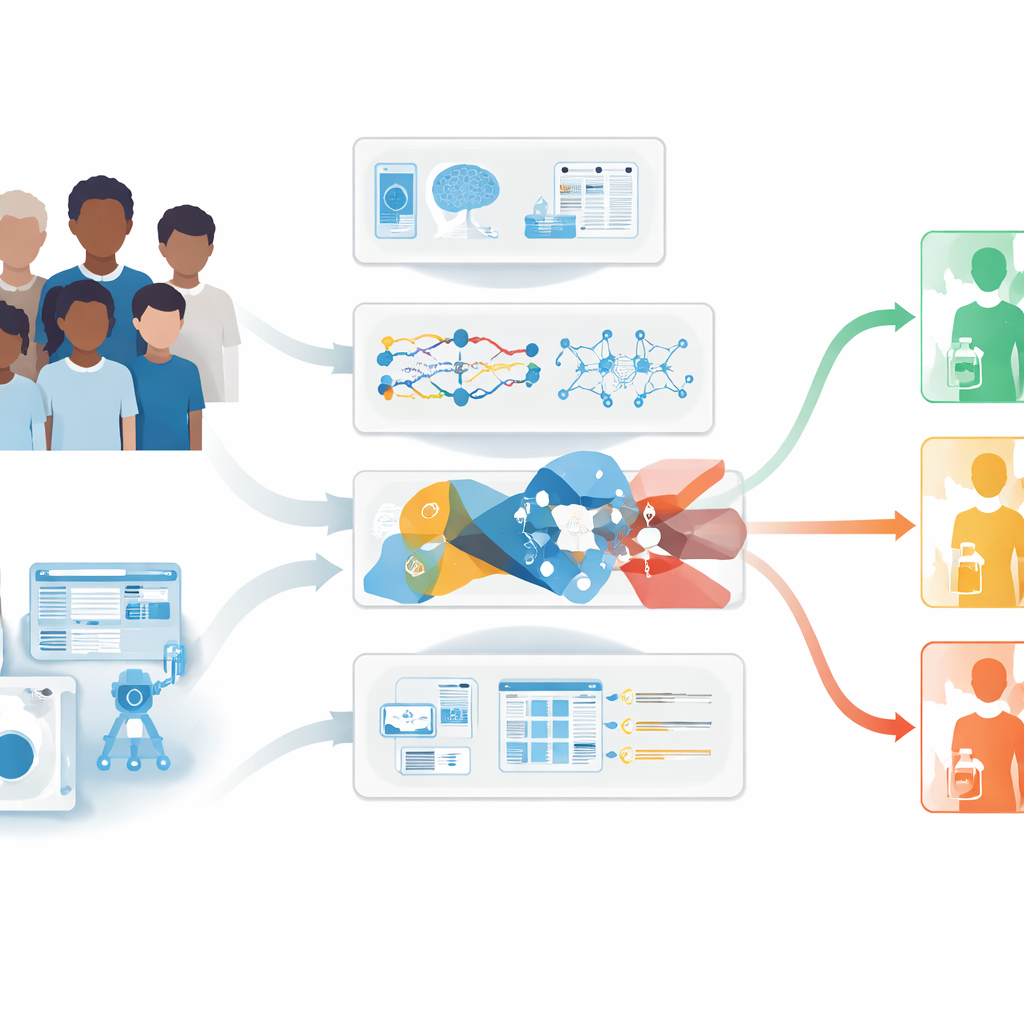
Jak uczenie maszynowe przekształca dane w prognozy
Zespół porównał sześć różnych algorytmów analizy przeżycia, aby sprawdzić, które najlepiej przewidują, jak długo pacjenci będą żyć po leczeniu. Metody te obejmowały tradycyjne podejścia statystyczne oraz nowocześniejsze techniki uczenia maszynowego, takie jak XGBoost i gradient boosting machines. Modele trenowano na części chińskiego zbioru danych i testowano na pozostałych pacjentach, a następnie sprawdzano ich wydajność ponownie przy użyciu kohorty międzynarodowej. W czterech scenariuszach danych modele XGBoost i gradient boosting generalnie dostarczały najbardziej wiarygodnych prognoz przeżycia ogólnego w perspektywie jednego, trzech, pięciu i dziesięciu lat, z dobrą zgodnością między prognozami a obserwowanymi wynikami. Co ważne, gdy dostępne były informacje molekularne i dotyczące napromieniania, dodanie tych danych poprawiało wyniki w porównaniu z poleganiem wyłącznie na danych klinicznych.
Co ma największe znaczenie dla rokowania
Ponieważ „czarne skrzynki” prognoz są trudne do zaufania w medycynie, badacze użyli techniki zwanej SHAP, aby rozłożyć na czynniki, jak każdy element wpływa na decyzje modelu. Analiza ta wyróżniła kilka zmiennych jako szczególnie wpływowe: czy nowotwór rozprzestrzenił się już w mózgu lub rdzeniu kręgowym, podgrupa molekularna guza oraz aktywność niektórych genów — w szczególności GFI1, MYC i MYCN. Wysoka aktywność niektórych z tych genów oraz obecność przerzutów wiązały się z gorszym przeżyciem. W aspekcie leczenia wyższe dawki promieniowania do loża guza w tylnej części mózgu były związane z lepszymi wynikami, a skojarzone napromienianie i chemioterapia również zmniejszały ryzyko w niektórych grupach. Pokazując, które cechy podnoszą lub obniżają ryzyko dla konkretnej osoby, system oferuje lekarzom i rodzinom bardziej przejrzysty wgląd w przyczyny danej prognozy.
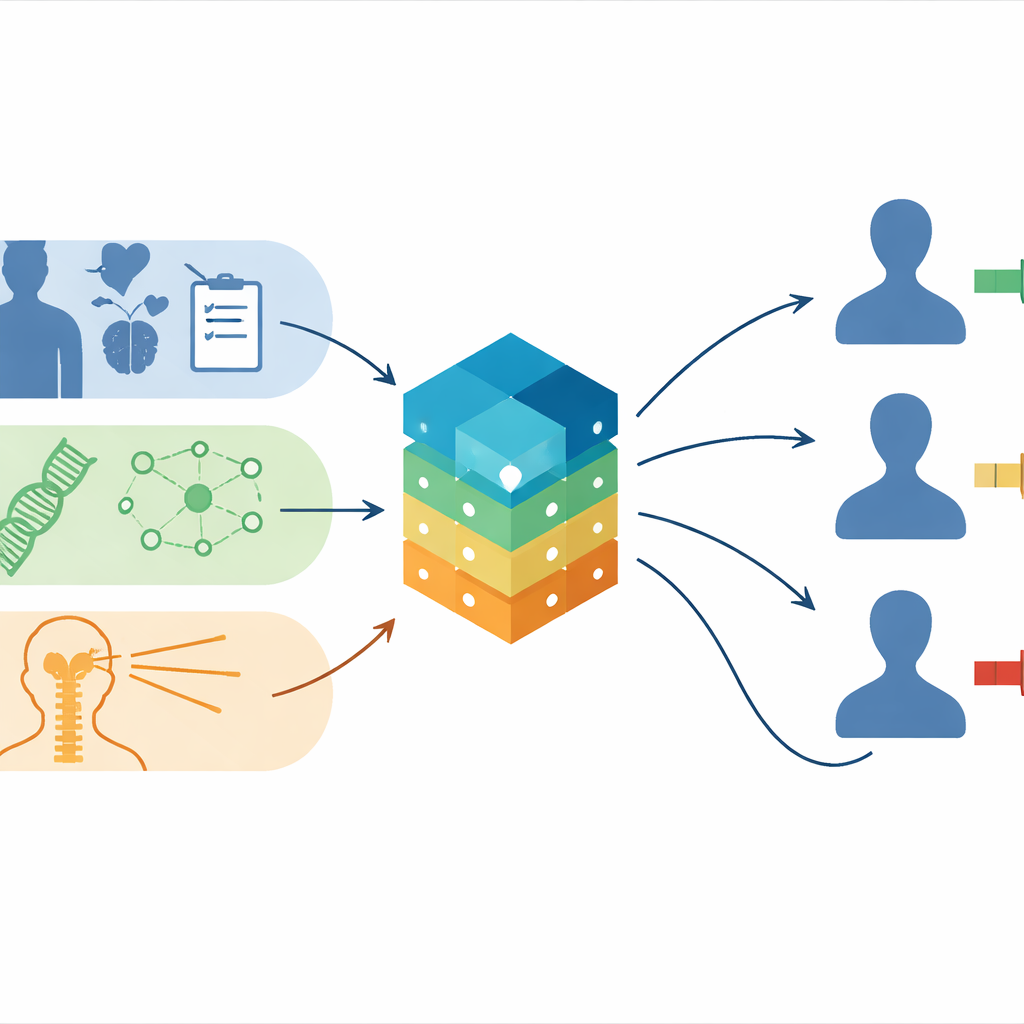
Przekształcanie złożonych modeli w narzędzia praktyczne
Aby pójść dalej niż teoria, autorzy stworzyli interaktywne aplikacje webowe oparte na swoich najlepiej działających modelach. Klinicyści mogą wprowadzać informacje takie jak wiek pacjenta, rozprzestrzenienie guza, podgrupa molekularna, dawka promieniowania i aktywność genów, jeśli są dostępne. Aplikacje wyświetlają następnie spersonalizowane krzywe przeżycia w czasie i pokazują, które czynniki najbardziej przyczyniają się do prognozy dla tego pacjenta. W sytuacjach, gdy brakuje danych molekularnych lub dotyczących dawki — co jest powszechne w ośrodkach o ograniczonych zasobach — prostsze wersje modelu wciąż mogą dostarczać użytecznych wskazówek, zapewniając inkluzywność podejścia.
Co to oznacza dla pacjentów i zespołów opiekuńczych
W istocie praca ta sugeruje, że starannie zaprojektowane, interpretowalne narzędzia uczenia maszynowego mogą pomóc przewidzieć, jak dzieci z medulloblastomą prawdopodobnie sobie poradzą, wykorzystując bogatszy obraz ich choroby niż dotychczas. Modele te nie zastępują sądu klinicznego i nadal wymagają dopracowania — zwłaszcza w przewidywaniu nawrotów guza — ale oferują sposób na lepsze dostosowanie rozmów o ryzyku, pewniejsze planowanie radioterapii i projektowanie opieki po leczeniu bardziej dopasowanej do sytuacji każdego dziecka. Dla rodzin może to oznaczać bardziej spersonalizowane decyzje i jaśniejszy obraz drogi przed nimi.
Cytowanie: Su, Y., Deng, K., Chen, X. et al. An interpretable machine learning model for predicting prognosis of medulloblastoma integrating genetic and clinical features. Commun Med 6, 134 (2026). https://doi.org/10.1038/s43856-026-01454-4
Słowa kluczowe: medulloblastoma, pediatric brain tumors, machine learning prognosis, radiotherapy dose, tumor genetics