Clear Sky Science · pl
Selektywne zablokowanie aktywacji utajonego TGF-β1 hamuje włóknienie tkanek przy dobrej tolerancji
Dlaczego ukryte bliznowacenie ma znaczenie
Wiele chorób przewlekłych cicho uszkadza narządy przez odkładanie sztywnej tkanki bliznowatej, proces zwany włóknieniem. To zmniejszanie funkcji może stopniowo upośledzać wątrobę, nerki, płuca, a nawet otaczać guzy, gdzie osłabia też skuteczność współczesnych immunoterapii przeciwnowotworowych. Białko TGF-β1 stoi w centrum tego procesu, ale jego globalne wyłączenie w organizmie okazało się niebezpieczne. W tym badaniu opisano nowe przeciwciało, nazwane SOF10, zaprojektowane tak, by blokować jedynie szkodliwą aktywację TGF-β1, przy zachowaniu jego niezbędnych funkcji, wykazując obiecujące efekty w modelach zwierzęcych chorób wątroby, niewydolności nerek i raka.
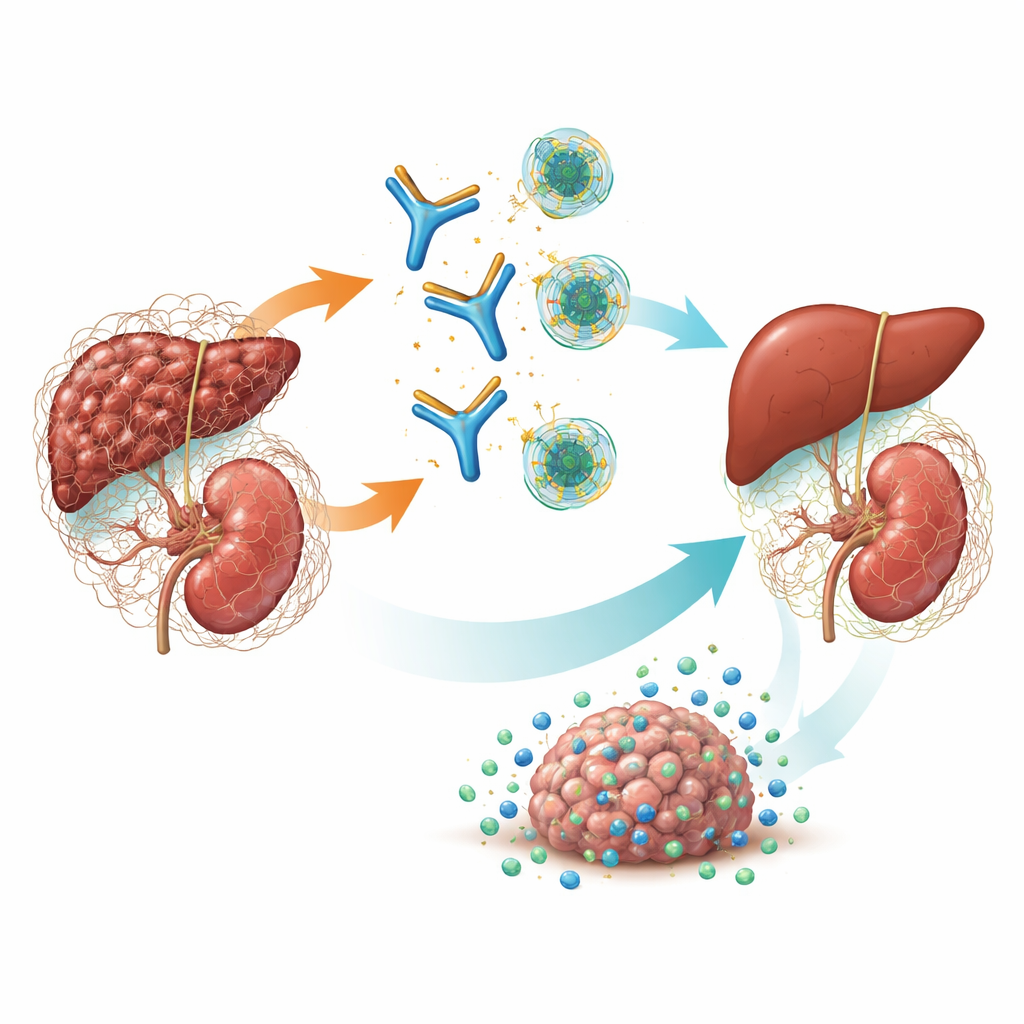
Główny przełącznik włóknienia i nowotworów
TGF-β to silna cząsteczka sygnałowa, która kontroluje wzrost komórek, gojenie i interakcje z układem odpornościowym. W chorobach przewlekłych jedna forma — TGF-β1 — pobudza fibroblasty do budowy nadmiaru tkanki łącznej, prowadząc do usztywnienia i niewydolności narządów. Tworzy też immunosupresyjną, włóknistą powłokę wokół guzów, która utrudnia komórkom odpornościowym i lekom dotarcie do komórek nowotworowych. Wcześniejsze leki próbowały jednocześnie wyłączyć wszystkie trzy formy TGF-β, ale taka „pan-blokada” powodowała poważne skutki uboczne, takie jak uszkodzenia zastawek serca, krwawienia i nowotwory skóry. Badania genetyczne i wcześniejsze modele wskazywały, że TGF-β1 jest głównym sprawcą włóknienia nerek i wielu nowotworów litych, co sugerowało, że precyzyjne ukierunkowanie tylko tego izoformy może być skuteczne i bezpieczniejsze.
Zablokowanie TGF-β1 w formie nieaktywnej
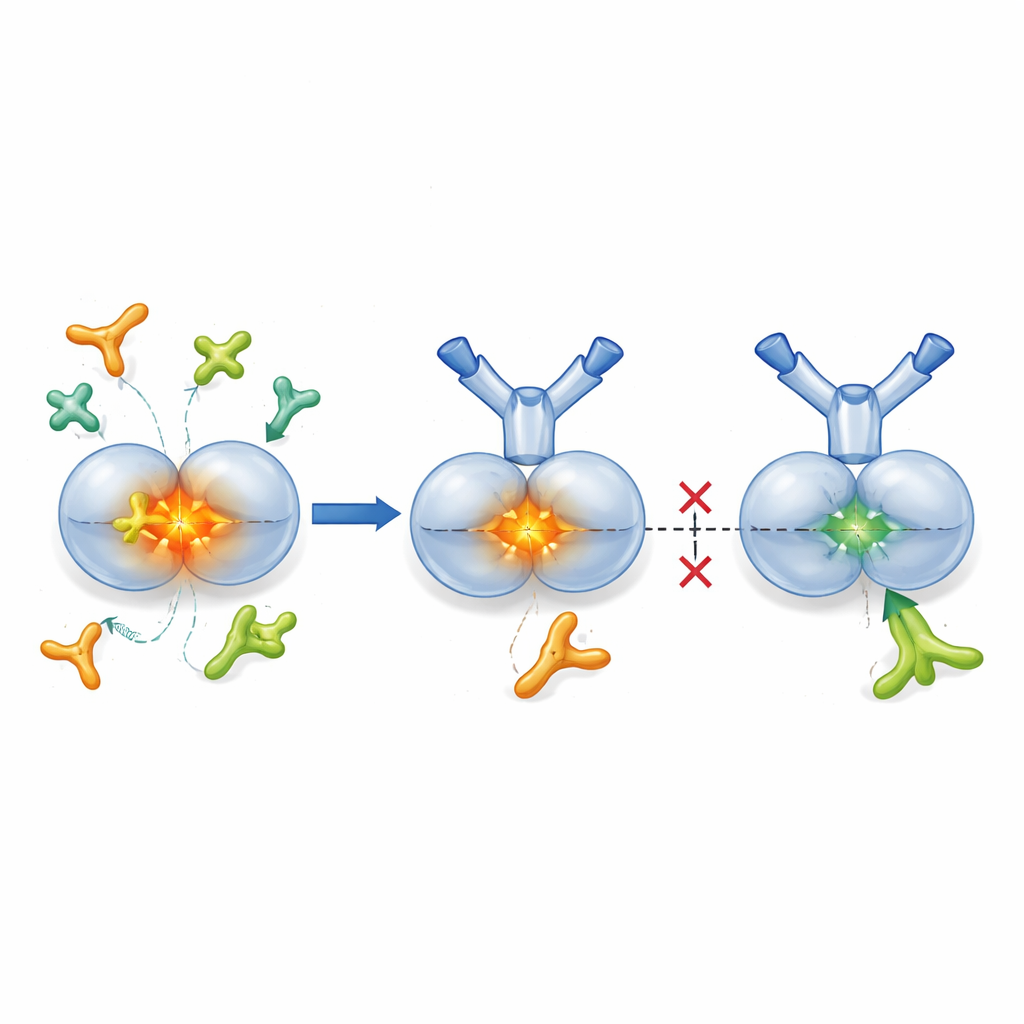
TGF-β1 jest zwykle wytwarzane w formie „utajonej”, w której aktywne jądro jest otoczone przez partnera białkowego, który utrzymuje je w stanie nieaktywnym do momentu potrzeby. Enzymy zwane proteazami i niektóre białka przytwierdzające się do powierzchni komórek, znane jako integryny, potrafią otworzyć ten pakunek, uwalniając aktywne TGF-β1 do otaczającej tkanki. Naukowcy skonstruowali SOF10, przeciwciało zhumanizowane, które wiąże jedynie utajoną formę TGF-β1, a nie aktywny hormon ani inne izoformy. Badania strukturalne z użyciem krystalografii rentgenowskiej wykazały, że SOF10 wciska się w interfejs między dwiema połówkami kompleksu utajonego, stabilizując go jak zacisk. W testach laboratoryjnych uniemożliwiało to proteazom i jednej integrynie (αvβ8) uwolnienie aktywnego TGF-β1, pozostawiając jednocześnie drugą integrynę (αvβ6) — istotną dla utrzymania równowagi immunologicznej w zdrowych tkankach — w dużej mierze nienaruszoną. W efekcie SOF10 selektywnie ucisza szkodliwe drogi aktywacji, oszczędzając kluczową ścieżkę homeostatyczną.
Ochrona wątroby i nerek przed przewlekłym uszkodzeniem
Aby sprawdzić, czy ten selektywny zacisk na TGF-β1 rzeczywiście może ograniczać bliznowacenie, zespół przetestował SOF10 w kilku modelach mysich. W szybkim modelu wywołanym dietą prowadzącym do stłuszczenia wątroby, które przechodzi w włóknienie, leczenie SOF10 zmniejszyło ekspresję genów odpowiedzi na TGF-β i genów budujących kolagen oraz obniżyło poziom hydroksyproliny, chemicznego markera nagromadzonej tkanki bliznowatej. W dwóch różnych modelach nerek — chirurgicznym modelu niedrożności wywołującym włóknienie śródmiąższowe oraz genetycznym modelu zespołu Alporta, w którym rozwija się zarówno bliznowacenie kłębuszków, jak i niewydolność nerek — SOF10 zmniejszało aktywność genów włóknieniowych, obniżało zawartość kolagenu i widocznie zmniejszało obszary zbliznowaceń pod mikroskopem. W przewlekłym modelu Alporta badania krwi wykazały poprawę funkcji nerek, a korzyści te były porównywalne z szerszym przeciwciałem blokującym TGF-β, lecz bez hamowania innych izoform TGF-β.
Uwolnienie układu odpornościowego wewnątrz guzów
Ponieważ włóknista tkanka otaczająca guzy może działać jako fizyczna zapora i immunologiczne hamulec, badacze sprawdzili, czy SOF10 może poprawić odpowiedź na leki hamujące punkty kontrolne. W mysich modelach raka piersi i okrężnicy, które zwykle słabo reagują na terapię anty–PD-L1, dodanie SOF10 istotnie spowolniło wzrost guza, podczas gdy SOF10 lub anty–PD-L1 podane osobno miały niewielki efekt. Guzy z myszy poddanych terapii skojarzonej zawierały więcej cytotoksycznych limfocytów CD8 i więcej toksycznych enzymów, których używają do niszczenia komórek nowotworowych. Fibroblasty pobrane z tych guzów wykazywały niższą aktywność szlaków budujących kolagen i macierz, ale wyższą aktywność szlaków interferonowych i prezentacji antygenu — przesunięcie w kierunku bardziej wspierającej odporność zrębu. Zmiany te zbliżone były do tych obserwowanych przy szerokiej blokadzie TGF-β, co sugeruje, że ukierunkowanie tylko utajonego TGF-β1 może podobnie przeprogramować mikrośrodowisko guza.
Sygnały bezpieczeństwa u zwierząt
Ponieważ wcześniejsze próby szerokiej blokady TGF-β napotkały problemy z bezpieczeństwem, zespół przeprowadził 13-tygodniowe badania toksyczności u myszy i małp koczkodanów cynomolgus, podając powtarzalnie wysokie dawki SOF10. Lek zachowywał się jak typowe przeciwciało we krwi, i w szerokim zakresie dawek nie zaobserwowano oznak uszkodzeń głównych narządów, zmian liczby komórek krwi ani zaburzeń funkcji serca i płuc. Najwyższe testowane dawki — do 200 mg/kg co dwa tygodnie u myszy i 100 mg/kg u małp — zostały uznane za poziomy bez obserwowanych szkodliwych efektów. Ten profil bezpieczeństwa wspiera hipotezę, że oszczędzanie TGF-β2, TGF-β3 i aktywacji zależnej od αvβ6 zmniejsza ryzyka widziane przy wcześniejszych, mniej selektywnych podejściach.
Co to może znaczyć dla pacjentów
Podsumowując, wyniki sugerują, że zablokowanie TGF-β1 w jego nieaktywnej otoczce — zamiast eliminowania całego sygnalizowania TGF-β — może złagodzić bliznowacenie w wielu narządach, poprawić funkcję nerek i uczynić oporne guzy bardziej podatnymi na immunoterapię, przy zachęcających wynikach bezpieczeństwa w testach na zwierzętach. Chociaż konieczne są badania kliniczne u ludzi, aby potwierdzić te korzyści i monitorować długoterminowe skutki, SOF10 i podobne strategie mogą otworzyć nową drogę leczenia przewlekłych chorób włóknieniowych i niektórych nowotworów, zmniejszając szkodliwe bliznowacenie przy jednoczesnym zachowaniu ról naprawczych i równoważących odporność, które tkanki nadal pełnią.
Cytowanie: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
Słowa kluczowe: włóknienie, TGF-beta1, przeciwciało monoklonalne, choroby nerek i wątroby, immunoterapia nowotworów